Am J Hematol综述:慢性淋巴细胞白血病的一线治疗
2022-09-27 聊聊血液 聊聊血液
慢性淋巴细胞白血病 (CLL) 是最常见的成人白血病,患者多为65-74岁,中位年龄70岁,因此身体素质可能介于非常fit到伴合并症的unfit以及frail,对于这些患者必须特别谨慎的选择治疗方案。
慢性淋巴细胞白血病 (CLL) 是最常见的成人白血病,患者多为65-74岁,中位年龄70岁,因此身体素质可能介于非常fit到伴合并症的unfit以及frail,对于这些患者必须特别谨慎的选择治疗方案。
WHO 将 CLL 归类为惰性 B 细胞淋巴瘤,但其病程可介于惰性到高侵袭性不等。部分遗传学和临床风险因素科可在治疗开始前预测病程的侵袭性,其中最具预后性的因素已被纳入 CLL-IPI,该加权评分包括年龄、Binet/Rai分期、β-2-微球蛋白、免疫球蛋白重链可变区基因 (IGHV) 突变状态和 TP53 状态,可将患者分层为不同总生存期的4个风险组。此外,未考虑治疗期间和治疗后的动态因素,如微小残留病 (MRD),因此,正在评价连续个体化风险指数 (CIRI),并适用于 CLL 的靶向治疗。目前的治疗策略纳入了deletion 17p(del17p)/TP53突变(mutTP53) 和未突变IGHV,作为更具侵袭性病程的指标。
为个体患者选择最佳方案时,建议考虑的参数包括临床分期、患者症状、fitness、合并症及遗传学风险因素等。
靶向药物的出现为CLL的一线治疗带来了巨大变化,其毒性通常是可以管理的,但也表现出特定的副作用,如伊布替尼和其他 BTK 抑制剂的心脏事件和出血,以及维奈克拉的肿瘤溶解综合征和感染,此外由于 BTK 抑制剂连续给药,还存在蓄积和副作用加重的风险。由于毒性,传统的化学免疫治疗是时间限制性方案,已知其与重度并发症(包括骨髓抑制、感染和继发恶性肿瘤)具有潜在相关性。总的来说,治疗医生在与患者一起做出个体化治疗决策时必须考虑所有方面。
一旦出现进行性骨髓衰竭或存在症状性/活动性疾病,应根据 iwCLL 指南给予治疗。而Binet(a或B)或 Rai (0-II) 分期较低的无症状患者观察等待,因为在该患者人群中治疗(伊布替尼或维奈克拉+奥妥珠单抗)尚未证实生存获益。
无del17p/mutTP53 CLL患者的一线治疗
IGHV突变的fit患者
fit患者的特征在于体能状态良好、合并症少和肌酐清除率良好等参数,如果患者IGHV突变且无 del17p/mutTP53则为低危。
对于 IGHV 突变的fit患者,最成熟且常用的靶向药物之一是连续 BTK 抑制剂无限期治疗。RESONATE-2 研究最初将伊布替尼与苯丁酸氮芥单药治疗作为一线治疗进行了比较,随访8年证实PFS和OS改善(7年PFS:伊布替尼59% vs.苯丁酸氮芥9%;伊布替尼未达到中位OS);然而苯丁酸氮芥已不再是 CLL 患者的标准治疗。对于老年和unfit患者,苯丁酸氮芥与 CD20 单抗联合使用可获得更好的疗效,如 CLL11研究所示。
E1912研究在<65岁年轻患者中比较了氟达拉滨、环磷酰胺和利妥昔单抗 (FCR,既往标准方案)与伊布替尼-利妥昔单抗。在随访5.8年的长期更新中,即使在 IGHV 突变亚组中PFS也存在显著差异(伊布替尼-利妥昔单抗组的5年 PFS 率为83%,FCR组为68%),但在该亚组中未获得 OS 获益。这些数据支持即使在一线治疗中也应考虑靶向药物,与遗传风险特征无关。
UK FLAIR研究在<75岁老年患者中比较了相同方案,但52.7个月时的首次数据未显示伊布替尼-利妥昔单抗和 FCR 之间有 OS 差异,但伊布替尼-利妥昔单抗的 PFS 改善(伊布替尼-利妥昔单抗未达到中位PFS vs. FCR 67个月)。
ALLIANCE A041202研究在≥65岁老年患者中比较了苯达莫司汀+利妥昔单抗 (BR) VS伊布替尼+利妥昔单抗VS伊布替尼单药治疗。结果基于伊布替尼的两种方案在PFS方面更优(所有患者的2年PFS:伊布替尼+利妥昔单抗组88%,伊布替尼组87%,BR组:74%),即使在 IGHV 突变亚组中也是如此(伊布替尼+利妥昔单抗组中位PFS未达到,伊布替尼组未达到,BR组51个月);这一结果也长于 IGHV 未突变亚组(伊布替尼+利妥昔单抗组中位PFS未达到,伊布替尼组未达到,BR组39个月)。然而靶向治疗和化学免疫治疗之间未显示 OS 差异;此外未观察到伊布替尼单药治疗与伊布替尼+利妥昔单抗之间的 PFS 有显著差异,因此添加该抗 CD20 单抗未改善缓解。
ILLUMINATE研究在unfit患者中评价了伊布替尼+奥妥珠单抗与苯丁酸氮芥+奥妥珠单抗,也获得了PFS获益(中位未达到vs. 49个月),但未显示 OS 差异。比较 ILLUMINATE 和 RESONATE-2研究之间的48个月 PFS 估计值,发现结果相似,伊布替尼单药组为74%,伊布替尼+奥妥珠单抗组为76%,因此在伊布替尼基础上加用抗 CD20 抗体似乎也无法改善结局,尽管第二项试验排除了 del17p 患者。根据这些数据可知,在伊布替尼基础上加用抗 CD20单抗不会产生额外疗效,因此不推荐使用。
另一种选择是二代 BTK抑制剂阿可替尼。ELEVATE TN研究在年龄≥65岁或18-65岁伴合并症的初治 CLL 患者中比较了阿可替尼(acalabrutinib)联合或不联合 奥妥珠单抗与苯丁酸氮芥+奥妥珠单抗。经过4年的长期随访,两个含阿可替尼组均未达到中位PFS,而奥妥珠单抗+苯丁酸氮芥组为27.8个月;在 IGHV 突变组中,所有治疗组均未达到中位PFS:阿可替尼+奥妥珠单抗组48个月 PFS 率为89%,而阿可替尼单药组为81%,奥妥珠单抗+苯丁酸氮芥组为62%。在事后分析中比较阿可替尼+奥妥珠单抗与阿可替尼单药时,也观察到 PFS 延长;尽管该研究效力不足以进行该比较,但加用奥妥珠单抗似乎可改善缓解,在启动阿可替尼治疗时应予以考虑。
ELEVATE RR研究在复发/难治性 CLL 患者中比较了伊布替尼与阿可替尼,结果显示疗效相似,两组的中位 PFS 均为38.4个月,但中位OS未达到。关于副作用,应特别考虑将阿可替尼用于心脏疾病患者,因为阿可替尼治疗的所有级别房颤/房扑发生率均显著更低(9.4% vs. 伊布替尼16.0%)。一般而言阿可替尼似乎耐受性更好,因为阿可替尼组14.7%和伊布替尼组21.3%因不良事件中止治疗。
另一种比伊布替尼脱靶效应更少的二代 BTK 抑制剂是泽布替尼。在 SEQUOIA 研究中,泽布替尼一线治疗的24个月 PFS 优于BR (85.5% vs 69.5%),而24个月 OS 相似(94.3%和94.6%);在 IGHV 未突变患者中有治疗获益,但在 IGHV 突变患者中未观察到治疗获益。
所有 BTK 抑制剂均为连续治疗,必须使用至出现不可耐受的毒性或进展,可能导致累积性远期副作用。因此在真实世界环境中,伊布替尼治疗17个月后记录的停药率较高(41%-49%),主要归因于毒性。鉴于现有 BTK 抑制剂的良好疗效,将来的主要议题,可能是如何针对患者需要的不同毒性特征进行个体化治疗,而非确定疗效最佳的 BTK 抑制剂。
患者也可以接受为期12个月的 维奈克拉+奥妥珠单抗固定时间治疗。CLL14研究在共存疾病(定义为累积疾病评定量表>6、肌酐清除率30-69 mL/min 或两者)的初治患者(包括具有高危遗传学特征的患者)中评价了该方案。经过39.6个月的长期随访,接受 维奈克拉+奥妥珠单抗治疗的患者的中位PFS显著长于苯丁酸氮芥+奥妥珠单抗(维奈克拉+奥妥珠单抗的中位PFS未达到;苯丁酸氮芥+奥妥珠单抗35.6个月)。在 IGHV 突变亚组中,维奈克拉+奥妥珠单抗的中位 PFS同样延长(未达到vs.苯丁酸氮芥+奥妥珠单抗54.5个月),但未显示 OS 获益。
该联合治疗也获批用于fit患者的一线治疗。CLL13 研究的首批数据显示,在一线治疗中比较维奈克拉+奥妥珠单抗与 FCR 或 BR 时,fit CLL患者获得了令人鼓舞的结果。第一项协同主要终点分析显示,第15个月时外周血中MRD无法检测(uMRD) 的比率优于化学免疫治疗 (86.5% vs. 52.0%)。在 EHA 2022 上展示的最新数据表明,uMRD的高发生率可转化为更长的PFS(第二共同主要终点)。随访38.8个月时,在所有患者中,维奈克拉+奥妥珠单抗组的3年 PFS 率 (87.7%) 优于 FCR 或 BR 组 (75.5%),但IGHV突变患者的差异较小,维奈克拉+奥妥珠单抗组为93.6%,FCR或 BR 组为89.9%。虽然OS结果仍有待确定,但基于长期数据,低危患者仍可在个体基础上考虑化学免疫治疗;然而靶向药物提供了大量证据,支持即使在低危患者中,靶向药物也优于使用化学免疫治疗。
IGHV未突变的fit患者
IGHV 未突变患者预后不良,生存率较短。在 RESONATE-2 研究中随访5年后,伊布替尼组IGHV未突变患者的 PFS 为67%,而苯丁酸氮芥组为6%;即使随访8年后,伊布替尼组IGHV突变和未突变患者的 PFS 也相似。
E1912 研究中,与化学免疫治疗相比,接受伊布替尼+利妥昔单抗治疗的 IGHV 未突变患者的5年 PFS 率为75%,而 FCR 为33%,5年 OS 也差异显著(伊布替尼+利妥昔单抗95% vs. FCR 84%)。此外在 FLAIR 研究的老年患者人群中也观察到 PFS 差异。同样,在 Alliance A041202 研究的老年患者人群中,IGHV未突变患者在中位随访33.6个月后,伊布替尼和伊布替尼+利妥昔单抗治疗的中位PFS未达到,而 BR 为39个月。
ELEVATE TN 研究随访4年后,IGHV 未突变患者给予含阿可替尼治疗的中位PFS未达到,而奥妥珠单抗+苯丁酸氮芥组为22.2个月。阿可替尼+奥妥珠单抗的48个月 PFS 率为86%,阿卡替尼单药为77%,而苯丁酸氮芥+奥妥珠单抗仅有4%。
泽布替尼在IGHV未突变患者中也显示治疗获益。中位随访26.2个月, 泽布替尼较BR可显著延长PFS (HR= 0.42, P<0.0001),包括IGHV未突变患者(HR= 0.24, P<0.0001),但IGHV 突变患者无统计学差异(HR= 0.67, P=0.0929)。泽布替尼和BR预估24个月PFS率分别为85.5%和69.5%,IRC 评估的ORR分别为94.6%和85.3%,CR率分别为6.6%和15.1%,预估24个月 OS 分别为94.3%和94.6%。
在 CLL14 研究中,尽管在随访39.6个月后,维奈克拉+奥妥珠单抗的固定持续时间治疗方案较苯丁酸氮芥+奥妥珠单抗延长了IGHV未突变患者的中位PFS(分别为57.3个月和26.9个月),但结局仍劣于IGHV突变患者。在 OS 方面,IGHV未突变亚组则未观察到差异。
鉴于与化学免疫治疗相比靶向药物可延长 PFS, IGHV未突变患者应首选靶向药物。
Unfit患者
由于合并症,unfit患者应接受侵袭性较低的治疗方案,可能选择包括 BTK 抑制剂,尤其是更新的药物,如阿卡替尼,因其毒性特征更好,或维奈克拉+奥妥珠单抗。与苯丁酸氮芥+奥妥珠单抗相比,维奈克拉+奥妥珠单抗作为固定持续时间方案在伴合并症患者中显示 PFS 延长,但 OS 未延长。同样,与苯丁酸氮芥+奥妥珠单抗相比,伊布替尼+奥妥珠单抗以及阿可替尼+奥妥珠单抗均可改善PFS,但未延长 OS。
因此还应考虑其他因素,如合并症负担和可能的副作用,以及连续与固定持续时间治疗的选择,这可能限制个体患者的选项。在不同临床试验的汇总分析中,靶向药物治疗在≥80岁伴合并症的frail患者中也是可行和有效的。这些frail患者在历史上通常被认为症状控制和可行性应是主要目的,但在靶向药物的重点研究中,患者甚至获得了与年龄和性别匹配人群相当的生存期。
Del17p/mutTP53 CLL患者的一线治疗
del17p/mutTP53患者具有侵袭性病程,通常对化疗免疫疗法反应不佳。尽管最终的治疗方法尚未确定,但靶向抑制剂已显示出更好的疗效,应推荐使用(不考虑身体素质)。
伊布替尼持续治疗在一线治疗中显示了可喜的结果。在一项仅评价 del17p 或 mutTP53 患者的2期研究中中位 PFS 和OS均未达到,估计的6年 PFS 为60%、OS 为79%。在另一项 II 期研究中,接受伊布替尼治疗的 TP53 改变患者的中位至进展时间为53个月。一项研究比较伊布替尼和伊布替尼+利妥昔单抗与 BR ,结果在中位随访38个月后中位PFS无法估计,而BR为7个月。在 ILLUMINATE 研究(伊布替尼+奥妥珠单抗)的最终分析中,del17p或 mutTP53 患者的48个月 PFS 率估计为74%,而不伴 del17p 或 mutTP53 患者为77%。
CLL14 试验中,接受 维奈克拉+奥妥珠单抗治疗的 del17p/mutTP53 患者的中位PFS(49.0个月)显著长于接受苯丁酸氮芥+奥妥珠单抗(20.8个月)。疾病进展患者维奈克拉-+奥妥珠单抗再治疗正在 ReVenG 研究 (NCT04895436) 中进行。
PI3K 抑制剂 idelalisib 联合利妥昔单抗在高危 CLL 中也显示出活性,但应慎用,只有在存在 BTK 抑制剂和 维奈克拉 禁忌症的情况下才考虑用于高危CLL,原因在于其非常严重的副作用,如致死性和/或严重感染、肝毒性、腹泻或结肠炎、肺炎和肠穿孔,只能作为最后选择进行讨论。
130例 TP53 功能障碍患者的一项回顾性研究中,患者在一线治疗中接受了 BTKi 联合/不联合 维奈克拉 和联合/不联合 CD20 抗体, 4年结局良好,接受双联或三联治疗的患者结局非常好。
CLL16 研究目前正在招募具有复杂核型或 del17p/mutTP53 的高危 CLL 患者,旨在比较 维奈克拉+奥妥珠单抗与维奈克拉+奥妥珠单抗+阿可替尼三联治疗14个月,并在MRD可检测的情况下再进行10个周期的阿可替尼治疗 (NCT05197192)。
然而高危患者即使接受靶向治疗,最终也会进展,除异基因干细胞移植外CLL仍无治愈方法,而在哪种治疗线之后给予异基因干细胞移植仍需要根据个体情况讨论,因为其死亡率和发病率较高。
拟定的治疗策略
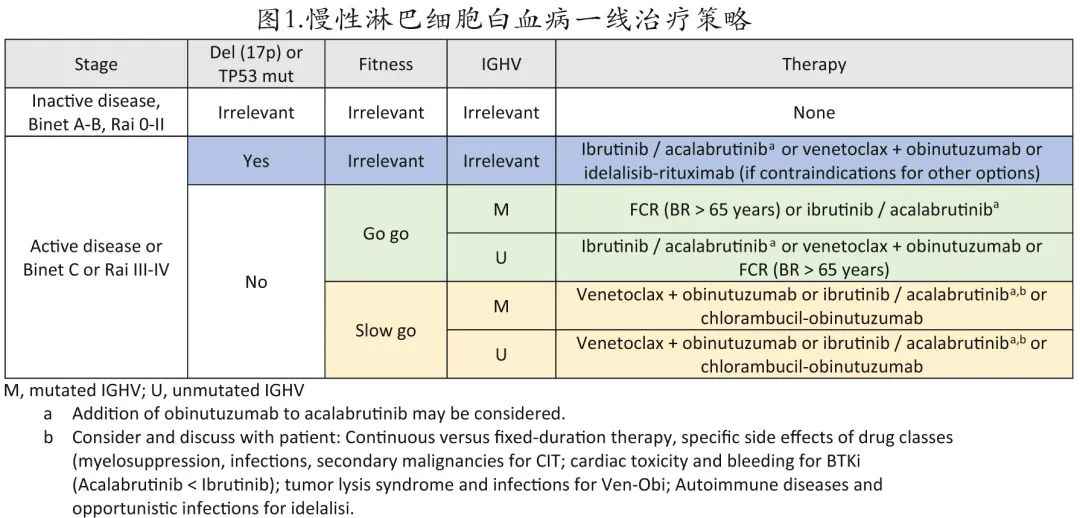
Hallek 和 Al-Sawaf 提出的治疗策略改编版本如图1所示,如果存在相关合并症或禁忌症应进行调整。一般而言应根据fitness以及 TP53 和 IGHV 状态对患者进行分层:IGHV 突变且无 del17p 或 mutTP53 的患者最好接受 维奈克拉+奥妥珠单抗治疗。由于副作用更优,大多数患者偏好靶向药物治疗,但化学免疫治疗仍可能是低危患者的可选方案。由于 E1912 研究显示 OS 改善,因此可优先给予IGHV 未突变的fit患者BTK 抑制剂,如伊布替尼或阿可替尼。
在合并症方面,IGHV突变或未突变的unfit患者可给予维奈克拉+奥妥珠单抗或 BTK 抑制剂。Frail和高龄患者多重用药风险较高,疗效和毒性之间的平衡高度相关,应避免住院治疗,阿可替尼可能是可行的选择。对于伴 del17p 或 mutTP53 的高危患者,BTK抑制剂治疗更佳,而在决定首选这两种药物中的哪一种时,除患者因素外,还应考虑偏好几个因素,如心脏合并症、合并用药,如抗凝剂和质子泵抑制剂以及给药频率;如果需要快速降低肿瘤负荷,可考虑在阿可替尼基础上加用奥妥珠单抗。
但由于尚未对 BTK 抑制剂连续治疗与基于固定持续时间的静脉给药方案进行直接比较,因此无法明确推荐应首选哪种治疗。这个问题目前正在德国 CLL 研究组 (NCT04608318) 的 CLL17 研究中探索,该试验比较了伊布替尼与 维奈克拉+奥妥珠单抗和维奈克拉+伊布替尼,但该研究仍在开放招募。
展望
口服抑制剂拓宽了 CLL 患者的治疗可能性,可以在更多的个体基础上做出选择。除了使用不同的 BTK 抑制剂进行连续治疗外,还引入了固定持续时间的治疗,从而可能限制相关毒性;维奈克拉+奥妥珠单抗是首个被批准用于 CLL 一线治疗的固定时间靶向治疗方案。随着治疗时间的延长,耐药相关突变的风险增加,在继续治疗的进展中,获得性继发性耐药将占大多数,需要进一步研究固定持续时间复方制剂。
另一种有前景、仍为时间限制性的联合方案是仅由口服药物组成的维奈托克+伊布替尼。高危和老年 CLL 患者在一线接受伊布替尼单药治疗3个月后联合维奈克拉治疗24个月,估计1年 PFS 为98%,OS为99%。
CAPTIVATE 研究入组 MRD 队列和单独的固定持续时间队列。在固定持续时间队列中,年龄≥18岁且≤70岁的患者接受3个周期的伊布替尼单药治疗,随后12个月的维奈克拉联合治疗,该队列的总体 CR 率为55%,24个月 OS 为98%。在所有患者中估计的24个月 PFS 率为95%,在 del17p/mutTP53 患者中也可达84%。在 MRD 驱动治疗组,在12个联合治疗后随机分配至安慰剂组的达到 uMRD 的患者的1年无病生存率为95%、伊布替尼组为100%,而安慰剂组估计30个月 PFS 率为95%、伊布替尼组为100%。
GLOW 研究还显示,与苯丁酸氮芥+奥妥珠单抗相比,伊布替尼+维奈克拉治疗后MRD阴性率更高(骨髓:51.9% vs. 17.1%;外周血:54.7% vs. 39.0%)。不管uMRD还是MRD 可检测的患者,伊布替尼+维奈克拉组治疗结束后前12个月内的 PFS 率均高于90%。然而在伊布替尼导入期报告了4例死亡,因此关于安全性数据中应谨慎,提示选择特定 BTK 抑制剂时应考虑合并症,尤其是老年患者人群。
一线 CLL 的时间限制性方案目前仅获批为固定持续时间治疗,而MRD驱动的治疗尚不推荐在临床实践中使用。
目前有多项研究正在测试 MRD 指导的方案(伊布替尼+维奈克拉)用于个体化治疗持续时间,但如果试图证明 MRD 驱动的方案优于固定持续时间方案,则必须在 III 期试验中进行评价。
三联方案在2期研究中也显示了可喜的结果。一项研究评估了奥妥珠单抗+伊布替尼+维奈克拉三联治疗14个周期,结果显示36个月 PFS 估计值为95%。奥妥珠单抗+阿可替尼+维奈克拉联合给药直至第16周期第1天,uMRD时可选择停止治疗,或直至第25周期第1天,结果骨髓uMRD完全缓解率为38%。
在一项MRD驱动方案中比较奥妥珠单抗+泽布替尼+维奈克拉的研究中,中位治疗持续时间10个月和中位随访25.8个月后,89%的患者血液和骨髓中均达到 uMRD。
靶向药物的三联组合是否可能显著改善结局,或毒性和耐药性的早期发展会限制这一方案?目前正在 III 期研究中进行评估。EA9161研究在初治患者中比较伊布替尼+奥妥珠单抗与伊布替尼连续治疗与固定持续时间伊布替尼+维奈托克+奥妥珠单抗治疗<70岁患者(NCT03701282),结果待定。MRD 驱动下在14个月后终止伊布替尼的类似设计仍在招募≥70岁的老年患者 (NCT03737981)。在3期 CLL13 研究中,维奈克拉+奥布替尼+奥妥珠单抗三联治疗的 uMRD 率更高,PFS最长,但毒性也更大(如3-4级感染)。只要疗效超过风险,更长时间的随访将提供更明确的信息。
随着多种选择和新的有希望的药物即将到来,CLL治疗的未来看起来很光明。接下来需要在 CLL 患者的异质性人群中进一步研究双重难治患者或由于药物相互作用或合并症而不适合靶向药物的患者的治疗,以及治疗选择的最佳顺序。此外应与患者讨论是否参与临床试验,而靶向药物治疗的全球可及性也应是积极推进的共同目标。
参考文献
Nadine Kutsch, Anna Maria Fink, Kirsten Fischer .Management of front line chronic lymphocytic leukemia.Am J Hematol . 2022 Nov;97 Suppl 2:S3-S10. doi: 10.1002/ajh.26677.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言