特定蛋白相关指标在糖尿病肾脏病防治中怎么用?
2022-09-21 检验之声 检验医学网
糖尿病肾脏病:是糖尿病最主要的微血管并发症之一,是目前引起终末期肾病(end-stage renal disease,ESRD)的首要原因。
糖尿病肾脏病(diabetic kidney disease,DKD)是糖尿病最主要的微血管并发症之一,是目前引起终末期肾病(end-stage renal disease,ESRD)的首要原因。
据统计,我国DKD在终末期肾病中占16.4%。国外报道20%~40%的糖尿病患者合并DKD,国内2型糖尿病患DKD患病率为10%~40%。与不合并DKD 的糖尿病患者相比,DKD患者死亡率更高,且大部分死亡是由于心血管事件导致。早期诊断、预防与延缓DKD的发生发展,对降低心血管事件的发生、提高患者存活率、改善生活质量具有重要意义。
一、DKD的定义与临床诊断
根据《糖尿病肾脏病诊治专家共识(2020)》:
DKD的定义:是糖尿病患者的常见慢性并发症之一,是指由糖尿病引起的慢性肾脏病 (CKD),表现为尿蛋白水平升高(尿白蛋白肌酐比值≥30mg/g)和(或)估算肾小球滤过率(eGFR)<60ml·min-1·1.73m-2并持续超过3个月,同时排除其他病因CKD而作出的临床诊断。
DKD的临床诊断:在排除其他原因导致的CKD前提下,T1D和T2D患者出现微量白蛋白尿(尿白蛋白肌酐比30-300mg/g)或大量白蛋白尿(尿白蛋白肌酐比≥300mg/g)或eGFR下降,若同时合并有糖尿病视网膜病变,可以临床诊断DKD。
该共识强调:DKD是排除性的临床诊断,大部分是基于患者临床表现而做出的诊断。因此,当糖尿病患者出现蛋白尿,特别是仅出现微量白蛋白尿时,需联合其他指标诊断DKD。
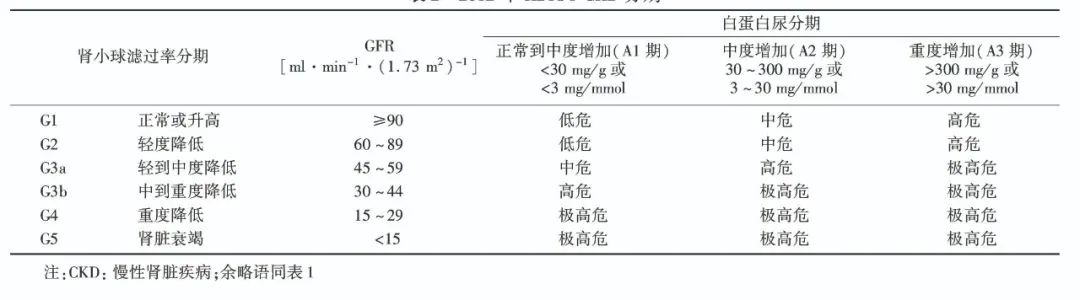
《中国成人糖尿病肾脏病临床诊断的专家共识(2015)》提出“完整DKD临床诊断的建议”:鉴于糖尿病的肾脏损害累及全肾,建议完整的 DKD 诊断应该包括:肾小球病变(临床分期参照2012年KDIGO指南,如诊断为 G1A1,见表1)、肾小管病变、肾脏形态、肾血管四个方面。
表1. 2012年KDIGO CKD分期
 二、DKD的筛查
二、DKD的筛查
《中国成人糖尿病肾脏病临床诊断的专家共识2015》建议:
所有糖尿病患者首次就诊时都应筛查CKD,如:尿沉渣、GFR、尿白蛋白与肌酐比值(ACR)与肾脏超声检查。
1.肾小球受累的早期筛查
(1) 初始筛查的时机为:
●1型糖尿病患者病程≥5年;
●2型糖尿病患者确诊时;
●无CKD者每年1次筛查。
(2) DKD筛查指标应包括:
①任意时点的尿标本(清晨首次尿最佳)检测 ACR评估尿白蛋白排泄;
②测量血肌酐值,并计算eGFR。
注意事项
①尿白蛋白排泄受多种生理或病理因素的影响,如24h内的剧烈运动、长时间站立、感染(尤其是泌尿系统感染)、发热、慢性心力衰竭、血糖过高、血压过高、血脂过高等。推荐在排除上述临床情况后,再筛查ACR。
②推荐DKD的诊断或A分期应当以3~6个月内的2~3次ACR结果作为基础。
2.肾小管受累的早期筛查
(1) 筛查时机:
推荐对G3A~5A1期DKD患者,即尿白蛋白阴性的DKD患者,进行肾小管受累的筛查。
(2) 筛查指标:
推荐采用任意时点(清晨首次尿最佳)尿标本测定α1-MG。文献中报道的临床评估指标包括:测定尿液中近端肾小管损害标志物α1-MG、β2微球蛋白(β2 -MG) 、视黄醇结合蛋白(RBP) 、中性粒细胞明胶酶相关脂质运载蛋白(NGAL) 、肾损伤分子1( Kim-1) 、肝脏型脂肪酸结合蛋白(L-FABP) 、N-乙酰-β-D-氨基葡萄糖苷酶(NAG)及远端肾小管损害标志物心脏型脂肪酸结合蛋白(H-FABP)等。
(3)注意事项:排除影响因素,依据2~3次结果判定。
3.肾脏血管受累的早期筛查
可使用彩色多普勒超声评估肾内血流动力学变化情况,测量肾微小动脉血流参数。
三、DKD的评估
根据《中国糖尿病肾脏疾病防治临床指南(2019)》,DKD的评估指标有:
1.尿白蛋白
推荐采用随机尿测定UACR反映尿白蛋白的量。随机尿UACR≥30mg/g为尿白蛋白排泄增加,即白蛋白尿。在 3~6个月内重复检查UACR,3次中有2次尿白蛋白排泄增加,排除感染等其他因素即可诊断白蛋白尿。白蛋白尿作为诊断依据时,需进行综合判断,多次检测并结合eGFR长期随访,且需排除其他可引起白蛋白尿的病因。
2.eGFR
肾功能改变是DKD的重要表现,反映肾功能的主要指标是GFR。计算eGFR采用的常见参数包括年龄、性别、血清肌酐浓度,推荐使用CKD-EPI公式或MDRD公式。当患者eGFR<60 ml·min-1·1.73 m-2时,可诊断为eGFR下降。但eGFR检测值可能有波动,当出现下降时应复查,以明确DKD分期。
值得一提的是,《老年慢性肾脏病诊治的中国专家共识(2018)》指出,对60岁以上老年人群的研究显示,与Cockcroft-Gault公式、肾脏病饮食改善研究公式相比,CKD-EPI公式表现出更好的准确性。与Scr相比,血清胱抑素C水平受肾外因素的影响相对较少,基于血清Scr和胱抑素C的联合公式(CKD-EPIcr-cyst)较单纯基于血清Scr的公式(CKD-EPIcr)估算eGFR更加准确。
建议:2型糖尿病和病程5年以上的1型糖尿病患者每年应至少进行一次UACR和eGFR 检测,以便早期发现DKD。
3.除肾小球外,DKD还可累及肾小管和肾间质
有条件时,可对DKD患者的肾小管受累情况进行临床评估,相关指标包括:尿α1-微球蛋白、β2-微球蛋白等。
除上述指标外,《中国成人糖尿病肾脏病临床诊断的专家共识(2015)》还强调对DKD肾小管受累的临床评估。
4.虽然DKD以肾小球系膜细胞病变为主,但也可累及肾小管肾间质,除肾小球外,DKD还可累及肾小管和肾间质
研究发现,肾小管间质病变与DKD肾脏功能恶化的相关性较肾小球病变更为密切;肾小管损伤在DKD 早期即可出现,且可先于肾小球病变。因此推荐对DKD 患者的肾小管受累情况也进行临床评估。可依据所在医院条件,选择如尿α1微球蛋白(α1-MG)等指标检测。
DKD常可出现其他血管病变,也会出现CKD的各种并发症,为了改善患者不良预后和减少患者病死率,故该共识还推荐对DKD的肾外病变进行评估。
5.心脑血管疾病(CCVD)及风险
DKD患者CCVD风险明显高于单纯的糖尿病或non-DKD患者,同时CCVD也是DKD患者死亡的首要原因。对于DKD患者,至少每年评估一次CCVD 风险。评估具体内容应包括:CCVD病史、年龄、有无CCVD危险因素(吸烟、脂代谢紊乱、糖代谢紊乱、高血压及家族史、腹型肥胖)、肾脏损害程度(尿白蛋白排泄率及GFR下降水平) 、房颤(可致卒中) 、颈动脉狭窄(可致卒中) 。
6.营养状态
DKD 患者营养不良的发生率较高,同时营养状况也是影响DKD患者预后的重要因素之一。
当GFR<60 ml·min-1·1.73m-2时,发生营养不良的风险明显增高,因此建议将此定为筛查的起始时机,监测频率应根据营养不良风险而定。
DKD营养状态综合评定的内容如下:(1)人体测量:体重指数、肱三头肌皮褶厚度和上臂围等;(2)生化指标:血清白蛋白、前白蛋白、转铁蛋白等指标;(3)通过主观综合营养评估(SGA) 量表评定,并给出SGA评分等级。
7.当 GFR<60 ml·min-1·1.73m-2时,还需对CCVD、营养不良以外的其他CKD并发症进行评估
包括代谢性酸中毒、电解质紊乱、贫血、慢性肾脏疾病-矿物质-骨代谢异常(CKD-MBD)、继发性甲状旁腺功能亢进等,具体评估指标、评估时机、监测频率详见表2。
表2 .糖尿病患者CKD的管理

除专家共识中的上述指标外,临床上常用于慢性肾脏病的标志物还有:尿转铁蛋白、尿IgG、尿α2巨球蛋白等。
尿转铁蛋白
尿TRF/Cr在糖尿病正常尿蛋白组即表现出异常增高,表明TRF/Cr能更敏感地反映肾小球的损伤,测定尿TRF和mAlb对早期诊断糖尿病肾病有良好的诊断价值。
尿IgG
反映肾小球分子筛屏障受损情况,主要用于肾功能恶化程度和预后评价。尿IgG排泄量>250mg/d,可作为肾功能恶化的指标。糖尿病患者代谢紊乱时,会导致弥漫性及渗出性肾脏病变,尿液中可出现大量IgG。
选择性蛋白尿指数(SPI)
同时测定血、尿IgG和TRF,计算SPI,可以反映肾小球通透性异常的严重性和可逆性。
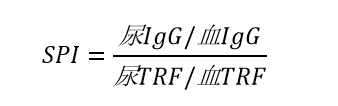
SPI界于0.1-0.2之间时为中选择性,是正常的临床表现。
SPI<0.1时为高选择性,即主要是分子量较小的蛋白质通过了肾小球滤膜,如肾病综合征。尿中以mALB为主,称为选择性蛋白尿,提示肾小球轻微病变。
SPI>0.2时为低选择性,提示肾小球病变严重,是非选择性蛋白尿,预后较差。
尿α2巨球蛋白
分子量达770kD,不能通过肾小球滤过膜,是肾小球滤过膜严重受损的指标。
四、总结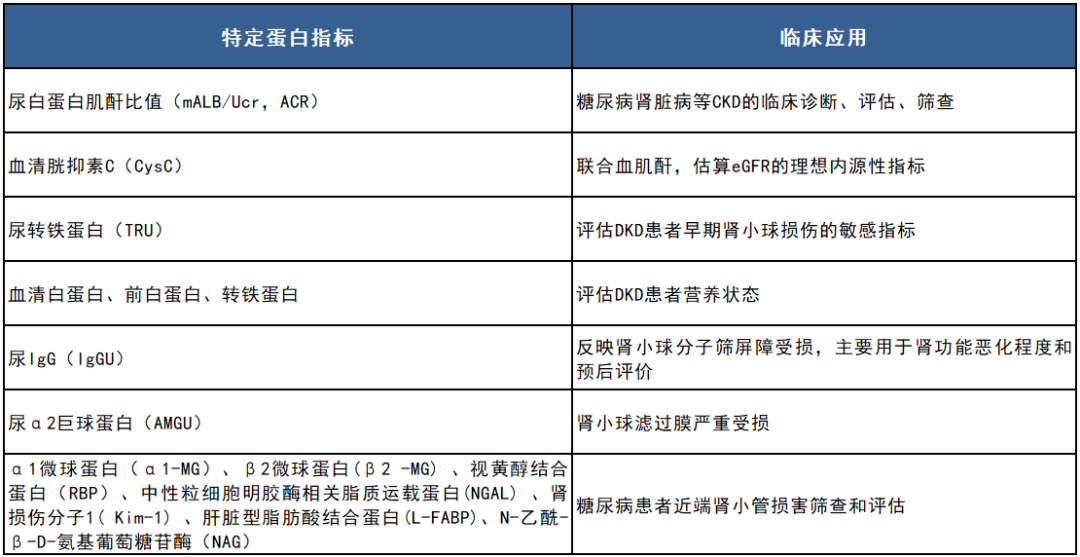
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






