01免疫单药
KEYNOTE-042研究旨在判断对于PD-L1≥1%的非小细胞肺癌(NSCLC)患者应用帕博利珠单抗(K药)单药相较于含铂双药化疗能否改善患者总生存期(OS)。基于此项研究结果,2019年4月11日,FDA批准了帕博利珠单抗单药治疗PD-L1≥1%且无EGFR突变/ALK融合的NSCLC。
整体患者(PDL1≥1%的患者)中,K药治疗组中位OS为16.7个月,标准化疗组OS为12.1个月,有4.6个月的延长,差异具有统计学意义,达到试验的主要终点,证实免疫在PDL1≥1%患者优于化疗的趋势。
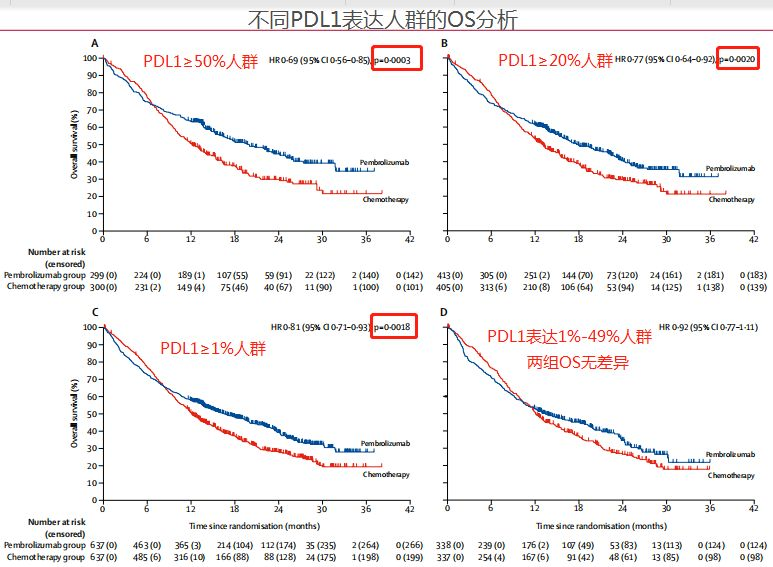
但可惜的是,当我们将1%-49%这部分人群单拎出来时,OS分析显示,免疫K药组和化疗组的中位OS并无统计学差异,分别是13.4个月vs 12.1个月。
02免疫联合化疗
KEYNOTE-407试验纳入559例初治肺鳞癌患者,分为K药+卡铂+紫杉醇,卡铂+紫杉醇两组。试验结果,两组的中位PFS分别为6.4个月 vs 4.8个月,K药组延长了1.6个月。PFS随着PD-L1的表达逐渐提高,在PD-L1表达低组仍优于单纯化疗。总生存时间OS上,K+化疗组达到15.9个月,单纯化疗组为11.3个月,联合治疗组降低36%的死亡风险,延长了OS4.6个月。同时,有效率从38.4%提高了57.9%。
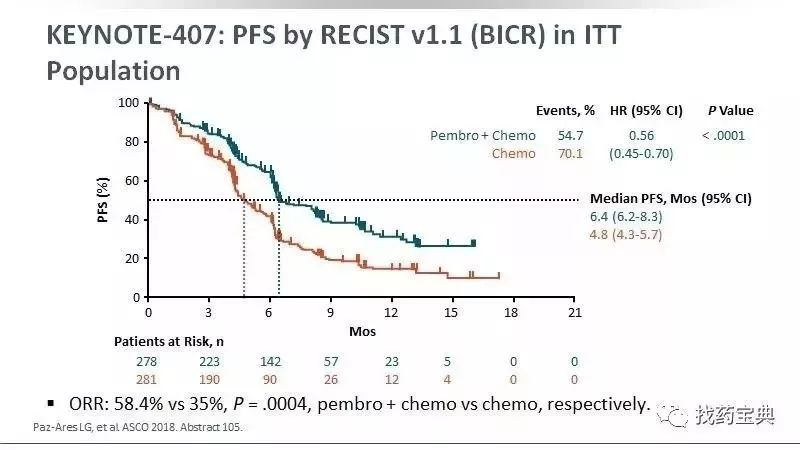
后在额外随访16个月后,进一步更新KEYNOTE-407研究的OS及PFS数据。两组的OS分别为17.1个月和11.6个月(HR=0.71, 95% CI, 0.58‒0.88)。PD-L1≥1%的患者HR为0.67;PD-L1<1%的患者HR为0.79;在PD-L1≥1%的这部分患者,≥50%和1~49%的患者HR值分别为0.79和0.59。 两组的PFS分别为8.0个月和5.1个月(HR=0.57, 95% CI, 0.47‒0.69)。
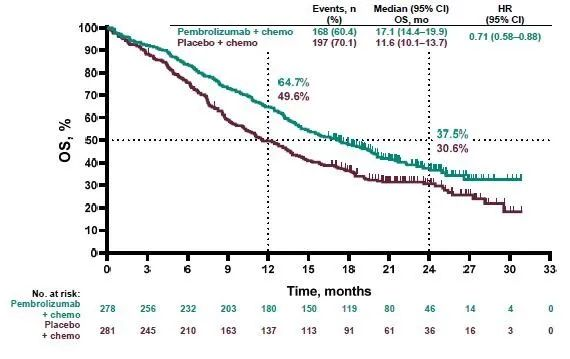
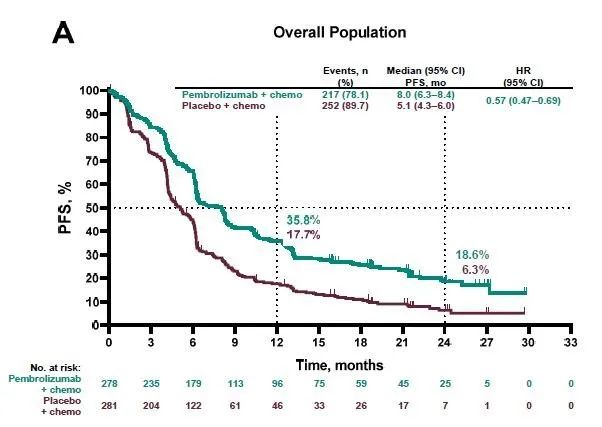
总之,与安慰剂加化疗相比,帕博利珠单抗联合化疗在先前未治疗的转移性鳞状非小细胞肺癌患者中提供了OS和PFS益处,这对PD-L1阴性、低或高表达的患者同样适用。
03Eftilagimod联合PD-1
2023年5月17日Immutep公布了其LAG-3融合蛋白Eftilagimod联合PD-1用于非小细胞肺癌一线治疗的Ⅱ期临床TACTI-002数据,结果显示,Eftilagimod+PD-1在NSCLC患者中取得出色的初步OS,其在PD-L1>1%NSCLC患者中的初步总生存OS为25个月,这已超以往PD-1单药以及联合治疗的OS数据。
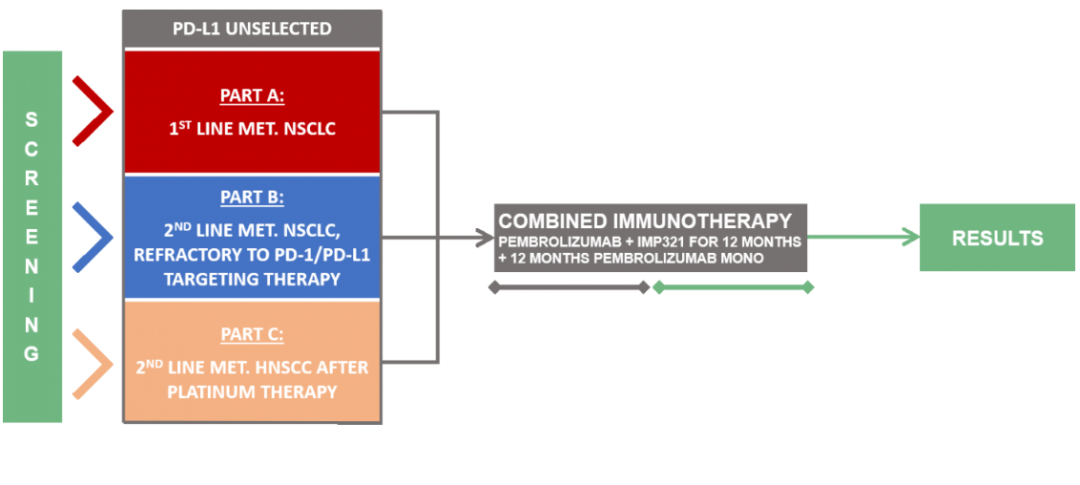
TACTI-002 是一项非随机、开放标签、多国试验,由 3 个部分组成。A部分纳入未接受 PD-L1治疗的一线NSCLC患者 (n = 114) ,B 部分纳入二线NSCLC患者 (n = 36) 且对PD-1/L1具有耐药性,C 部分纳入先前接受过铂类治疗的二线头颈部鳞状细胞癌患者 (n = 39) 。在 2022 年 SITC 年会上提交了 A 部分患者的数据:35.6%的患者PD-L1 TPS<1%,42.2%的患者 TPS 在1%~49% 之间,22.2%的患者TPS≥50%。
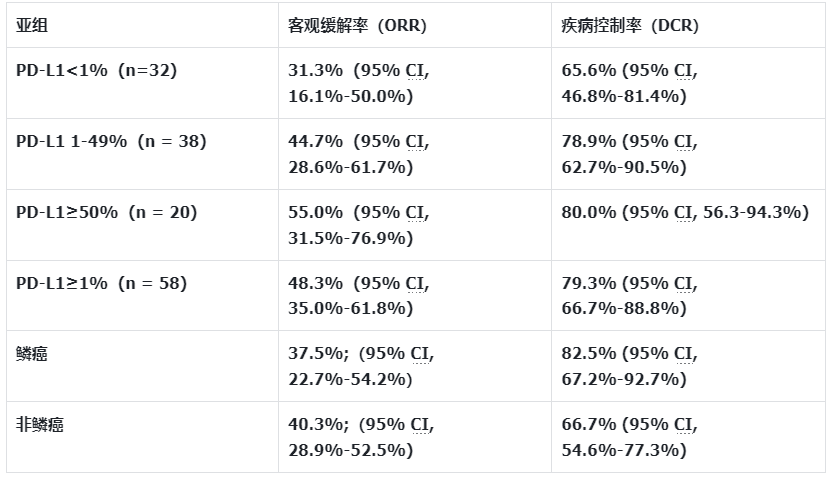
联合用药引起的总缓解率 (ORR) 为 38.6%(95% CI,29.6%-48.2%),其中包括 0.9%的完全缓解率和37.8%的部分缓解率。联合用药的 ORR 在 ITT 人群中为 40.4%(95% CI,31.3%-50.0%)。在 TPS<1% 的患者 (n = 32) 中,该方案的 ORR 为 31.3%(95% CI,16.1%-50.0%),中位 PFS 为 4.2 个月(95% CI,3.6-6.1 )。在 TPS为 1% ~49% 的组中(n = 38),ORR 为 44.7%(95% CI,28.6%-61.7%),中位 PFS 为 8.3 个月(95% CI,4.4-15.7 )。在 PD-L1 TPS ≥50% (n = 20) 的患者中,ORR 最高,为 55%(95% CI,31.5%-76.9%),中位 PFS 为 16.7 个月(95% CI , 4.0-16.8)。在TPS≥1%患者(n = 58)中,ORR 为 48.3%(95% CI,35.0%-61.8%),中位 PFS 为 9.3 个月(95% CI,6.1-15.7)。
在安全性方面,10.5% 的患者经历了严重的毒性反应,2.6% 的患者经历了具有致命后果的事件。12.3% 的患者发生了 3 级或更高级别的不良反应 (AE)。毒性导致 9.6% 的患者停止治疗。
04
阿替利珠单抗+贝伐珠单抗+卡铂+紫杉醇
IMpower150是第一个探索免疫治疗联合抗血管生成治疗和含铂双药化疗用于晚期非鳞非小细胞肺癌一线治疗的疗效和安全性的III期研究,根据IMpower150的研究结果研究,FDA于2018年12月6日批准阿替利珠单抗+贝伐珠单抗+卡铂+紫杉醇作为转移性非鳞状非小细胞肺癌患者的一线治疗方案,已列入NCCN指南。
IMpower150研究结果中,ABCP(阿替利珠单抗-贝伐珠单抗-卡铂-紫杉醇)组的 PFS显著长于BCP(贝伐珠单抗-卡铂-紫杉醇)组,中位PFS分别为8.3 vs 6.8个月(HR=0.62,95%CI:0.52-0.74;P<0.001);且OS 获益持续(中位OS:19.5 vs 14.7 个月;HR=0.80;95%CI:0.67-0.95)。无论患者PD-L1的表达状态如何,ABCP组较BCP组均有不同程度OS的改善。
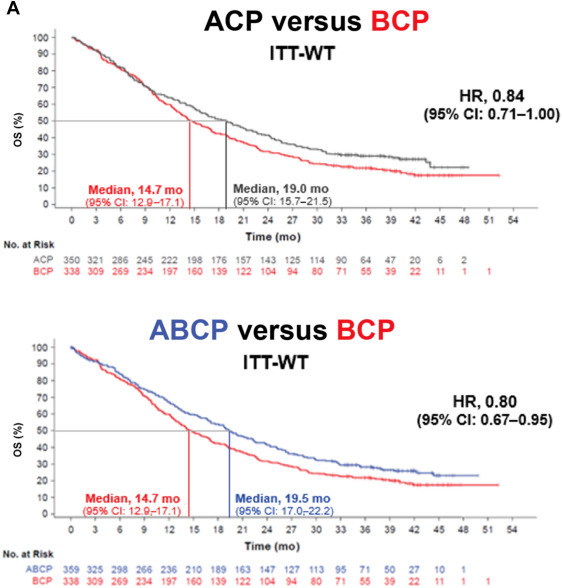
05O+Y双免治疗
2020年5月15日,美国药品监督管理局(FDA)基于CheckMate 227研究1a部分,批准纳武利尤单抗联合伊匹木单抗用于转移性NSCLC成人患者(PD-L1≥1%且无EGFR或ALK基因突变)的治疗,成为全球首个肺癌一线治疗的双免疗法。
CheckMate 227是一项开放性III期临床研究,评估以O药为基础的治疗方案对比含铂双药化疗用于晚期NSCLC患者(包括鳞癌和非鳞癌患者)一线治疗的情况。研究第一部分在评估O+Y与化疗比较时共有两个主要终点:一个是具有PD-L1表达的肿瘤患者的总生存期(OS, 在1a部分评估),另一个主要终点是高肿瘤突变负荷(TMB > 10个突变/Mb,无论PD-L1表达状况如何)患者的无进展生存期(PFS,在1a和1b部分评估)。1b部分:在未表达PD-L1(PD-L1<1%)的患者中评估,与化疗(每3周一次,最多4个疗程)相比,O+Y或者O药联合化疗的疗效。
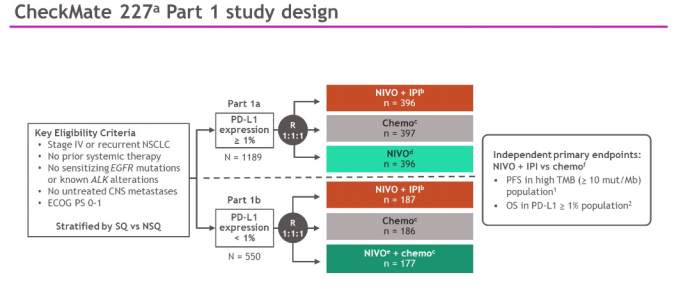
结果显示:在第1部分中,无论患者PD-L1表达状况如何,与化疗相比,O+Y用于高肿瘤突变负荷(TMB≥10个突变/Mb)患者,研究结果达到共同主要终点PFS。此外,相比化疗,O+Y联合治疗用于PD-L1 ≥1%的一线非小细胞肺癌患者,可以带来更高的总生存期(OS)获益。
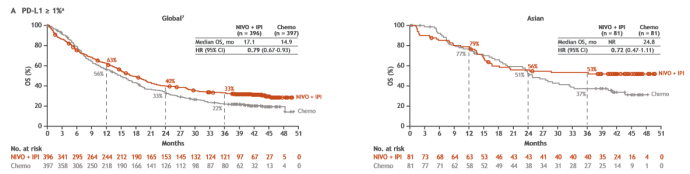
在PD-L1≥1%患者中,全球人群和亚裔人群均能持续从O+Y双免疫治疗中得到OS获益,在亚裔人群数据中,双免疫组1年、2年、3年OS率分别为79%、56%和53%,过半患者接受双免疫治疗生存超过了3年,而化疗组这一比例仅为37%。双免中位OS仍然未达到,化疗组中位OS为24.8个月(HR=0.72,95% CI 0.47-1.11),即与单纯化疗相比,双免降低了亚裔患者28%的死亡风险。相比在全球数据中,双免疫组63%、40%和33%的1年、2年、3年OS率,及17.1 vs 14.9月的OS(HR=0.79,95%CI 0.67-0.93)。可以说,双免疫治疗在亚裔患者中的数据毫不逊色。
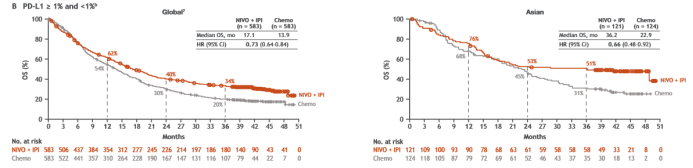
在ITT人群中(PD-L1≥1%和PD-L1<1%),获益仍显著,亚裔双免疫组1年、2年、3年OS率分别为76%、53%和51%,双免对比化疗中位OS为36.2个月vs 22.9个月(HR=0.66,95%CI 0.48-0.92),与单纯化疗相比,双免降低了亚裔患者34%的死亡风险。而全球双免疫组1年、2年、3年OS率分别为62%、40%和34%,双免对比化疗中位OS为17.1个月vs 13.9个月(HR=0.73,95%CI 0.64-0.84)。证实了亚裔患者与全球的整体人群获益旗鼓相当。
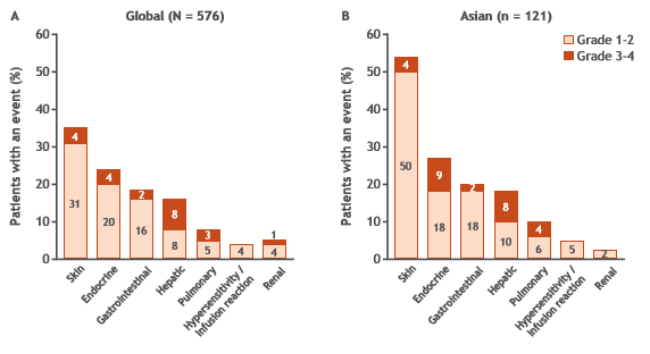
CheckMate-227研究中的安全系数要明显优于化免联合,并优于化疗本身。此次亚裔患者安全性分析再次证实,亚裔患者与全球安全性数据基本一致,尚未发现新的安全信号。
06
O+Y+2周期化疗
Checkmate-227研究奠定了双免治疗在晚期非小细胞肺癌泛癌种一线的应用地位,但研究专家们未曾停止探索,仍继续优化治疗方案。在O+Y双免方案上追加2个周期化疗,来寻求疾病早期的快速控制,争取更大的生存获益。Checkmate-9LA研究就此应运而生。根据CheckMate 9LA的阳性结果,2020年FDA批准纳武利尤单抗与伊匹木单抗+ 2周期化疗用于无EGFR/ALK改变的转移性或复发性NSCLC成人一线治疗,无论PD-L1表达水平如何。
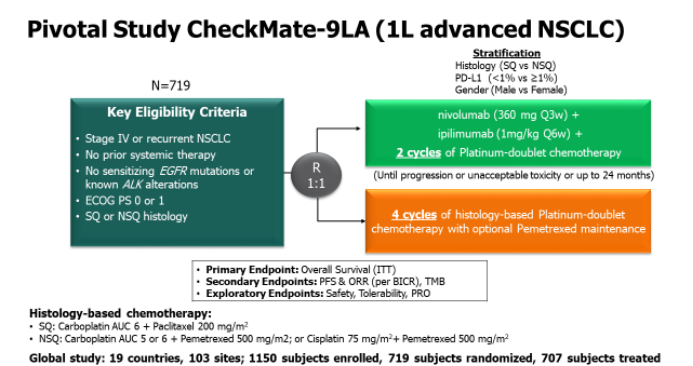
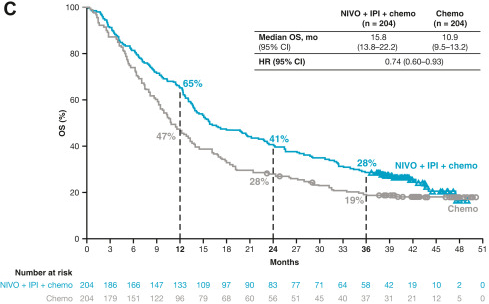
719 名 (62.5%)患者被随机分配至纳武利尤单抗加伊匹木单抗加2周期化疗 (n=361 [50%]) 或单独化疗四个周期(n=358 [50%])。在预先计划的中期分析中(中位随访时间 9.7个月),实验组的总生存期明显长于对照组(中位OS分别为 14.1个月 [95% CI 13.2–16.2] vs 10.7个月[95%CI 9.5–12.4];HR :0.69)。中位随访时间延长3.5个月(中位随访时间 13.2个月),数据更新显示,实验组与对照组的中位OS为15.6个月vs 10.9个月。
亚组分析显示,无论患者PD-L1表达水平和肿瘤组织学类型(鳞癌或非鳞癌)如何,疗效评估均显示出临床获益。PD-L1<1%的患者,两组中位OS分别为16.8个月和9.8个月,HR=0.62;PD-L1≥1%的患者,两组的中位OS分别为15.8个月和10.9个月,HR=0.64;非鳞癌患者,两组中位OS分别为17.0个月和11.9个月,HR=0.69;鳞癌患者两组中位OS分别为14.5个月和9.1个月,HR=0.62。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言