SCIENCE ADVANCES:可卡因总是戒不掉?突触pH稳态调节酶CA4治疗可卡因戒断引起的复吸
2022-12-05 周科 “ 神经周K”公众号 发表于上海
物质使用障碍是在反复接触成瘾药物和药物戒断过程中,引起相关神经环路发生适应性改变,驱动强烈的觅药动机和复吸行为。伏隔核(NAc)是奖赏系统相关环路的关键枢纽,在药物引起的适应性改变中发挥重要作用。在可
物质使用障碍是在反复接触成瘾药物和药物戒断过程中,引起相关神经环路发生适应性改变,驱动强烈的觅药动机和复吸行为。伏隔核(NAc)是奖赏系统相关环路的关键枢纽,在药物引起的适应性改变中发挥重要作用。在可卡因戒断过程中,NAc脑区的中型多棘神经元(MSNs)的突触结构发生明显变化,树突棘密度增加,钙透性的AMPA受体(CP-AMPAR)功能增加,这一变化会增加可卡因复吸行为。
酸敏感性离子通道1A(ASIC1A)是细胞外氢离子激活的阳离子通道,被发现是突触生理过程的调节剂,突触间隙的氢离子激活ASIC1A亚基,可影响兴奋性突触后电流(EPSC)的强度。敲除ASIC1A可通过增加神经元树突棘密度、增强EPSC而易化可卡因的行为敏化。碳酸酐酶4(CA4)是关键的pH调节缓冲酶,通过糖基磷脂酰肌醇锚定在细胞膜上,调节突触部位的pH。但是CA4是否调节可卡因的戒断反应,目前并不清楚。
2022年11月16日爱荷华大学精神病学系的John A. Wemmie研究团队发现CA4可通过影响ASIC通道改变MSN的活性,调节可卡因戒断后的神经适应性。敲除CA4通过增加ASIC1A介导的EPSC,预防可卡因戒断引起的觅药行为。

1
敲除MSN神经元的CA4增加ASIC通道介导的EPSC
对NAc的组织、细胞膜和突触体蛋白裂解液进行Western blot检测,发现CA4在以上三类样本中均有表达,说明CA4表达在神经元的突触结构。随后使用组织膜片钳技术对NAc脑区MSN的兴奋性突触后电流(EPSC)进行记录,当阻断谷氨酸受体和GABA受体后的EPSC为ASIC通道介导的EPSC,发现敲除MSN神经元上的CA4,会导致ASIC通道介导的EPSC显着增加。
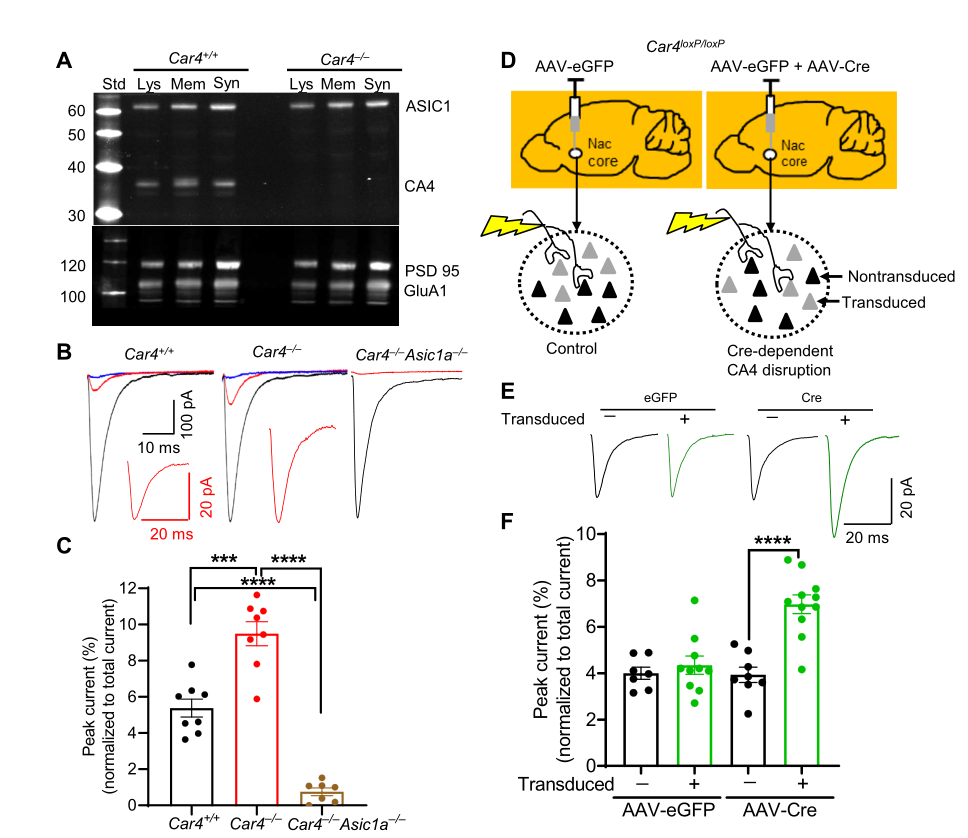
图1: 敲除MSN神经元的CA4增加ASIC通道介导的EPSC
2
敲除MSN神经元CA4降低可卡因戒断引起突触可塑性改变
AMPAR/NMDAR的比值是可卡因诱导神经元可塑性的标志指标之一,可驱动小鼠的复吸行为。可卡因成瘾小鼠在戒断过程中,MSN的AMPAR/NMDAR的比值显著增加。敲除MSN神经元上的CA4后,可卡因戒断过程中不会引起AMPAR/NMDAR的比值的增加,说明敲除CA4可降低可卡因戒断引起的复吸行为。
对其他神经元可塑性的电生理指标进行记录,发现可卡因戒断过程中,MSN钙渗透性的AMPA受体介导的EPSC明显增强,神经元微小兴奋性突触后电流的频率和幅度均显着增加,并且神经元树突棘密度明显上调。敲除CA4可阻断可卡因戒断引起的上述变化。
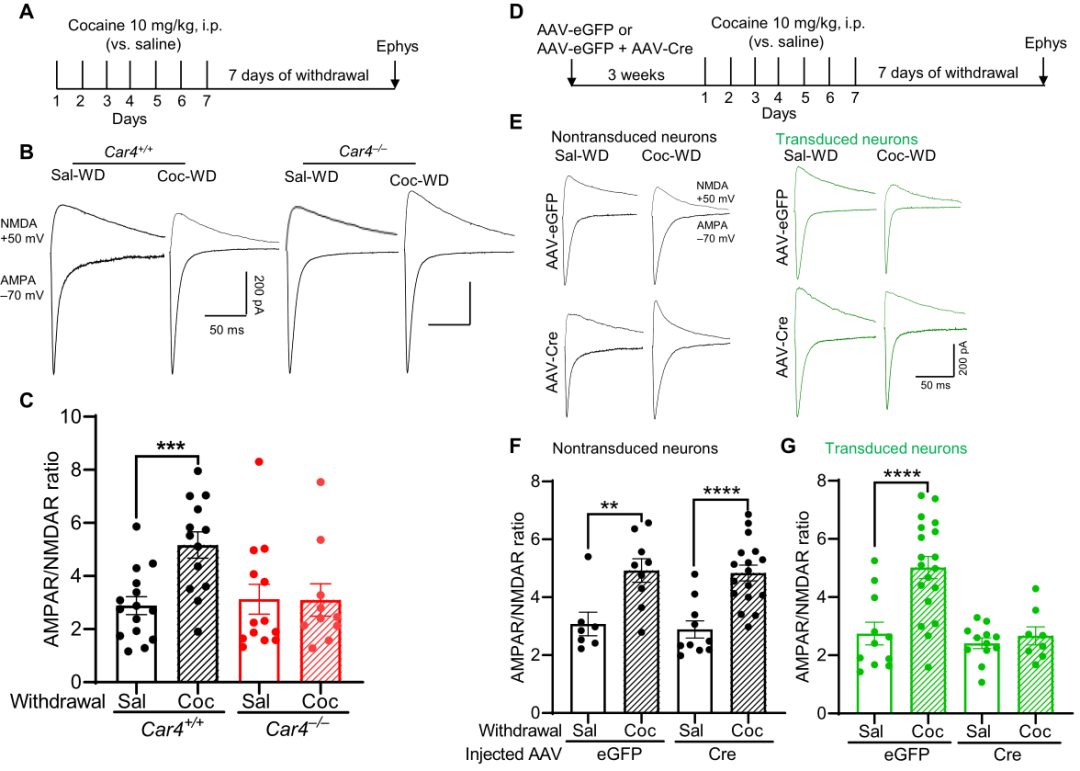
图2:敲除CA4阻断可卡因戒断引起AMPAR/NMDAR比值的增加
3
敲除MSN神经元的CA4降低可卡因戒断引起的药物复吸
构建小鼠自身给药成瘾模型,发现在小鼠成瘾过程中对照小鼠和CA4敲除小鼠均表现出相同的压杆行为,说明在可卡因成瘾过程中,两类小鼠对可卡因均有强烈的渴求。但是在可卡因戒断之后,对照小鼠对可卡因仍有强烈的渴求,而CA4敲除小鼠对获得可卡因的动机明显减弱。
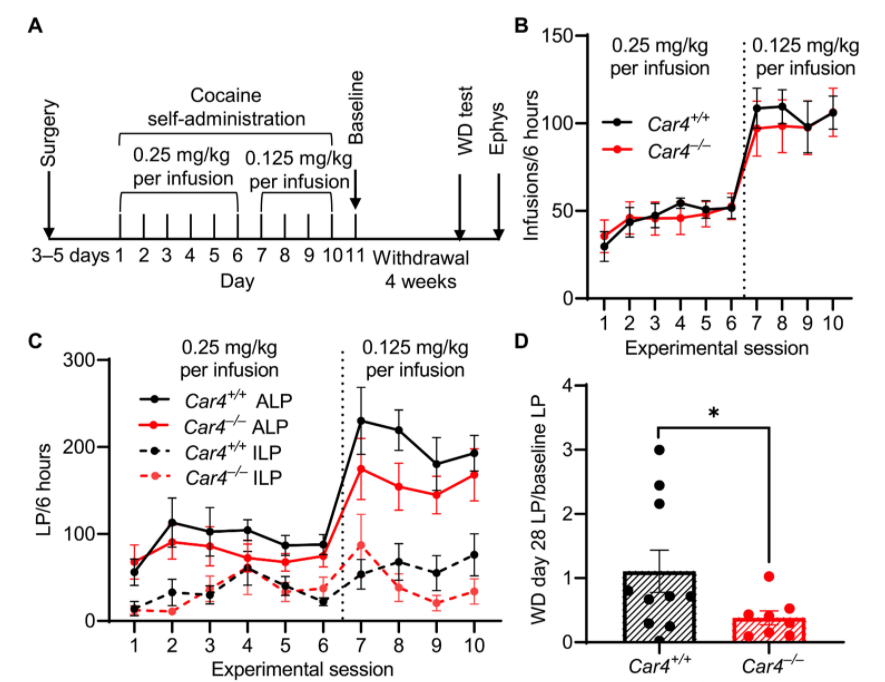
图3:敲除CA4降低可卡因戒断引起的药物复吸
总结
本文发现敲除CA4会破坏突触间隙pH的稳态,增加细胞间隙的氢离子,激活ASIC1A通道介导的兴奋性突触电流,降低MSN神经元AMPAR/NMDAR的比值,抑制突触可塑性功能的增强,进而改善可卡因戒断引起的药物复吸,提示抑制CA4或可成为治疗可卡因复吸的关键。
原始出处:
SUBHASH C. GUPTA, et al. Carbonic anhydrase 4 disruption decreases synaptic and behavioral adaptations induced by cocaine withdrawal. SCIENCE ADVANCES, 16 Nov 2022, Vol 8, Issue 46.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言