Bioact Mater:壳聚糖@葛根素水凝胶促进糖尿病患者的伤口愈合
2022-08-07 August MedSci原创
不愈合的慢性皮肤伤口的常见病因是糖尿病和相关的合并症。伤口修复是一个复杂但高度程序化的过程,包括涉及止血、炎症反应、细胞增殖和组织重塑的阶段。然而,该过程在慢性皮肤伤口的炎症阶段停止。
伤口愈合是糖尿病患者的主要全球健康问题之一。促炎 M1 巨噬细胞的过度活化与糖尿病伤口愈合延迟有关。miR-29ab1 在糖尿病相关巨噬细胞炎症中起关键作用。因此,抑制炎症和调节 miR-29 表达被认为是皮肤伤口愈合的新点。在这项研究中,引入中药葛根素构建了一种可注射的自愈壳聚糖@葛根素(C@P)水凝胶。C@P 水凝胶促进糖尿病伤口愈合和加速血管生成,这与抑制 miR-29 介导的炎症反应有关。与健康受试者相比,糖尿病模型的皮肤伤口中 miR-29a 和 miR-29b1 异位升高,伴随着上调的 M1 极化,以及升高的 IL-1β 和 TNF-α 水平。miR-29ab1 敲除小鼠的进一步评估显示出优异的伤口愈合和减轻炎症。目前的结果表明,miR-29ab1 通过调节炎症反应对糖尿病伤口愈合至关重要。C@P 水凝胶对 miR-29ab1 的抑制有可能改善伤口修复的医学方法。
C@P水凝胶的合成和表征:
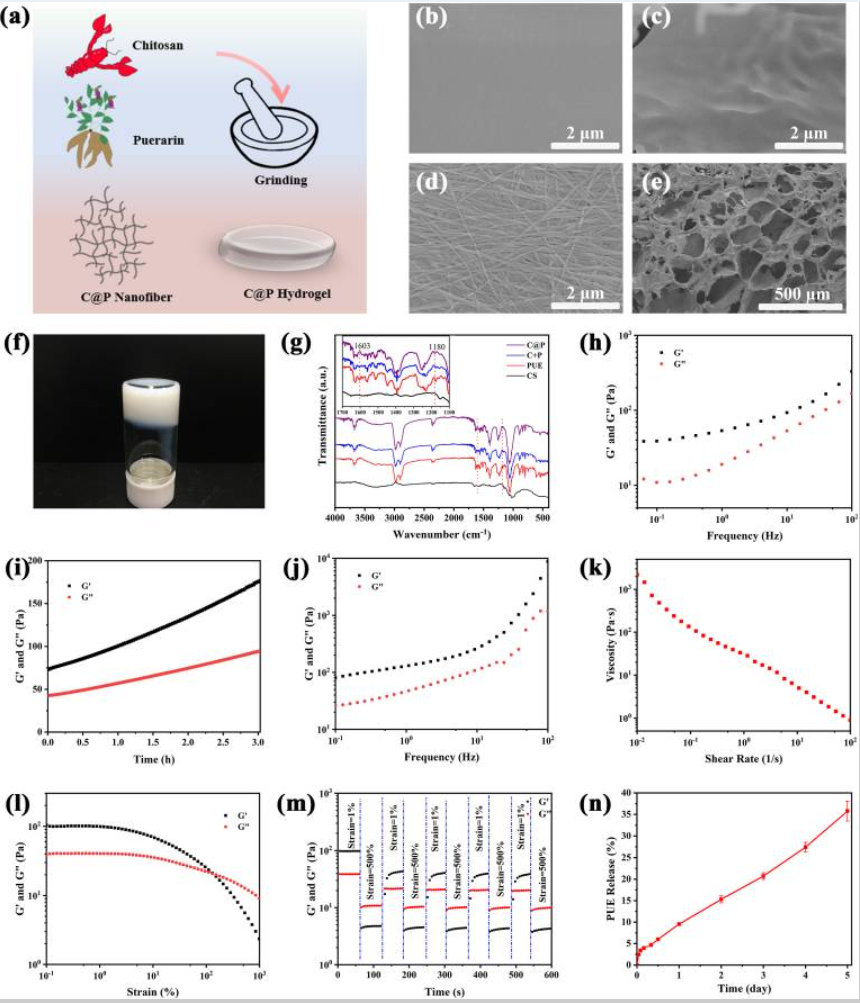
C@P 水凝胶促进 DM 慢性伤口的伤口愈合:
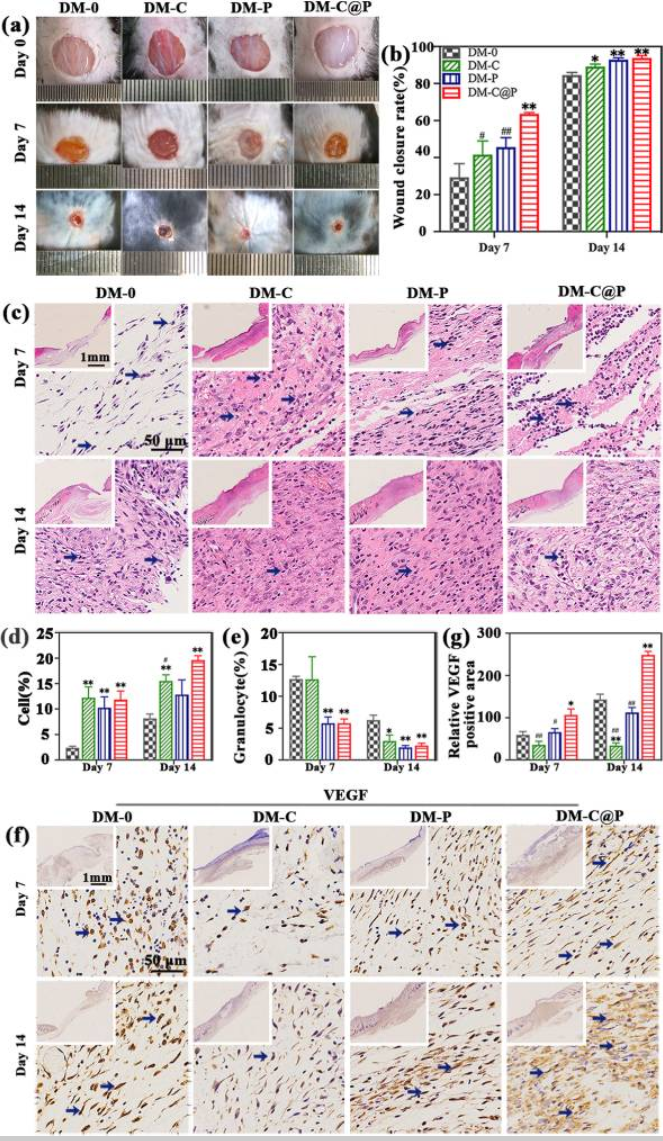
C@P 水凝胶抑制 M1 巨噬细胞的表达:
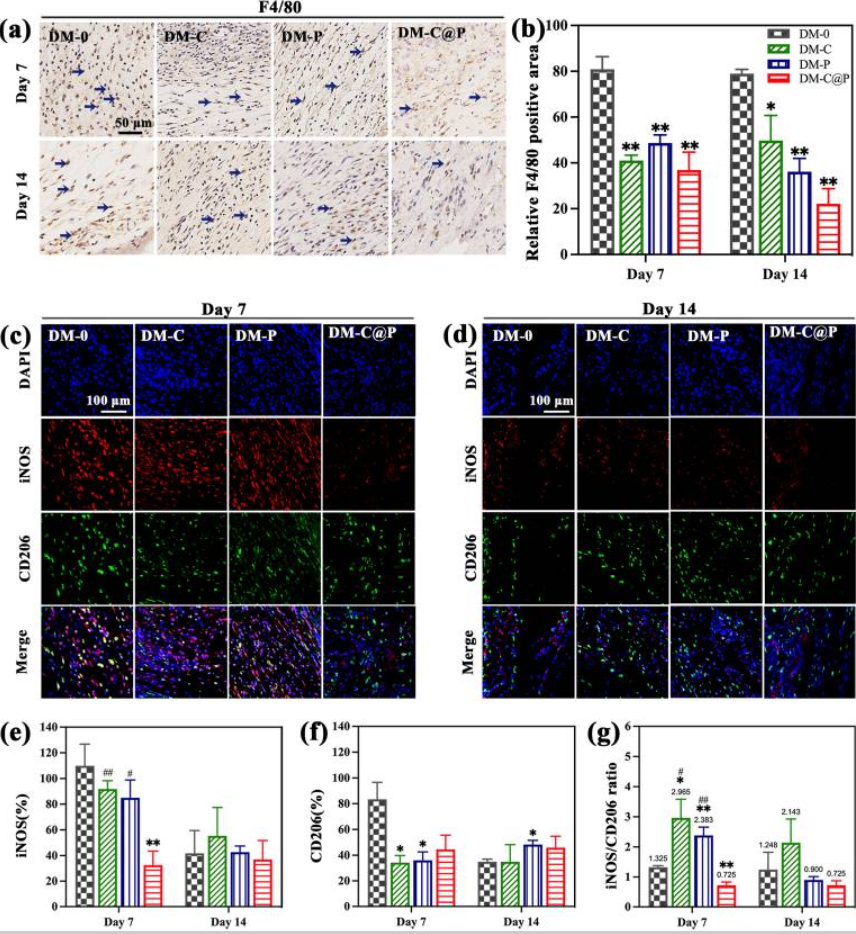
C@P 抑制 miR-29a/b1 表达,这在糖尿病伤口愈合中异位增加:
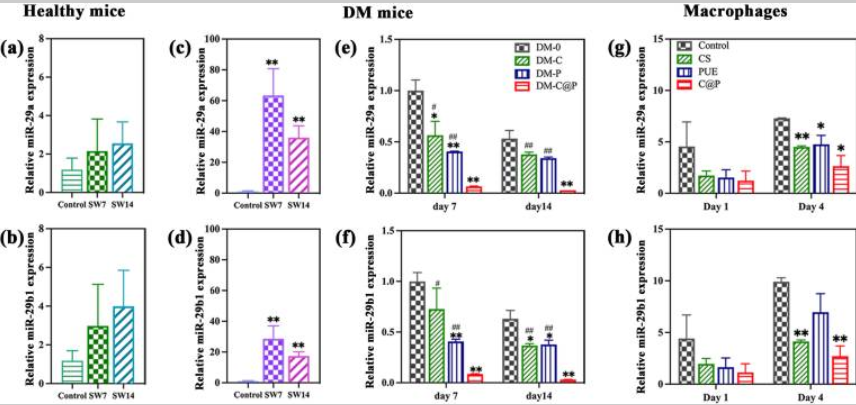
miR-29ab1 -/-小鼠通过抑制炎症来抑制炎症反应:

综上所述,由于持续的炎症,糖尿病皮肤伤口在临床上难以愈合。在这项研究中,发现异位高 miR-29ab1 与糖尿病伤口愈合不良密切相关,这被认为有助于糖尿病小鼠中 M1 巨噬细胞极化延长和 TNF-α 和 IL-1β 水平升高。结果通过在 miR-29ab1 缺失小鼠中观察到的逆转趋势得到验证。合成了壳聚糖@葛根素水凝胶,结果表明它通过抑制异位 miR-29ab1 介导的巨噬细胞和调节炎症来促进糖尿病伤口愈合。这种机制可以在用于糖尿病伤口愈合的材料设计中提供广泛的应用。
原文:Zeng X, Chen B, Wang L, Sun Y, Jin Z, Liu X, Ouyang L, Liao Y. Chitosan@Puerarin hydrogel for accelerated wound healing in diabetic subjects by miR-29ab1 mediated inflammatory axis suppression. Bioact Mater. 2022 May 11;19:653-665. doi: 10.1016/j.bioactmat.2022.04.032. PMID: 35600974; PMCID: PMC9109129.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#葛根素#
55
#Bio#
58
新发现,学习了
45
,。看看
48
#水凝胶#
53
#伤口愈合#
45
#凝胶#
38
#糖尿病患者#
44
#壳聚糖#
47