Nat Commun:IL6反式信号转导通路:弥漫性癌细胞转移的潜在机制
2020-10-16 xiaozeng MedSci原创
在乳腺癌中,肿瘤细胞转移到远端的时间要比转移的临床表现早6到8年。尽管在进行初次手术前,成千上万的乳腺癌细胞会扩散并归巢于骨髓,但通常只有不到一小部分会在数月至数年后成功的建立明显的转移灶。
在乳腺癌中,肿瘤细胞转移到远端的时间要比转移的临床表现早6到8年。尽管在进行初次手术前,成千上万的乳腺癌细胞会扩散并归巢于骨髓,但通常只有不到一小部分会在数月至数年后成功的建立明显的转移灶。
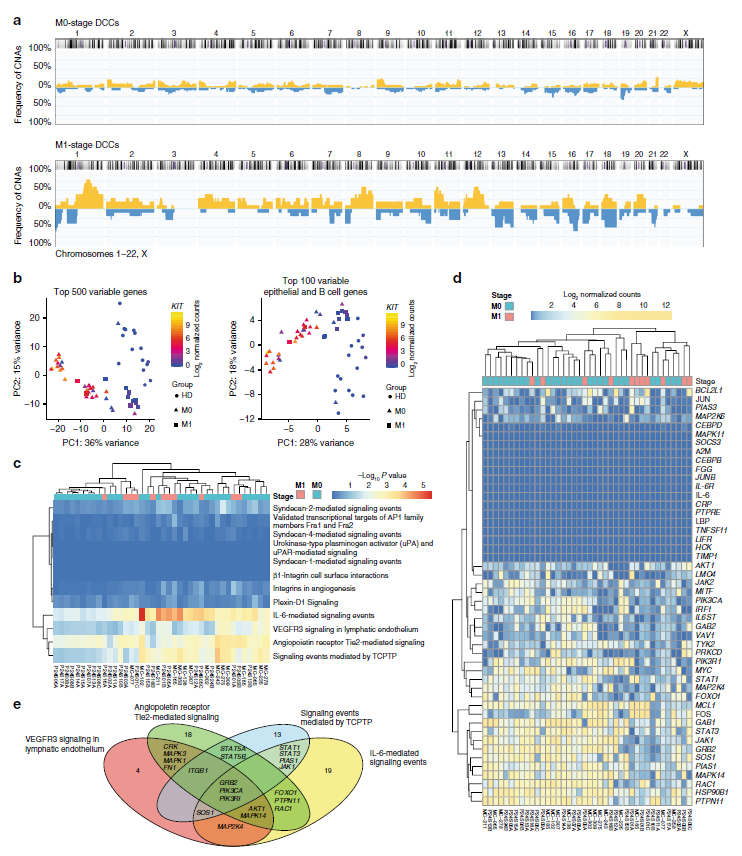
为了确定支持患者生存或肿瘤增长的相关信号,研究人员在转移灶出现前的较长时间点就针对罕见的骨髓源性的弥漫性癌细胞(DCC)进行分析,并鉴定出IL6/PI3K信号通路位为DCC激活的候选通路。令人惊讶的是,类似于乳腺上皮细胞,DCC细胞缺乏细胞膜IL6受体的表达。且机制研究显示,IL6反式信号转导通路能够通过gp130调节乳腺上皮细胞的干性状态。
IL6信号通路在乳腺干细胞中被激活
研究人员发现,IL6反式信号转导通路的响应是干细胞微环境(niche)依赖性的,与血管微环境细胞相反的,在恶化前乳腺上皮细胞中的骨髓干和骨内膜细胞中gp130的表达下调。PIK3CA激活的细胞独立于IL6反式信号转导通路。研究人员发现,与微环境DCC细胞的瓶颈功能一致的是,PIK3CA突变与晚期转移细胞高度相关,而在早期DCC中极为罕见。
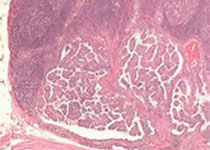
乳腺癌患者BM-DCCs中IL6信号通路被激活
综上,该研究结果揭示,肿瘤转移的初始形成通常不是癌细胞自主的,而是取决于微环境相关信号。
原始出处:
Werner-Klein, M., Grujovic, A., Irlbeck, C. et al. Interleukin-6 trans-signaling is a candidate mechanism to drive progression of human DCCs during clinical latency. Nat Commun 11, 4977 (05 October 2020).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#COMMUN#
35
#Nat#
41
#IL6#
49
#癌细胞#
39
#弥漫性#
54
#细胞转移#
0
#癌细胞转移#
47
谢谢分享
85
机制研究离临床仍然有距离,不过与临床结合思考,仍然有帮助的,不能仅仅是纯临床思维,转化思维同样重要
57