非小细胞肺癌 靶向治疗 EGFR突变 1. 一项研究(新辅助):II期,奥希替尼,MPR率仅15%(未达预设终点),pCR率为0% 2. ADAURA研究(辅助):III期,奥希替尼±化疗 vs 化疗,5年OS率分别是85% vs 73%,获统计学意义延长 3. AGAIN研究(晚期):III期,吉非替尼/奥希替尼+化疗 vs 吉非替尼/奥希替尼,中位OS无差异 4. SYMPHONY研究(C797X耐药):I期,BLU-945 ± 奥希替尼,疗效有待提高,2期推荐剂量(RP2D)仍未确定 5. CHRYSALIS-2研究:I/Ib期,奥希替尼耐药,Amivantamab+Lazertinib,MET(3+)ORR达61% EGFR 20ins 6. WU-KONG1、15研究:I/II,舒沃替尼,初治ORR达77.8% 免疫治疗 围术期免疫治疗 7. KEYNOTE-671研究:III期,K药+化疗→手术→K药维持 vs 化疗→手术,EFS获益;确立治疗新模式 8. Neotorch研究:III期,特瑞普利单抗围术期免疫治疗,EFS获益 晚期免疫治疗 9. TROPION-Lung02研究:Ib期,Dato-DXd+K药±铂类,双联、三联ORR分别为38% vs 49% EGFR-TKI耐药 10. KEYNOTE-789研究:III期,K药+化疗 vs 化疗,PFS、OS均无差异
非小细胞肺癌-靶向治疗部分
新辅助靶向治疗
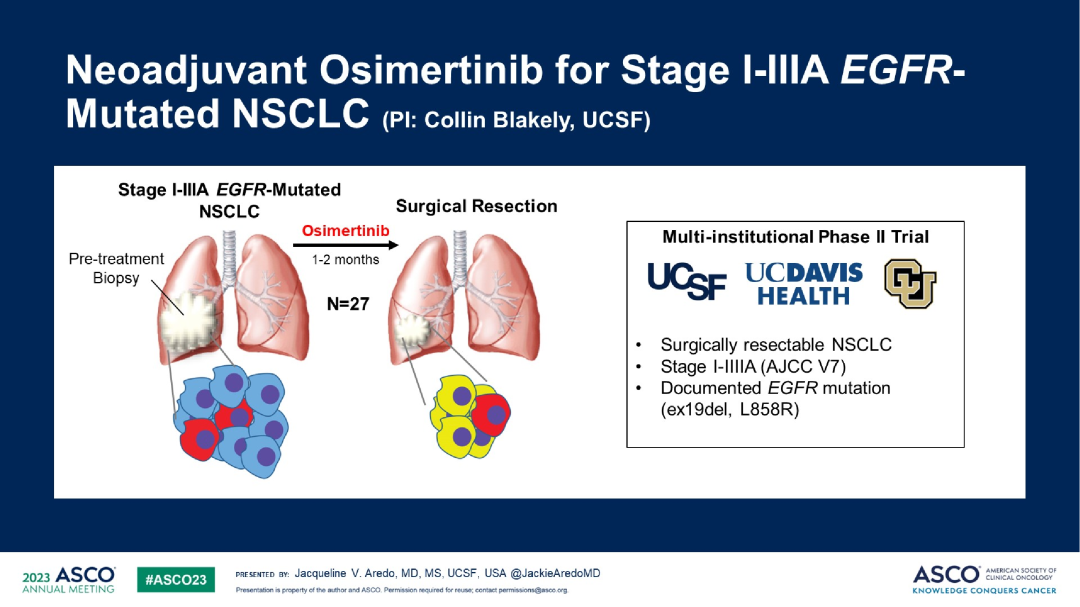
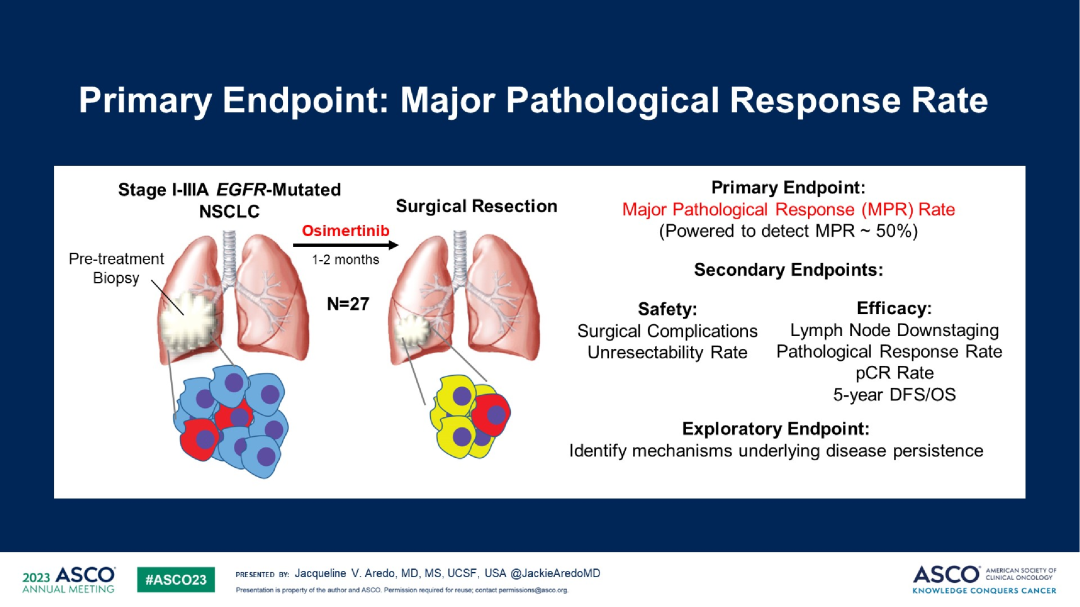

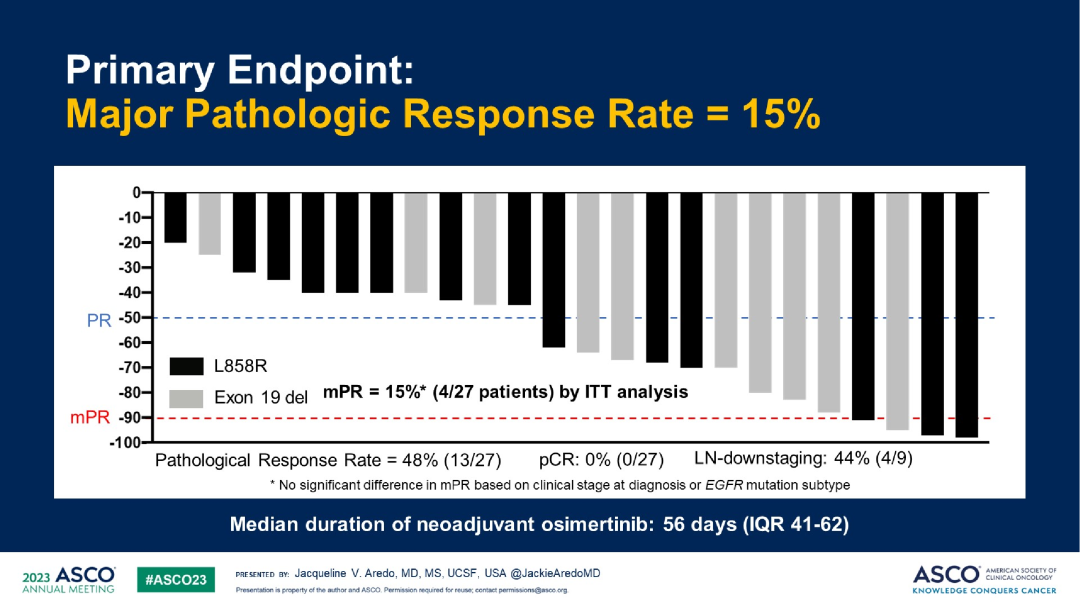
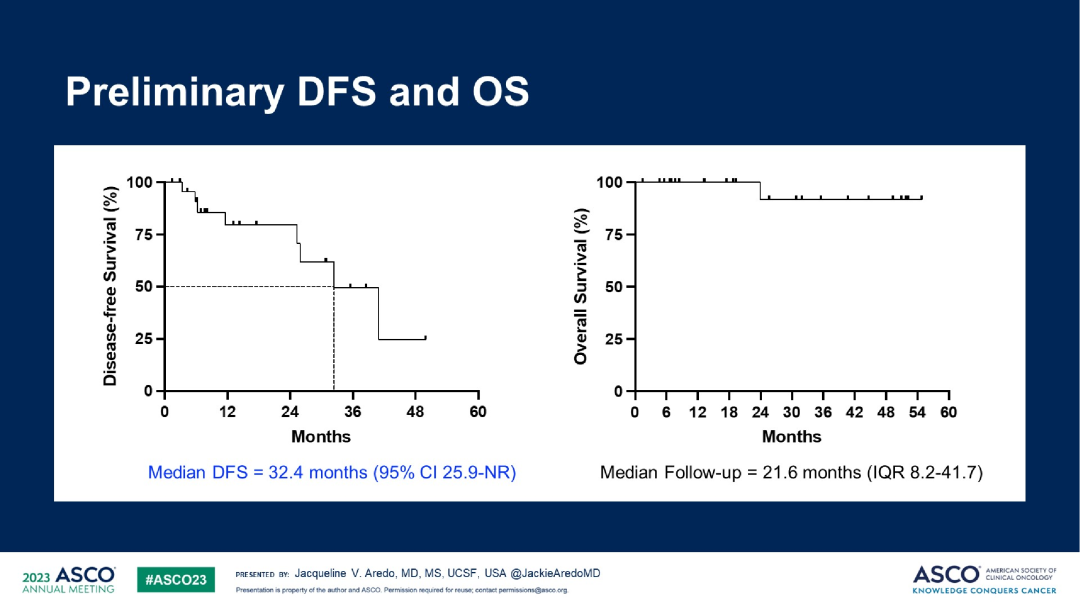
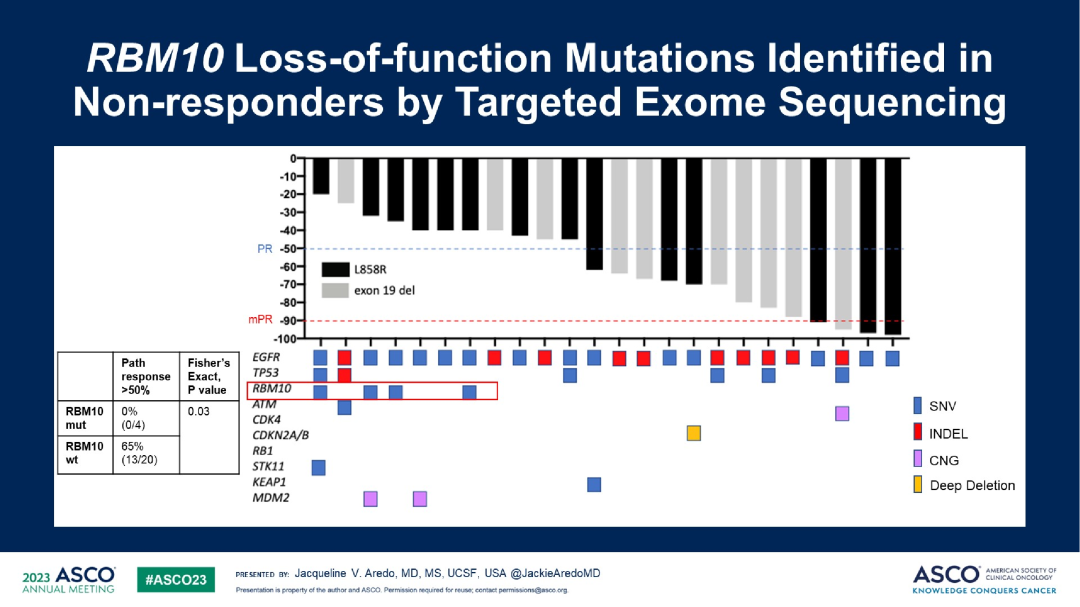
探索性分析发现,残留病灶中存在RBM10功能缺失突变与治疗无应答相关;另外,残留病灶中YAP的基因表达增加,可能与肿瘤细胞存活相关。
辅助靶向治疗

研究结果:1)DFS,在本次OS分析结果发布前,最后更新(截至2022年4月,中位随访时间44.2个月)的DFS数据显示[2],II-IIIa期患者两组中位DFS分别为65.8个月和21.9个月,HR=0.23,48个月的DFS率分别为70%和29%;Ib-IIIa期患者中,两组中位DFS分别为65.8个月和28.1个月,HR=0.27。
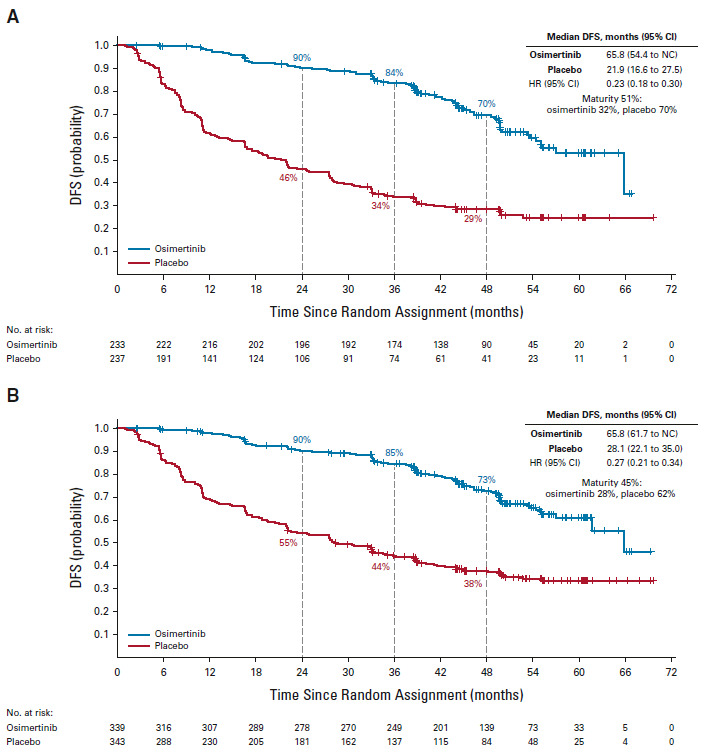
II-IIIa的DFS
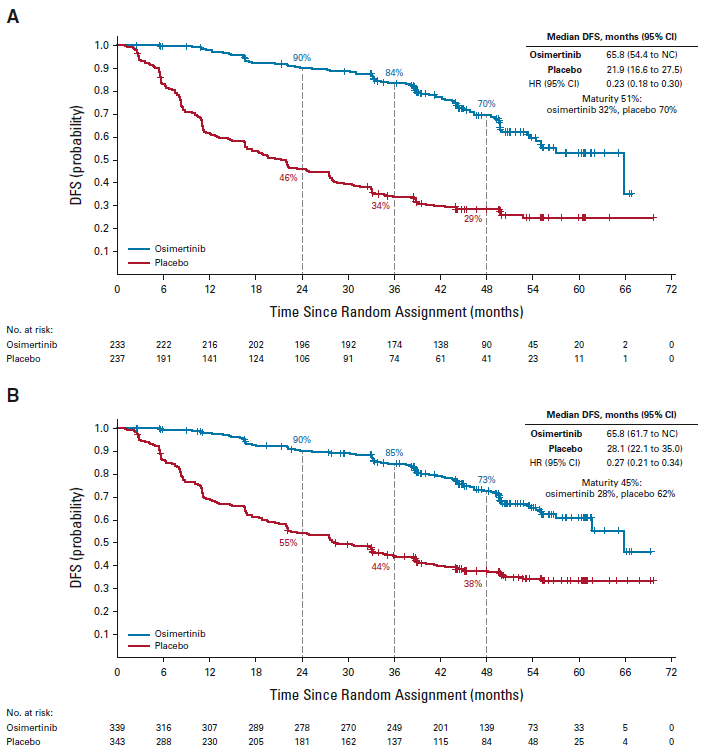
Ib-IIIa的DFS
2)OS,奥希替尼组和安慰剂组分别有339例和343例患者纳入本次最终OS分析,两组分别发生42和82例OS事件,数据成熟度为12.4%和23.9%,已符合研究预设的最终OS分析标准(Ⅱ-ⅢA期患者中发生100例OS事件,预设为约94例)。奥希替尼组和安慰剂组患者的中位OS均尚未达到,在Ⅱ至ⅢA期疾病患者中,奥希替尼组和安慰剂组5年OS率分别是85% vs 73%(HR=0.49,P<0.001);在总体人群(ⅠB至ⅢA期疾病患者)中分别为,88% vs 78%(HR=0.49,P<0.001)。
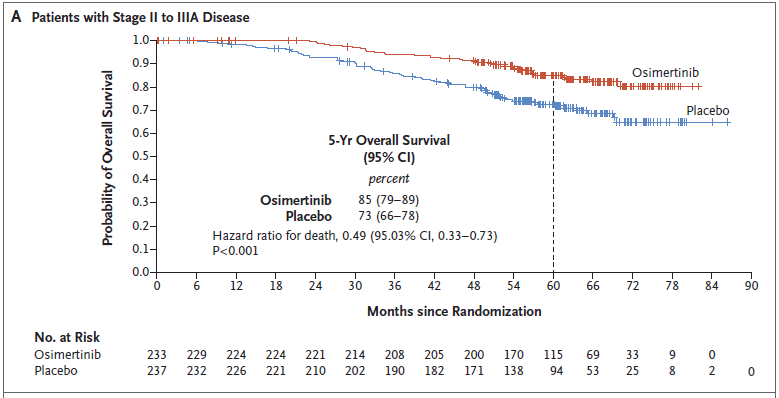
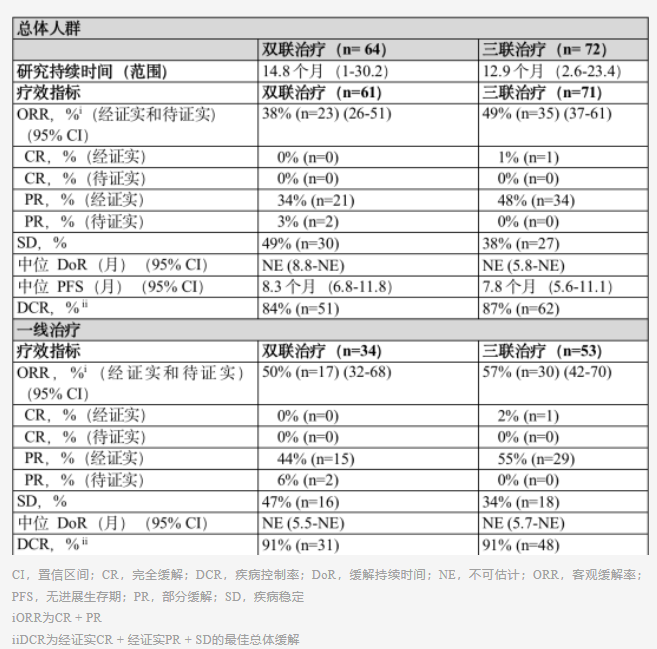
II-IIIA期OS曲线
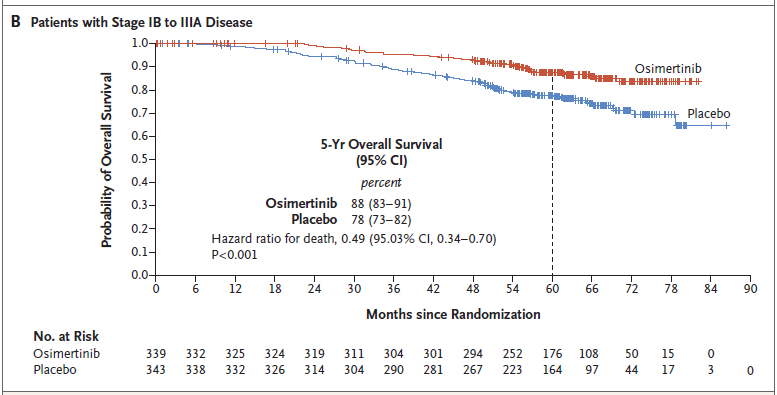
II-IIIA期OS曲线
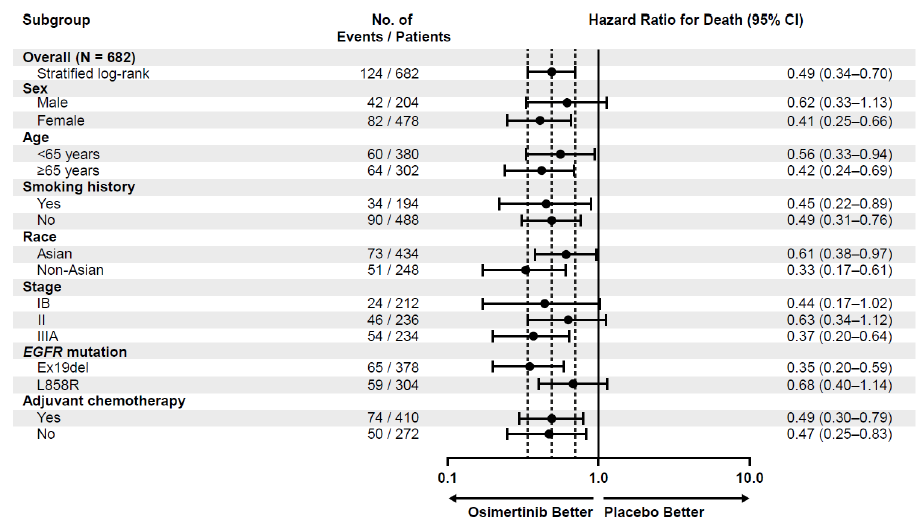
亚组分析结果显示,奥希替尼辅助治疗的获益在各亚组中整体一致,无论患者是否接受过辅助化疗,均不影响奥希替尼治疗的OS获益。
在之前公布的数据截止日期之后报告了一起新的严重不良事件(COVID-19相关肺炎)。研究者认为该事件与试验治疗方案无关,且患者完全康复。奥希替尼辅助治疗安全性与主要分析结果一致。
小结:在完全切除术后的EGFR突型ⅠB至ⅢA期NSCLC患者中,奥希替尼辅助治疗具有显著总生存获益。
晚期靶向治疗
AGAIN(JCOG1404/WJOG8214L)研究:一项开放标签、多中心、III期随机对照研究,对比了吉非替尼联合顺铂+培美曲塞或EGFR-TKI单药一线治疗EGFR突变非鳞非小细胞肺癌的疗效与安全性【研究假设加上化疗可以消除耐药的克隆】。研究纳入局部晚期或晚期EGFR敏感突变的非鳞状NSCLC患者,联合化疗组第1~56天接受吉非替尼或奥希替尼治疗,接着空窗2周,后第71、92和113天给予顺铂和培美曲塞3周期化疗,再第134天重新给予吉非替尼或奥希替尼直至疾病进展;靶向单药组接受吉非替尼或奥希替尼治疗直至疾病进展。主要终点是总生存期(OS)。

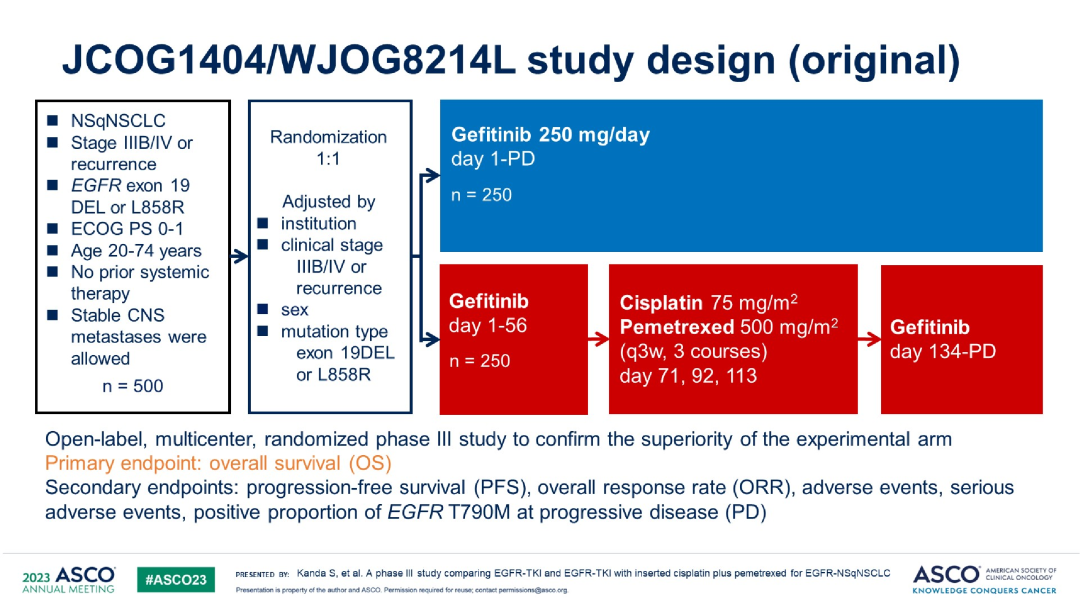

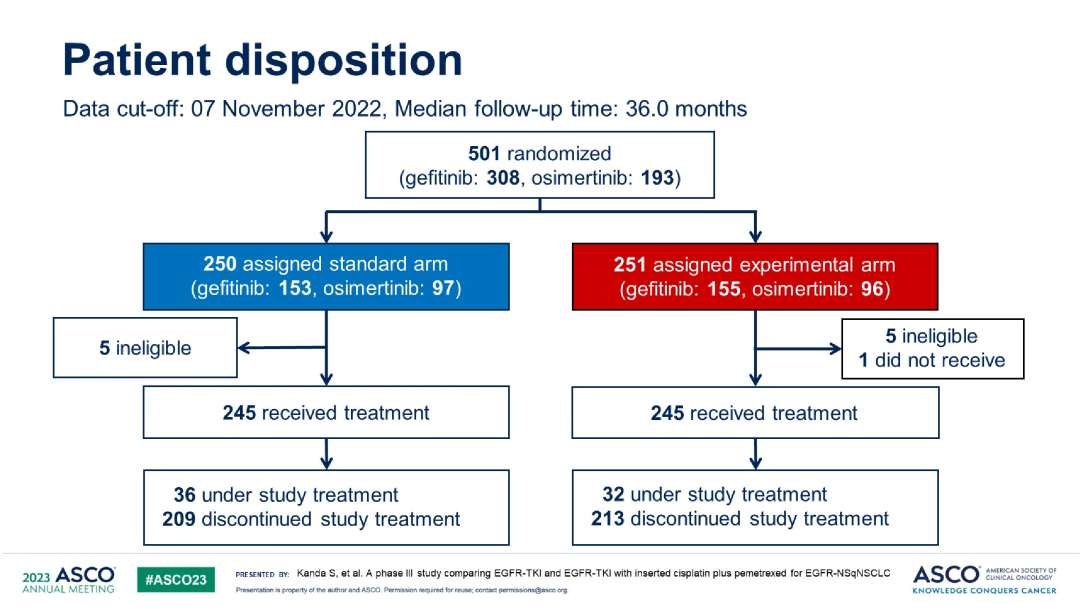
入组情况
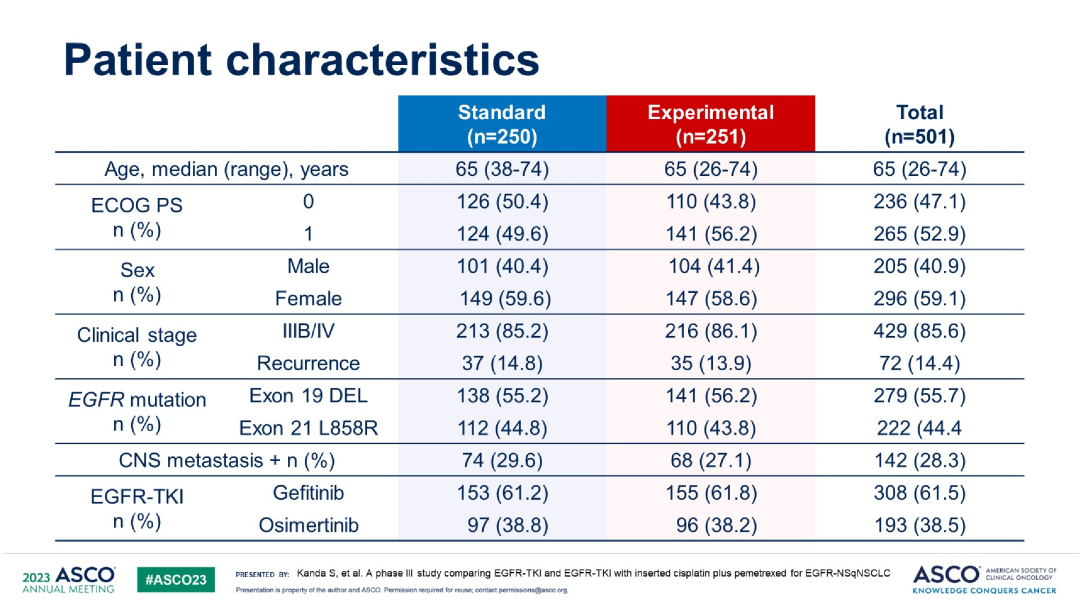
基线特征

PFS
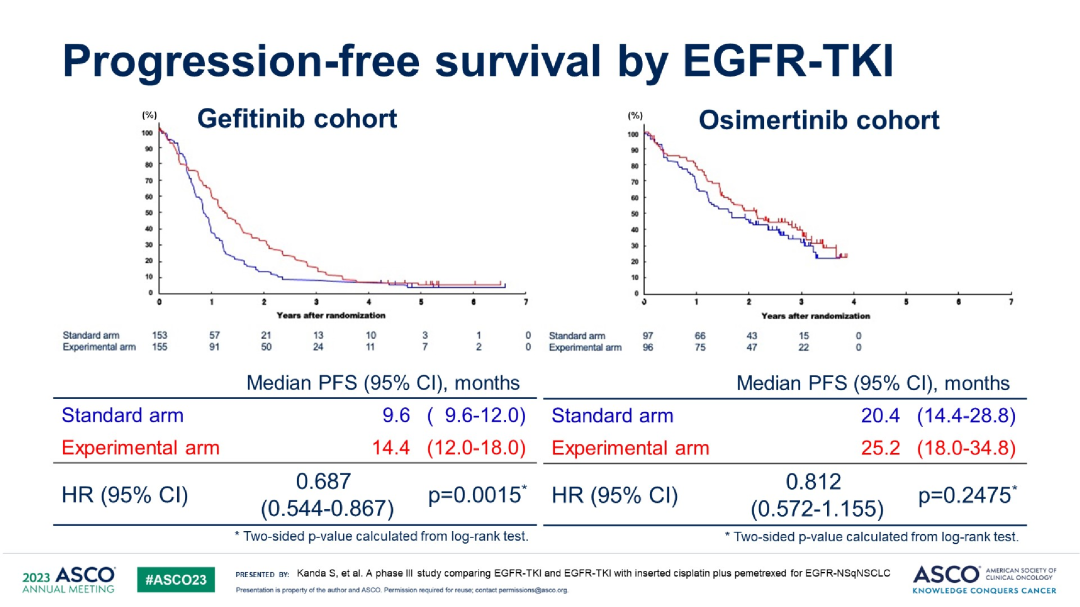
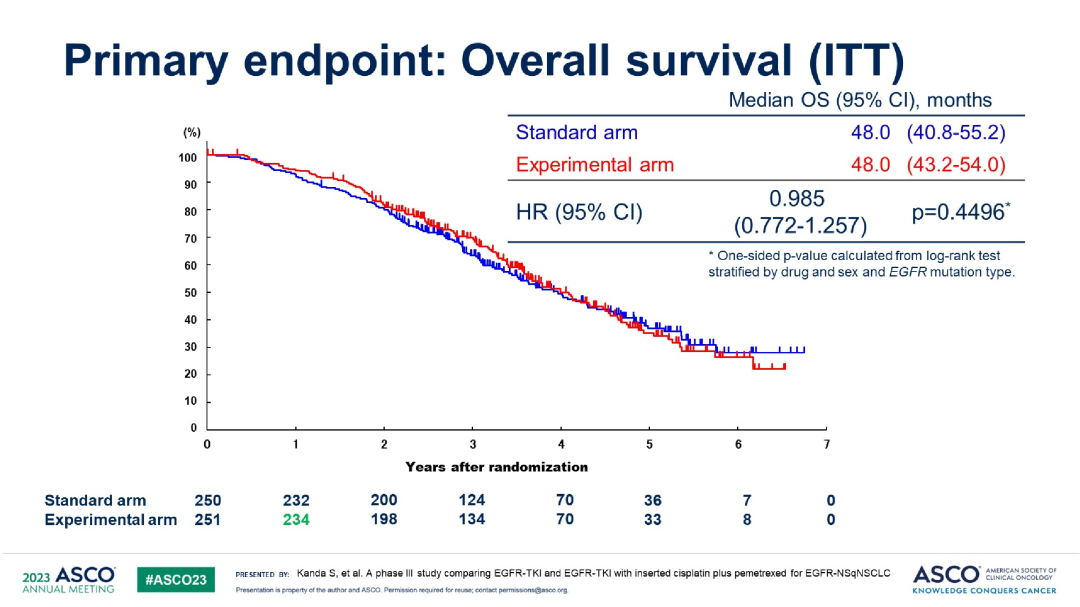
OS
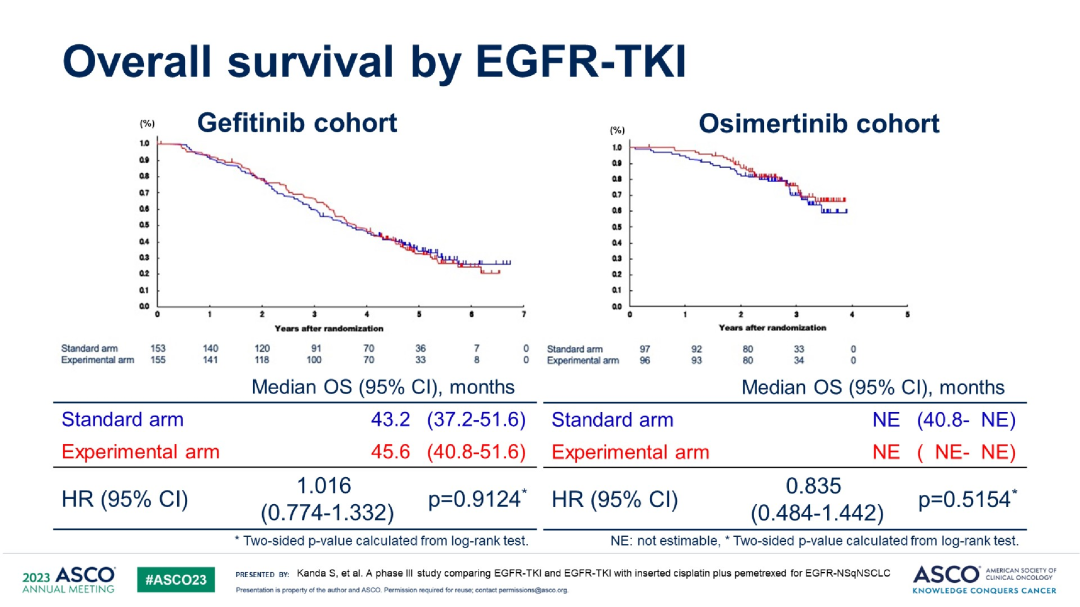
按不同靶向药分组的OS
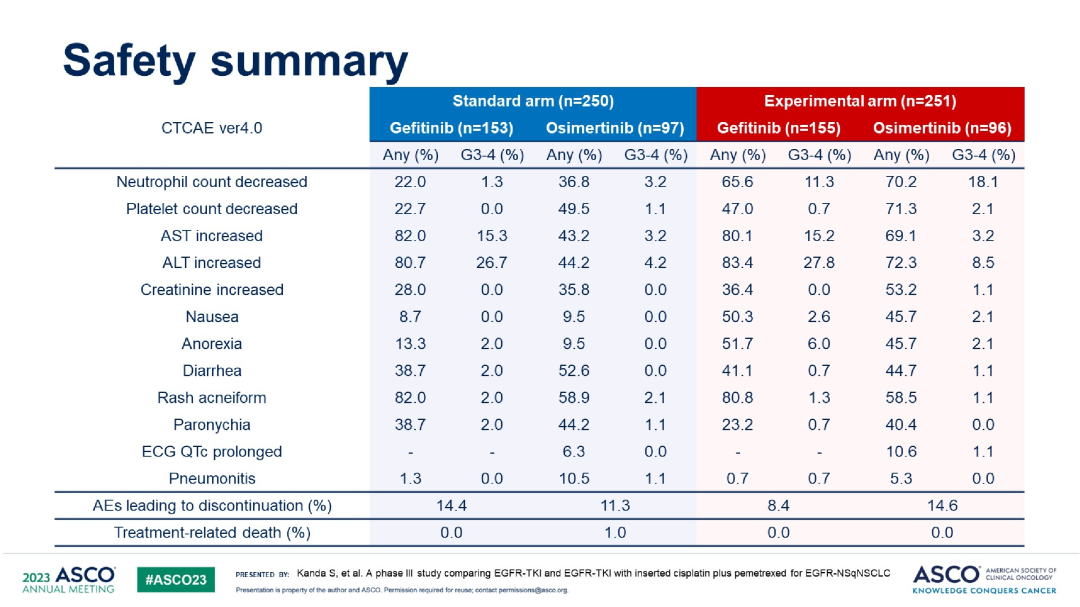
靶向耐药治疗
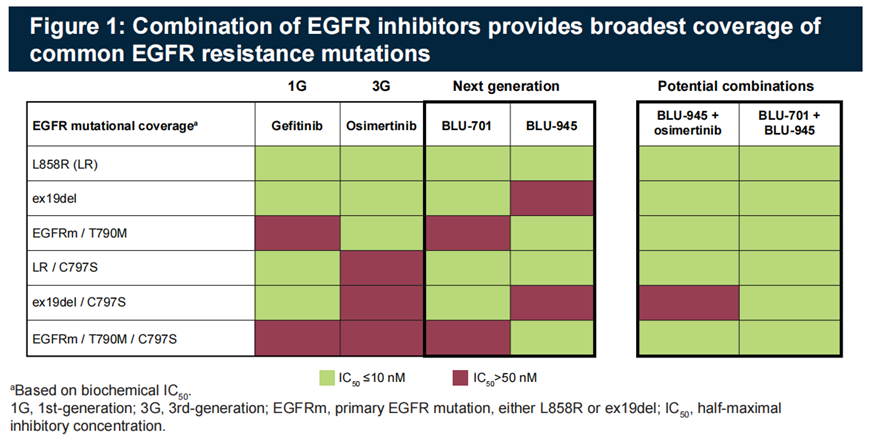
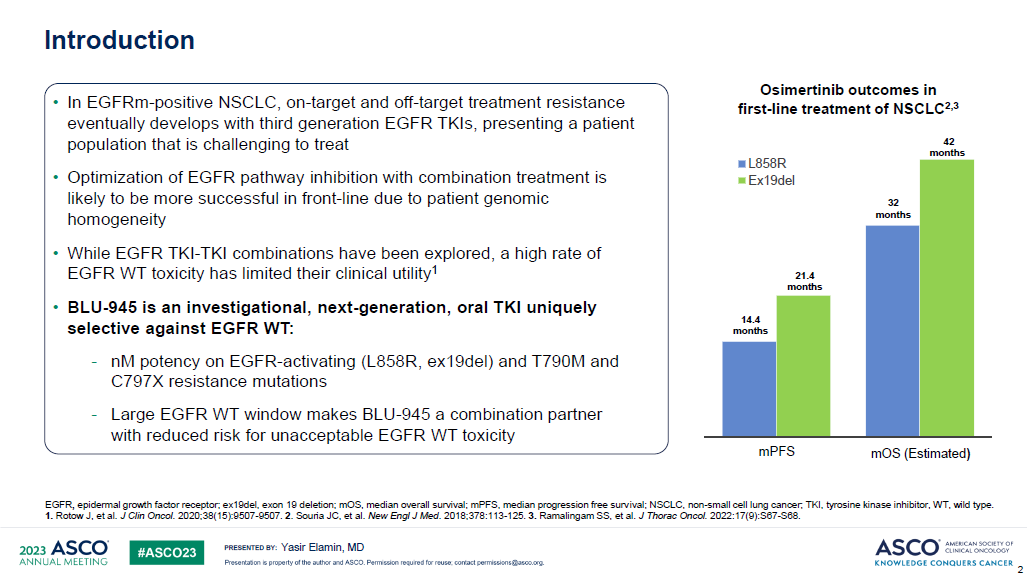

研究结果:BLU-945单药组,纳入112例三代EGFR-TKI耐药的晚期NSCLC患者,剂量范围25–600 mg qd或100–300 mg bid。大部分治疗相关不良反应为1-2级,有12例患者在每日400-600mg时出现剂量限制毒性,最常见的为3级ALT和AST升高。有2例患者死于不良反应,1例为肺炎(BLU-945 300mg bid),1例为颅内出血(BLU-945 100mg bid)。
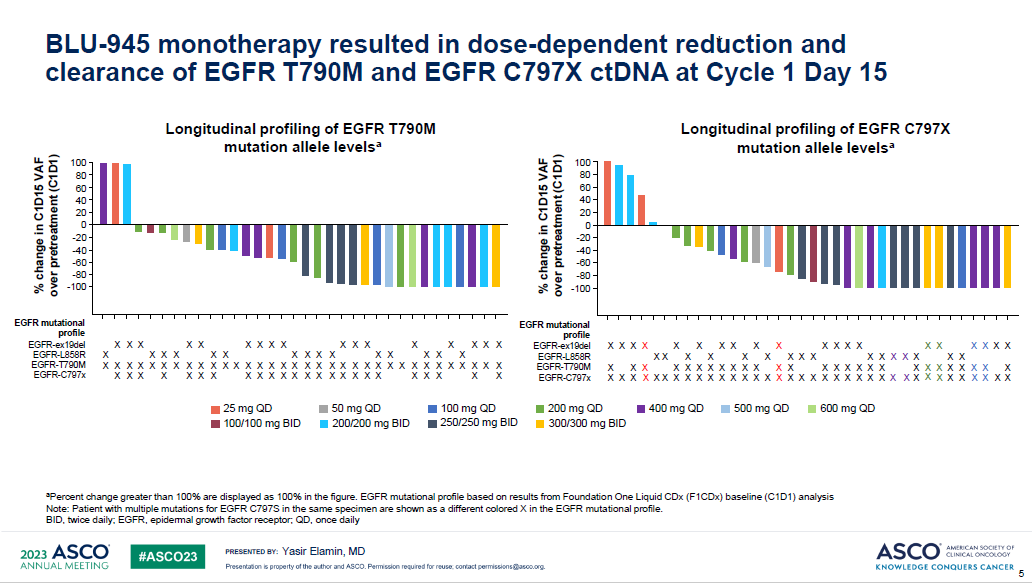
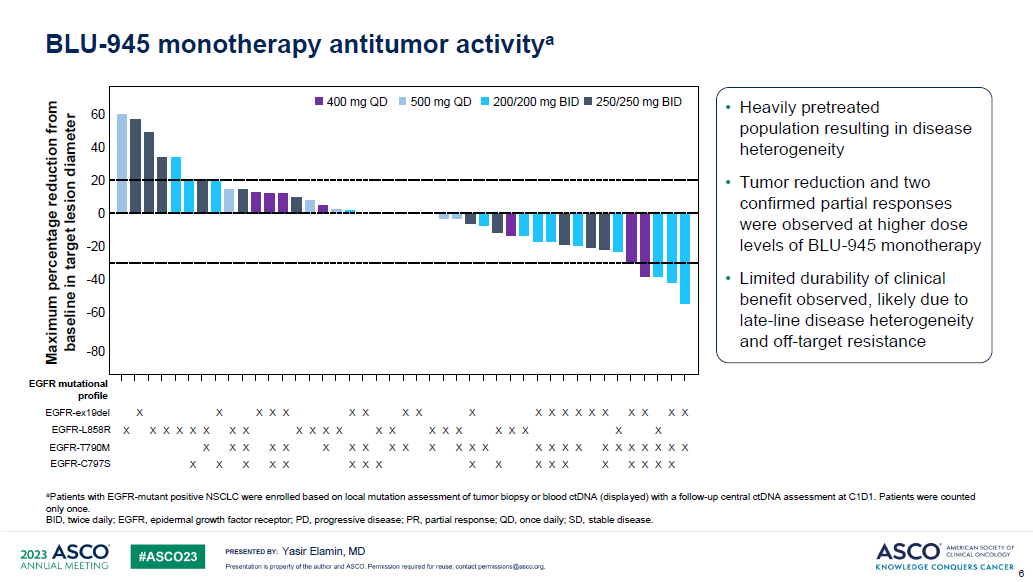
第15天的ctDNA检测结果显示,绝大多数患者的T790M和C797X突变丰度下降。其中4例患者部分缓解,剂量分别为200mg bid 3例,400mgqd1例。
BLU-945+奥希替尼组,纳入55例三代EGFR-TKI耐药的晚期NSCLC患者,剂量范围200–400 mg qd或100–200 mg bid。≥3级的治疗相关不良反应为10.9%,EGFR靶向相关副作用主要是腹泻、皮肤干燥、痤疮样皮肤炎和甲沟炎,多为1级。3例患者发生剂量限制毒性,3级急性呼吸衰竭、4级肺炎、3级皮疹各1例。没有治疗相关性死亡病例。2期推荐剂量(RP2D)仍未确定。

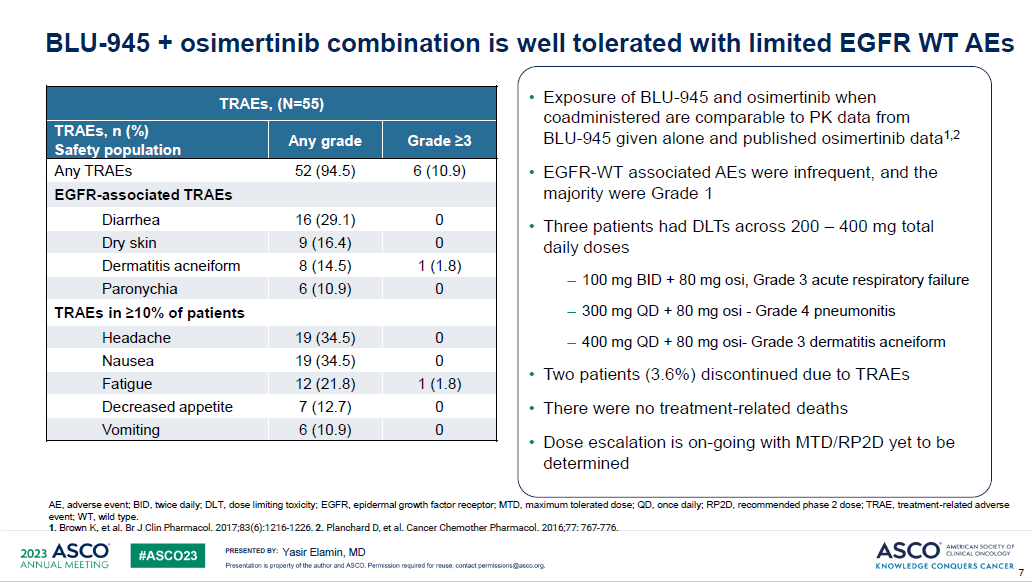
第15天的ctDNA检测结果显示,绝大多数患者的T790M和C797X突变丰度下降。其中9例患者部分缓解,剂量如下图所示。
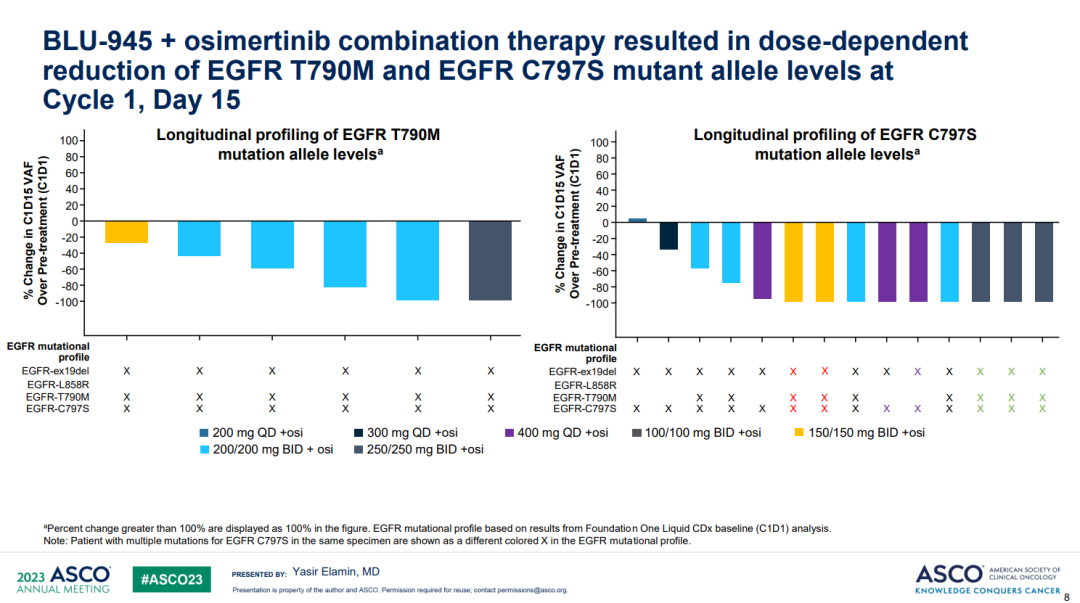

小结:在多线治疗后的EGFR突变NSCLC患者中,BLU-954治疗展现出一定的疗效,安全性可耐受,然而疗效有待提高。
CHRYSALIS-2研究:是一项正在进行的I/Ib期研究,评估Amivantamab+lazertinib对EGFR NSCLC患者的疗效。D队列纳入108例奥希替尼耐药且未经化疗的EGFR突变晚期患者接受Amivantamab+Lazertinib治疗,本次会议公布了生物标志物研究结果。

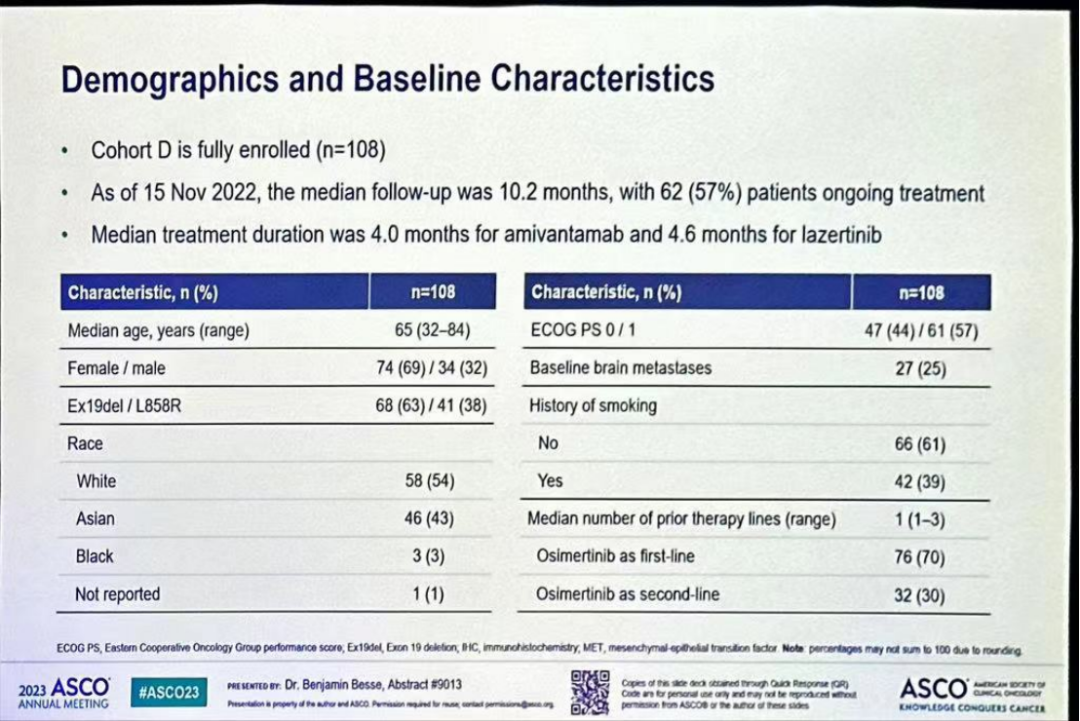
研究结果:87例患者具有可检测的基线ctDNA,77名患者具有可评估的MET IHC。训练集(n=50)确定了基于IHC在≥25%肿瘤细胞中染色为3+(MET+)可以作为潜在的生物标志物,验证集(n=27)证实了该结果。研究共有28例为MET+,MET+患者总ORR率为61%(95%CI,41-78),中位PFS为12.2个月;而MET-患者总ORR率为12%,中位PFS为4.1个月。

值得注意的是,ctDNA NGS评估没有发现符合预先设置的预测性生物标志物标准。只有1例患者的ctDNA结果为MET扩增(同时IHC也为MET+)。
 EGFR靶向耐药,单抗和ADC药物疗效
EGFR靶向耐药,单抗和ADC药物疗效
舒沃替尼(DZD9008)是一款口服、不可逆的、针对多种EGFR突变亚型的、高选择性EGFR抑制剂。舒沃替尼针对经治的EGFR exon20ins突变型NSCLC的两项关键性研究正在进行中【包括全球II期关键研究“悟空1 B部分”(WU-KONG1 Part B ,NCT03974022)和中国II期关键研究“悟空6”(WU-KONG6,NCT05712902)】;WU-KONG6初步结果显示,舒沃替尼具有良好的疗效和安全性。此外,针对初治EGFR exon20ins突变患者的两项研究也在进行中【“悟空1 A部分”(WU-KONG1 Part A)和“悟空15”(WU-KONG15,NCT05559645)】,本文首次报道了舒沃替尼对该人群的初步疗效分析结果。
WU-KONG1是一项全球多中心I/II期研究,WU-KONG15是一项中国研究者发起的II期研究,两项研究均纳入了初治的EGFR exon20ins突变型晚期NSCLC患者。入组患者接受舒沃替尼单药口服治疗(剂量:200mg QD或者300mg QD)。
研究结果:截至2023年2月21日,共28例初治的EGFR exon20ins突变患者纳入疗效分析集,超过12种突变亚型。舒沃替尼单药一线治疗EGFR exon20ins突变患者,在RP2D剂量(300mg QD)下的最佳客观缓解率(ORR)达77.8%。
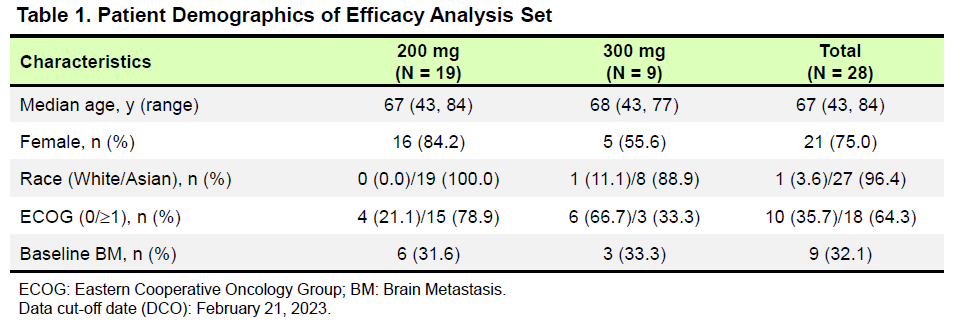
汇总分析的基线特征
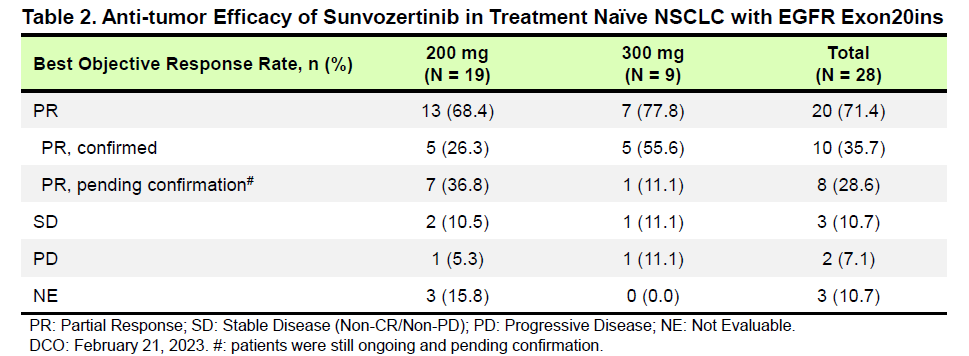
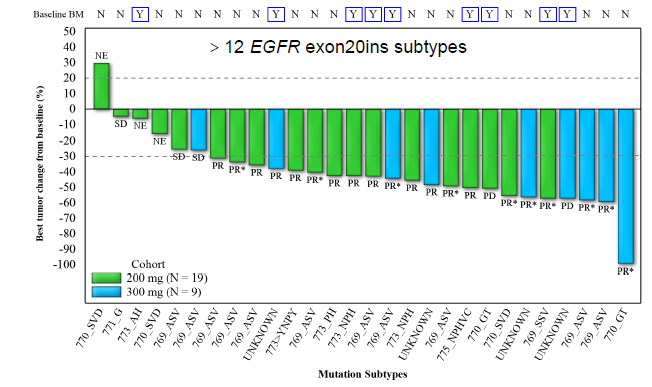
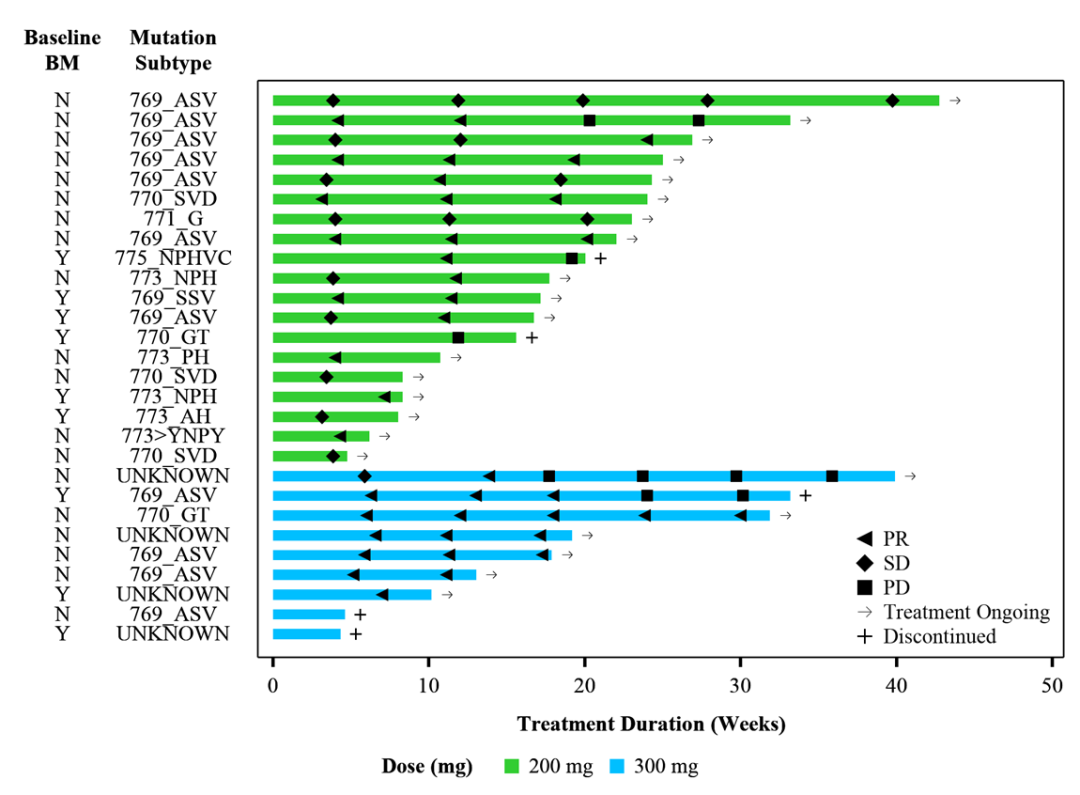
治疗持续时间
非小细胞肺癌-靶向治疗部分
围术期免疫治疗
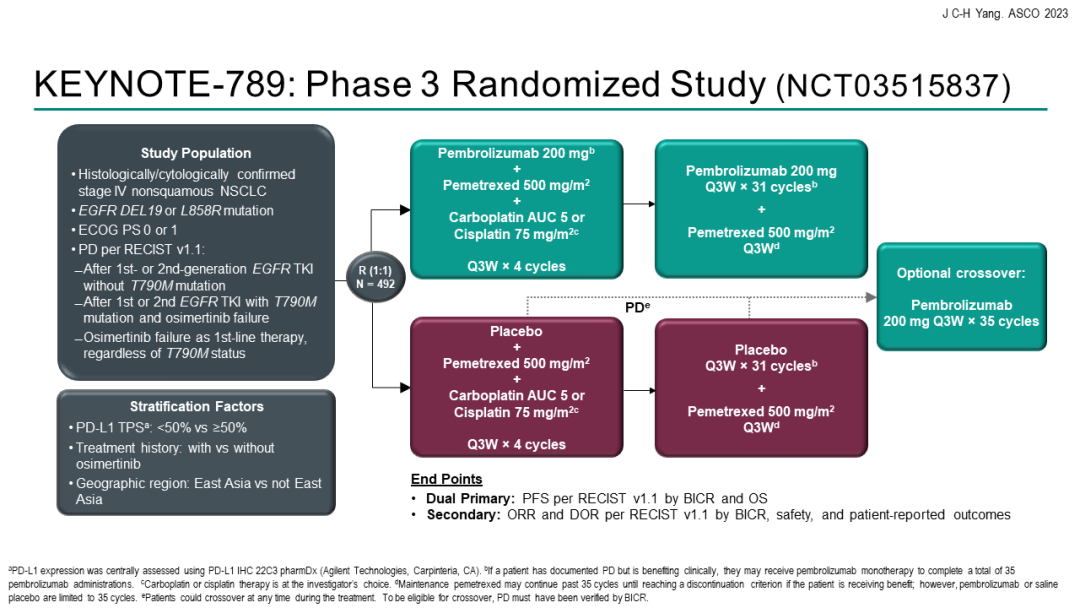
KEYNOTE-671研究[3]:是一项随机、双盲、 3期试验, 旨在评估帕博利珠单抗联合化疗新辅助治疗用于可切除的 Ⅱ、ⅢA、ⅢB 期非小细胞肺癌患者,并在术后接受帕博利珠单抗单药辅助治疗的疗效与安全性。可手术切除的Ⅱ、ⅢA、ⅢB期(N2期)NSCLC参与者以1:1比例分配接受帕博利珠单抗(200 mg)或安慰剂新辅助治疗,每3周一次,两组均联用4个周期以顺铂为基础的化疗,随后进行手术;再接受帕博利珠单抗(200 mg)或安慰剂辅助治疗,每3周一次,最多13个周期。研究分层因素包括PD-L1表达水平、病理学类型和肿瘤疾病分期。研究主要终点是无事件生存期(EFS)和总生存期(OS);关键次要终点为病理学完全缓解率(pCR)、主要病理学缓解率(mPR)。
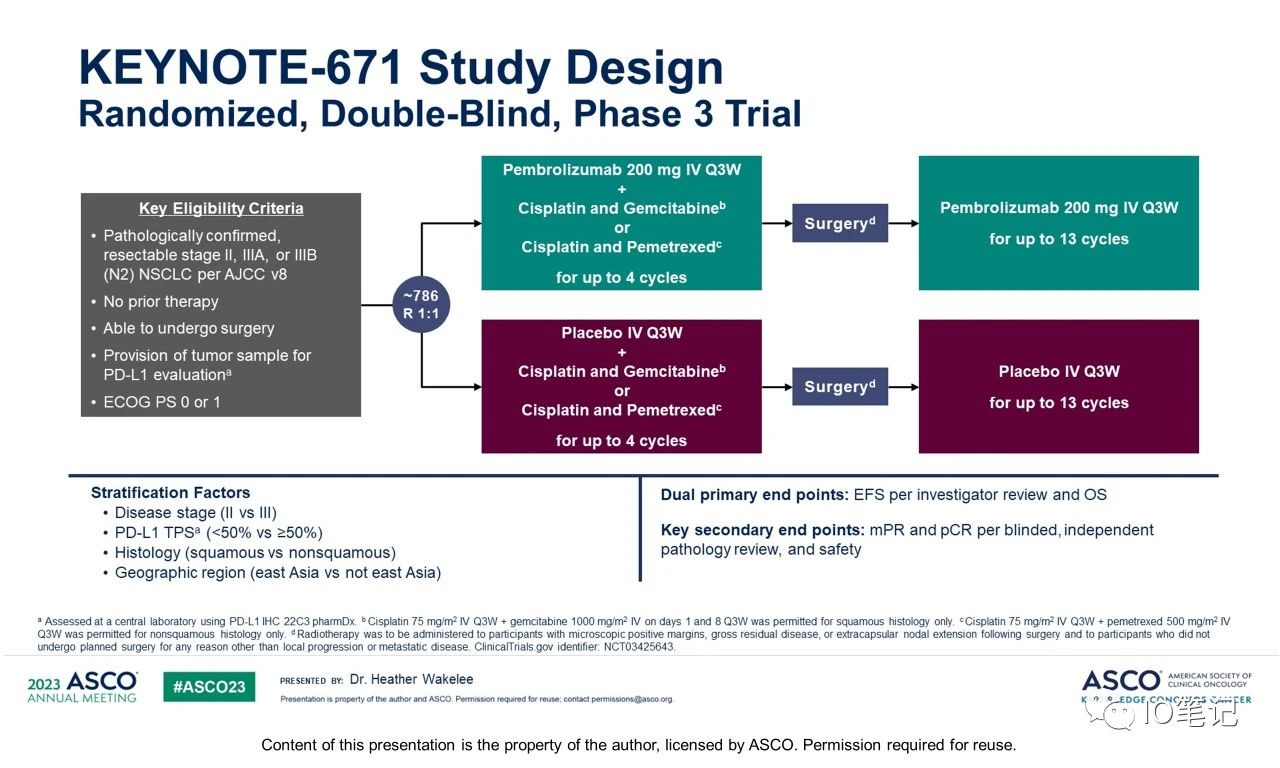
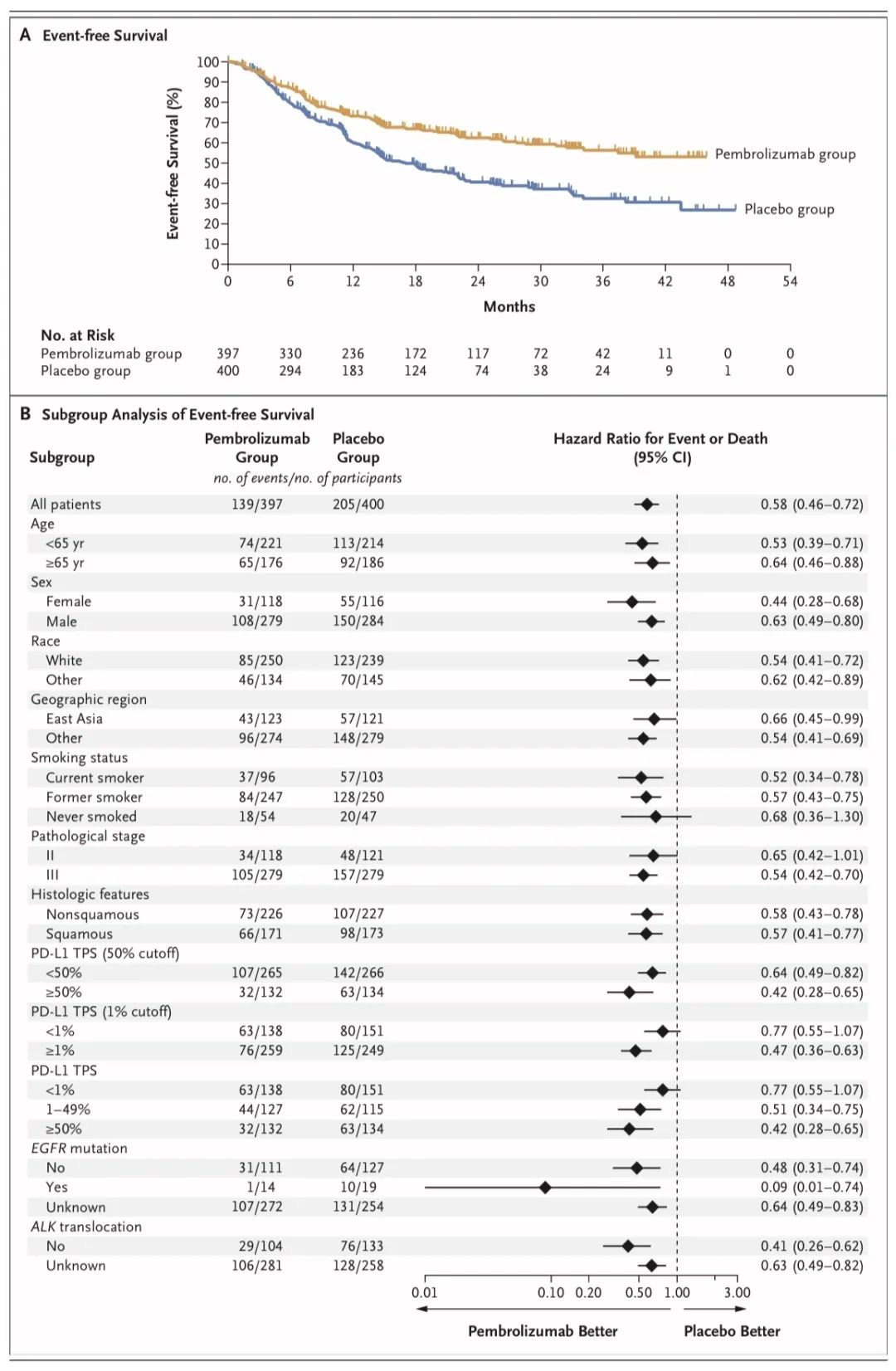
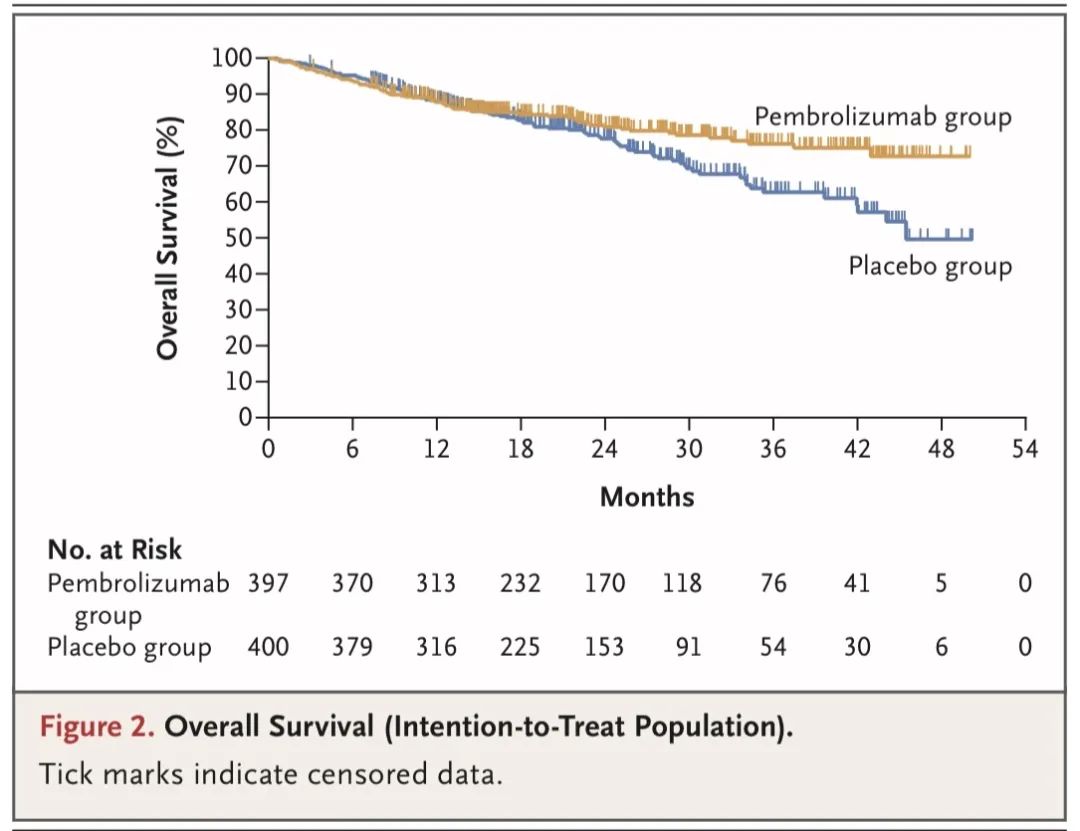
↑ 总生存率
← 无事件生存率
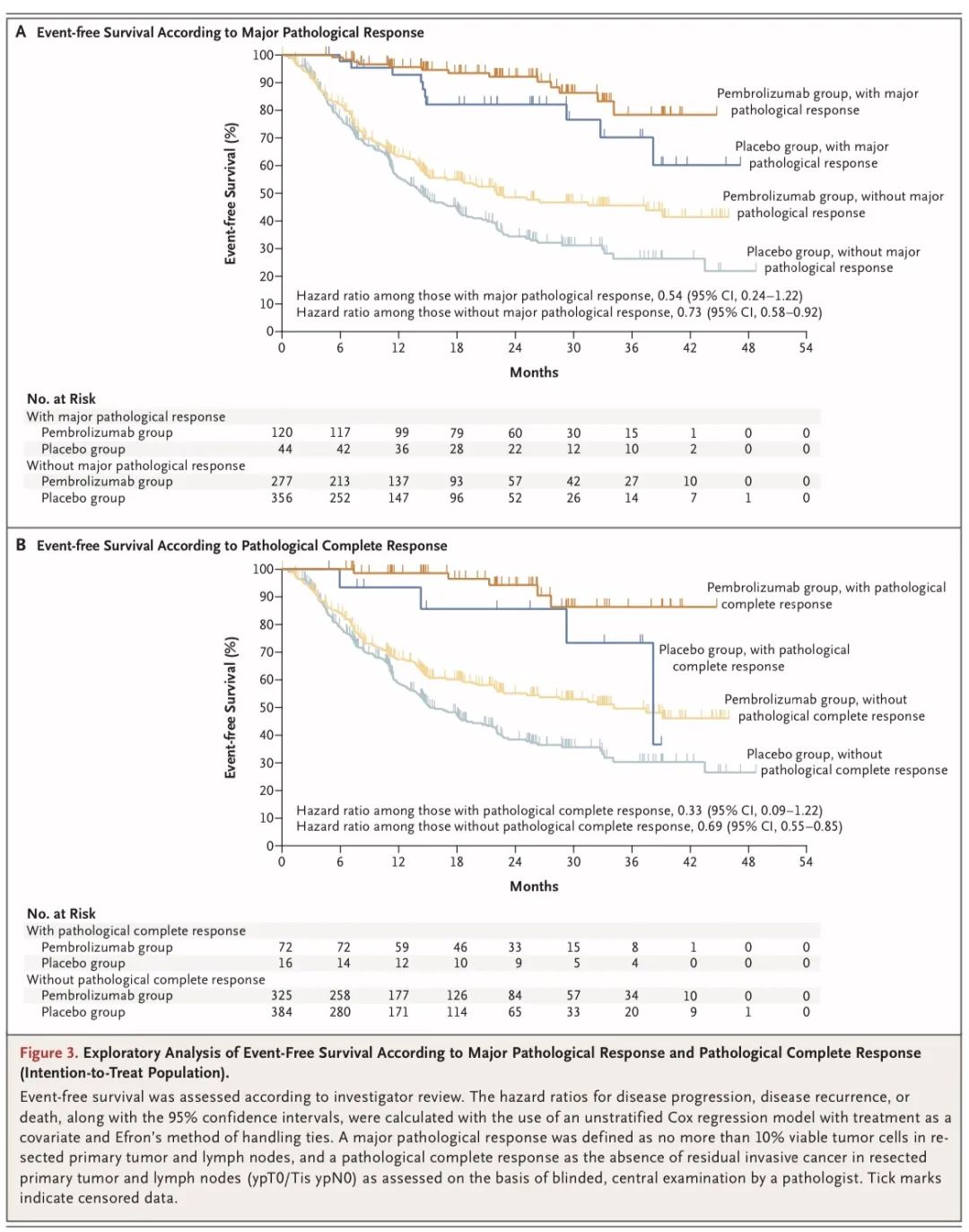
探索性分析
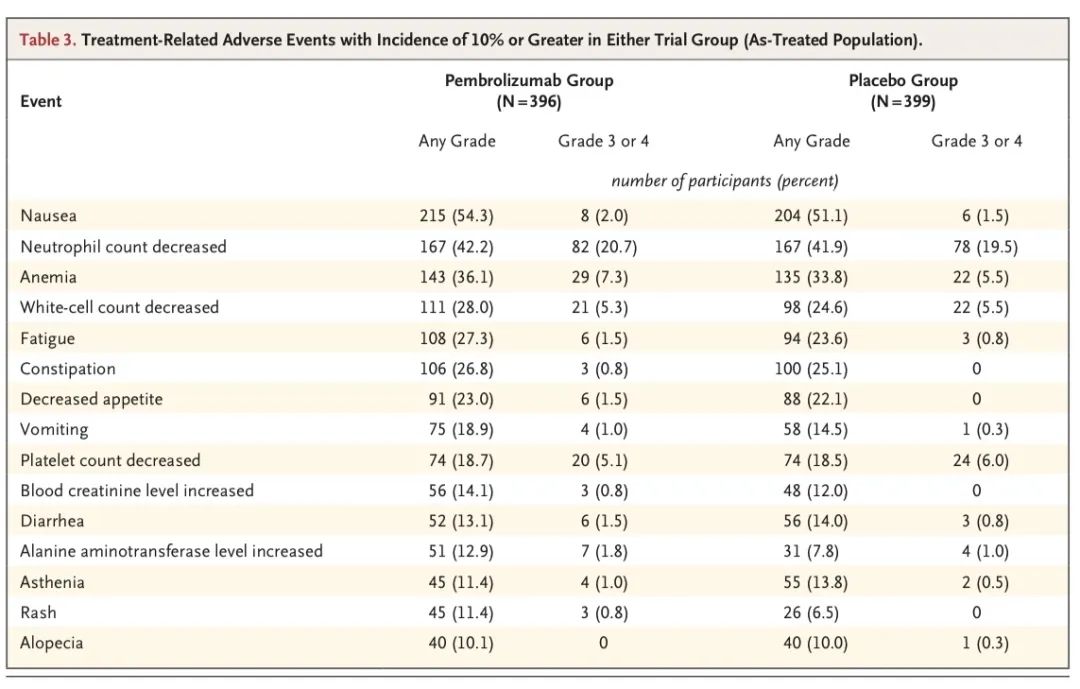
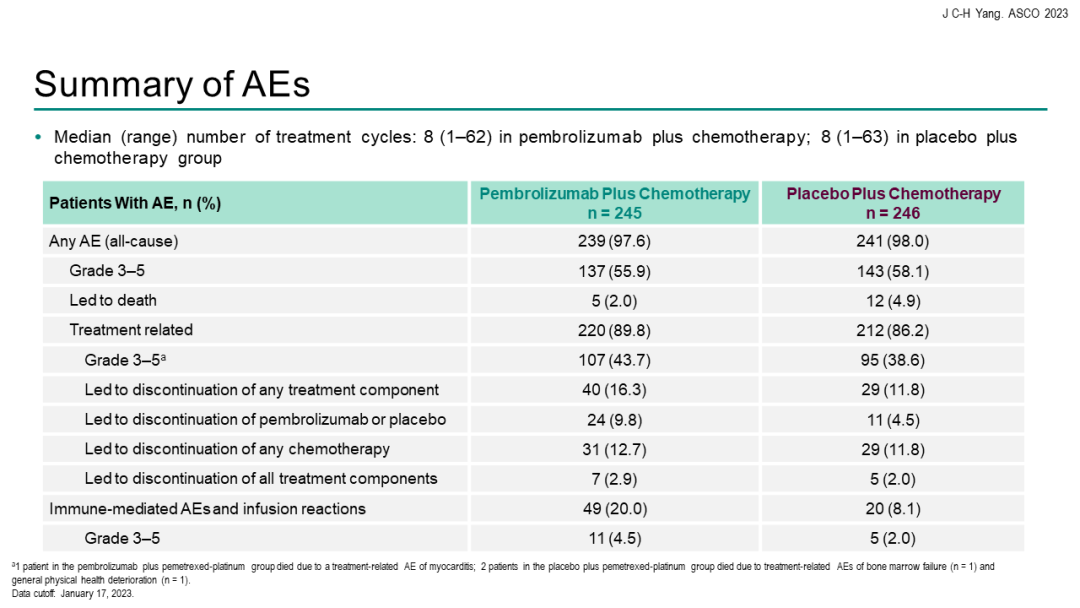
不良反应
安全性:在所有治疗阶段,帕博利珠单抗组和安慰剂组分别有44.9%和37.3%的参与者发生了≥3级治疗相关不良事件,分别有1.0%和0.8%的参与者发生了5级事件。在整个治疗期间,有7名患者因治疗相关的不良事件死亡,其中帕博利珠单抗组有4名(在新辅助-手术阶段,各有1人死于免疫介导的肺部疾病、肺炎和心脏猝死;在辅助治疗阶段1人因心房颤动死亡),安慰剂组3名(在新辅助治疗-手术阶段,急性冠状动脉综合征、肺炎和肺出血各导致1人死亡)。
Neotorch研究:是一项随机、双盲、安慰剂对照的III期临床研究,旨在比较特瑞普利单抗或安慰剂联合化疗用于II/III期可手术NSCLC患者围手术期治疗的疗效和安全性。研究计划纳入II-III期NSCLC患者500名,以1:1的比例随机接受特瑞普利单抗或安慰剂联合化疗术前3周期及术后1周期治疗(鳞癌患者化疗方案为紫杉类+铂类,非鳞癌患者化疗方案为培美曲塞+铂类),随后接受特瑞普利单抗或安慰剂巩固治疗13周期。研究按照疾病分期、拟手术方式、组织学分型、肿瘤PD-L1表达情况进行分层。主要终点为研究者评估的III期及II-III期患者的EFS、BIPR评估的III期及II-III期患者的MPR。次要终点包括OS、pCR、独立评审委员会(IRC)评估的EFS、无病生存期(DFS)和安全性等。
左右滑动查看更多


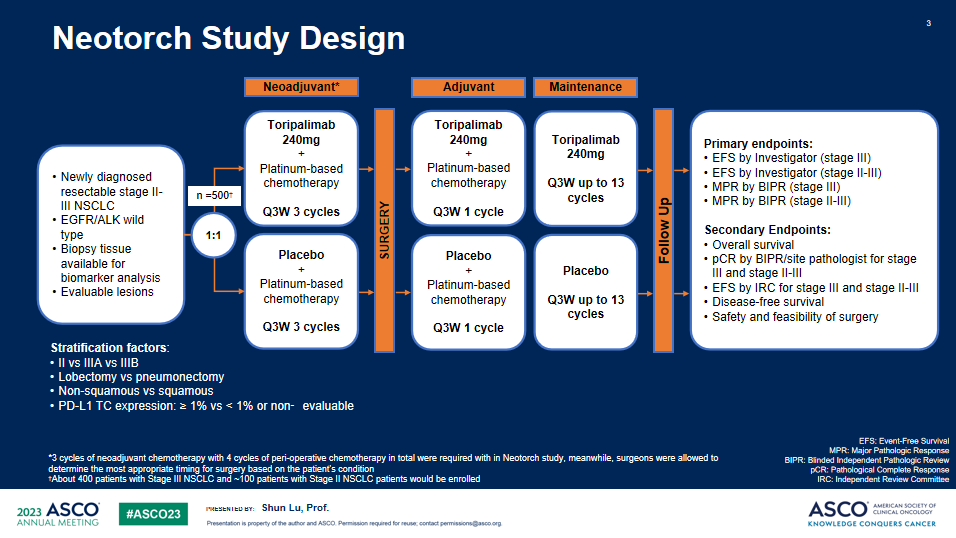
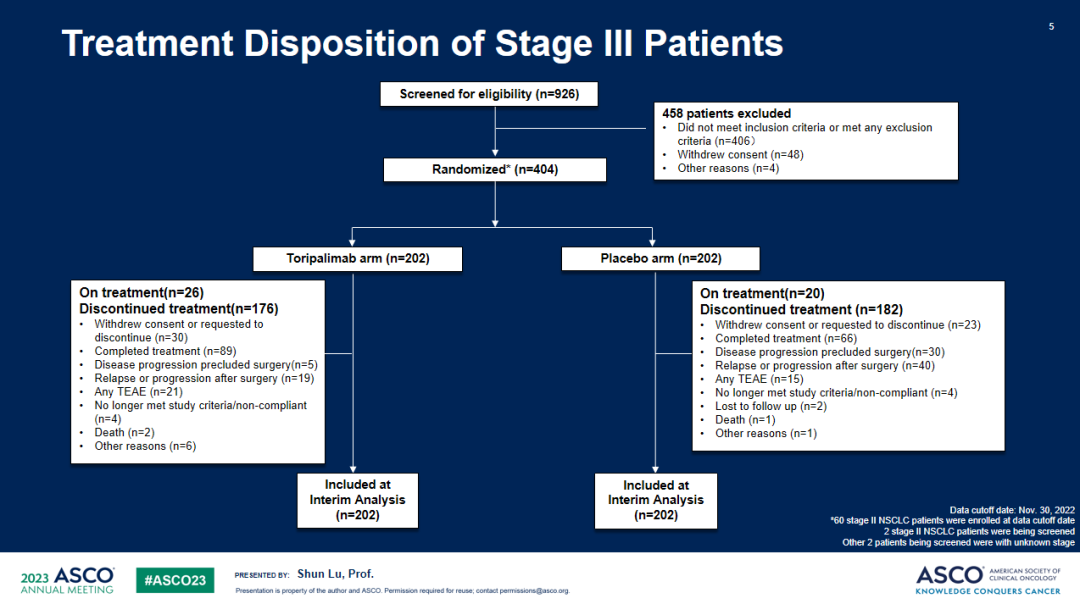
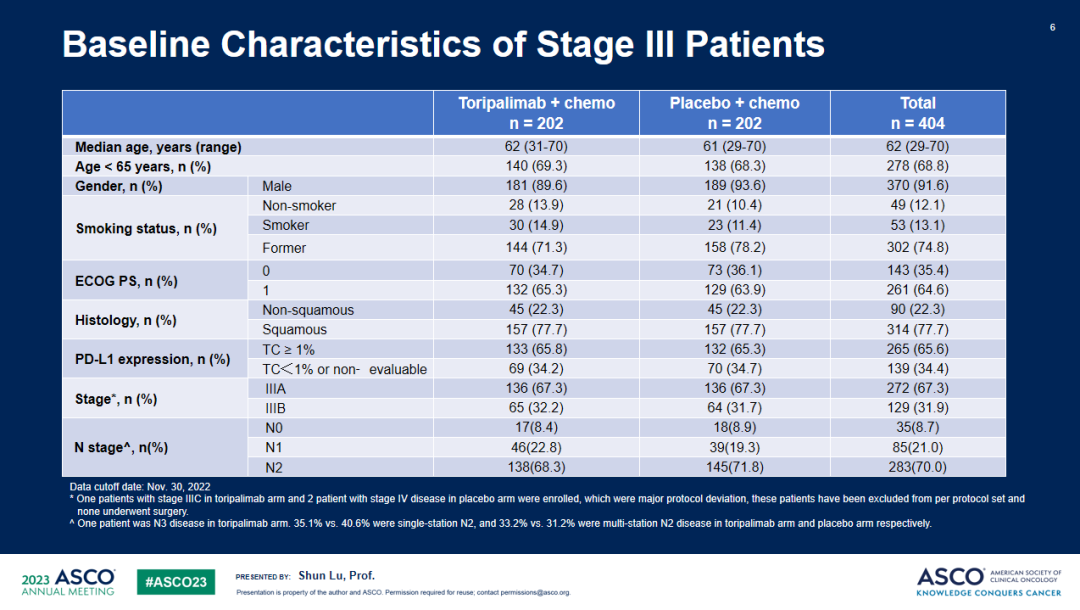
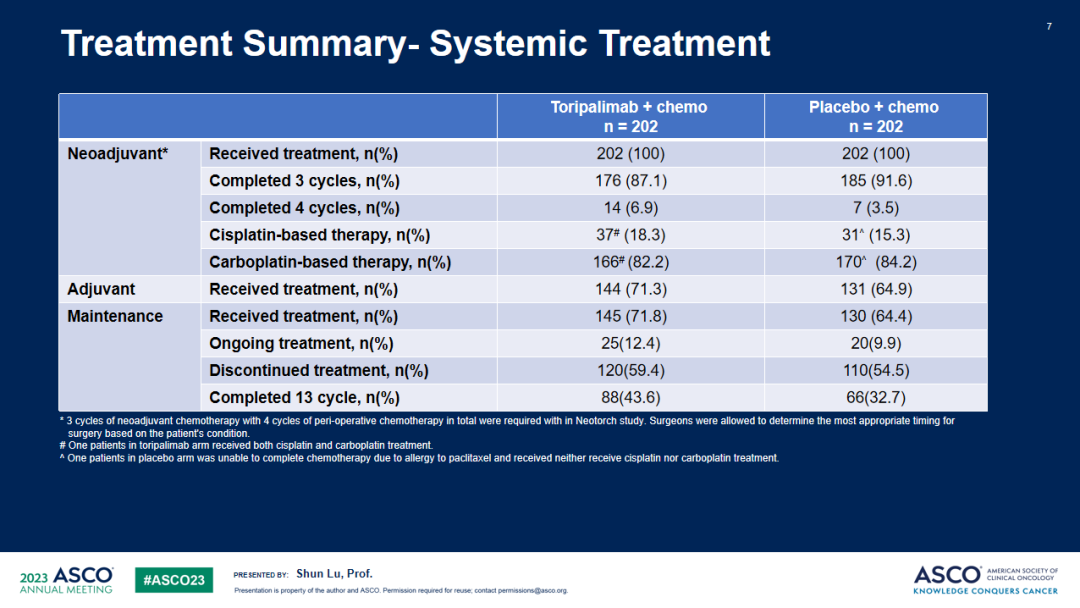
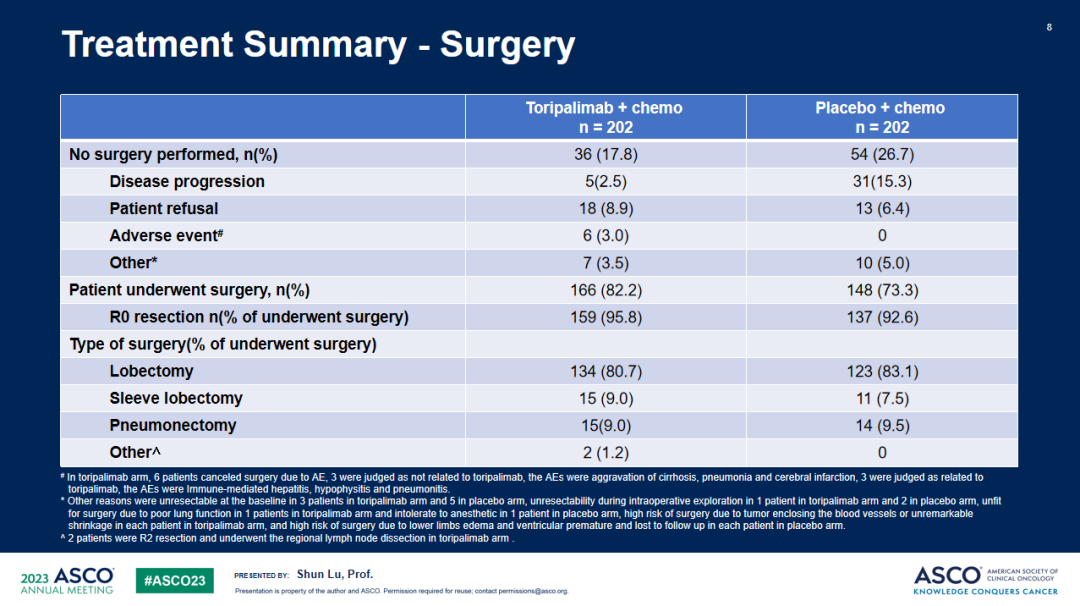
研究结果:共纳入404例III期NSCLC患者,被随机分配至特瑞普利单抗联合化疗组(n=202)或安慰剂联合化疗组(n=202),两组受试者基线特征均衡。截至2022年11月30日,共观察到144例研究者评估的EFS事件数,中位随访18.25个月。

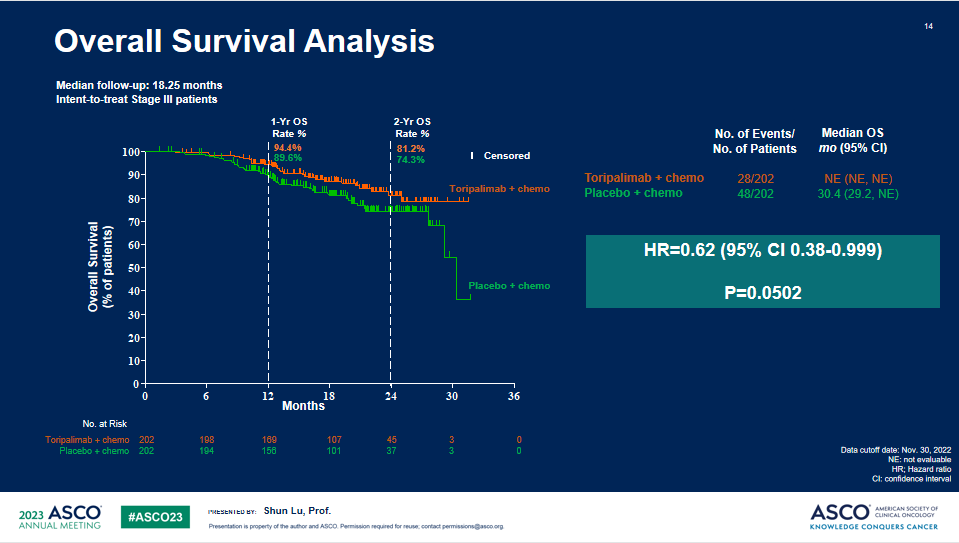
OS
a. 与安慰剂联合化疗相比,特瑞普利单抗联合化疗组EFS显著延长,中位EFS分别为 尚未成熟 vs 15.1个月 (HR=0.40;95%CI:0.277-0.565)。所有关键亚组中均观察到特瑞普利单抗联合化疗组的EFS获益。b. OS描述性分析显示,特瑞普利单抗联合化疗组有明显的OS获益趋势:两组中位OS分别为未成熟 vs 30.4个月, HR = 0.62(95% CI: 0.381-0.999)。
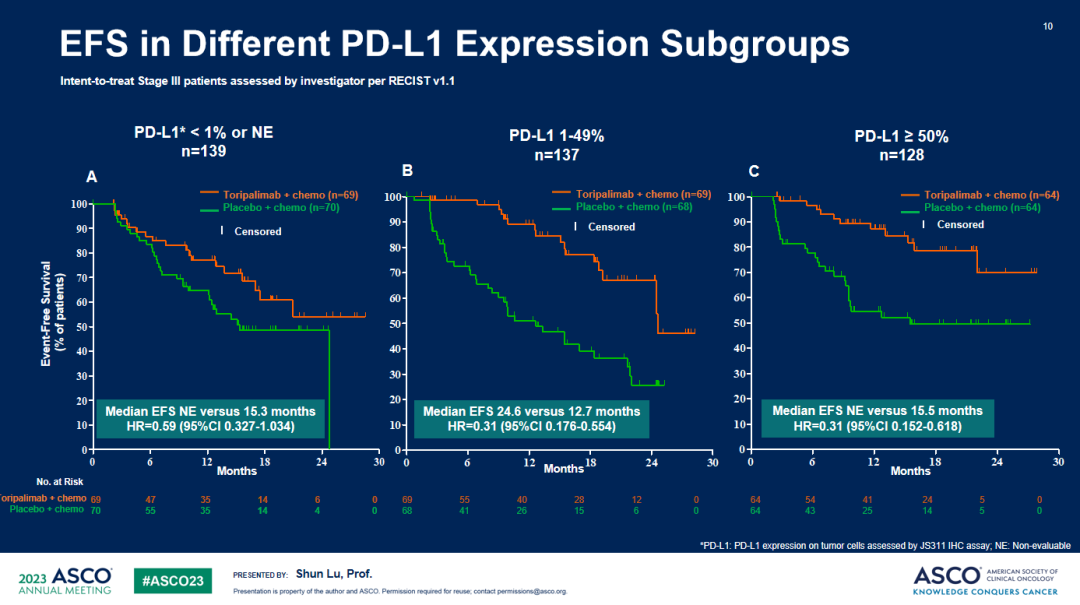
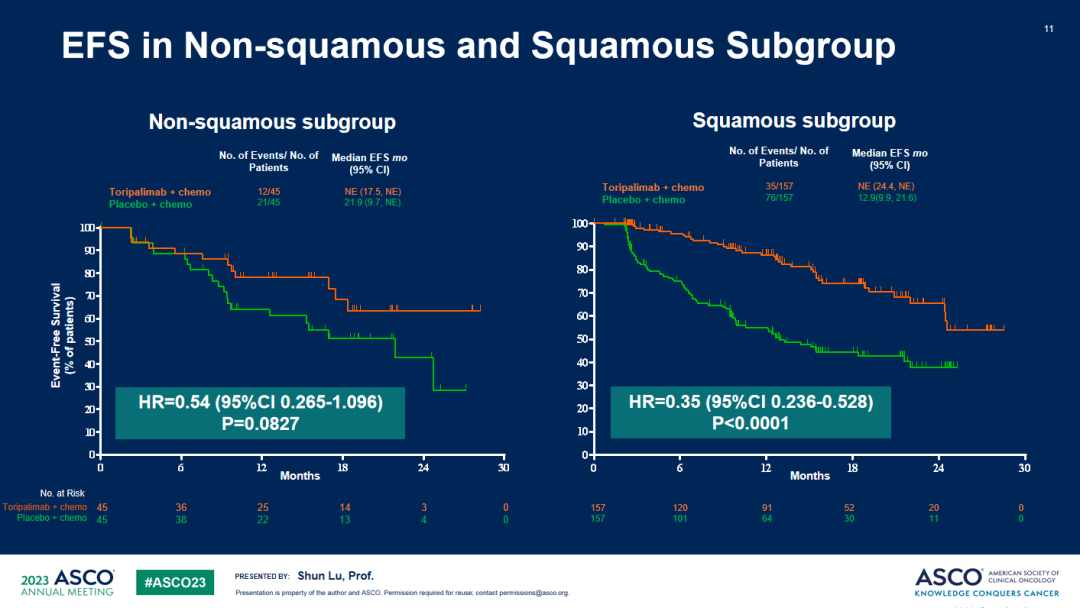 EFS亚组分析2
EFS亚组分析2
c. 特瑞普利单抗联合化疗组的MPR及pCR率均明显高于安慰剂联合化疗组,BIPR评估的MPR率分别为48.5% vs 8.4%(P<0.0001)、pCR率分别为24.8% vs 1.0%(P<0.0001)。
 MPR
MPR

pCR
安全性方面,两组治疗期间出现的不良事件(TEAE)发生率相似,未发现新的安全性信号。与安慰剂联合化疗组相比,特瑞普利单抗联合化疗组发生≥3级AE(63.4% vs 54.0%)。
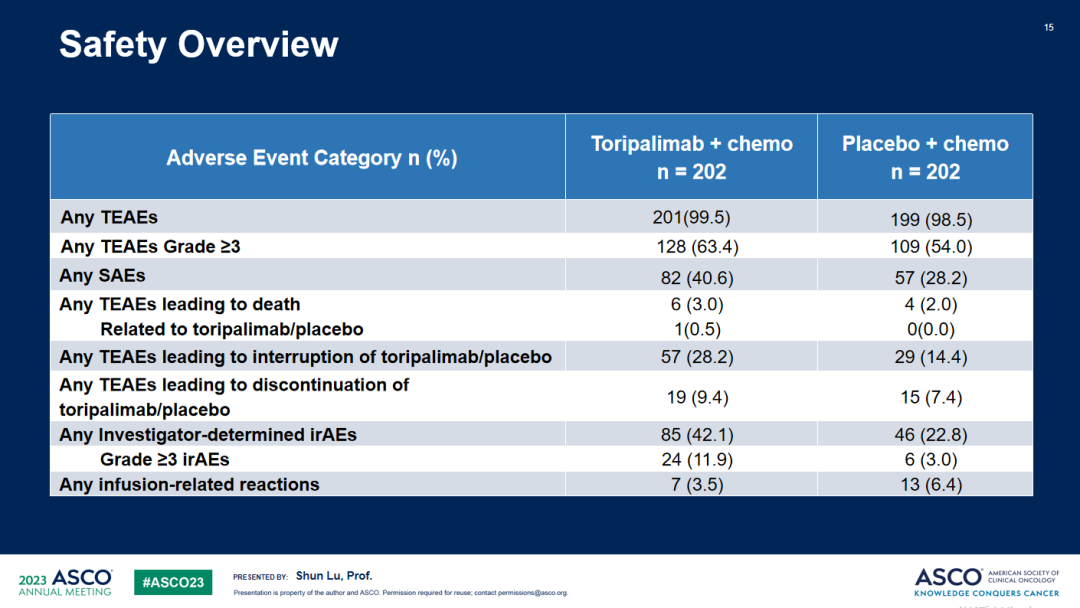
安全性
综上,与单纯化疗相比,特瑞普利单抗联合化疗围手术期治疗后特瑞普利单抗单药巩固治疗可显著改善III期NSCLC患者的EFS,提高MPR和pCR率,更多的患者可通过特瑞普利单抗联合治疗获得根治性手术的机会,且安全性可预期、可管理,未观察到新的安全性信号。患者将继续进行OS随访。
晚期免疫治疗
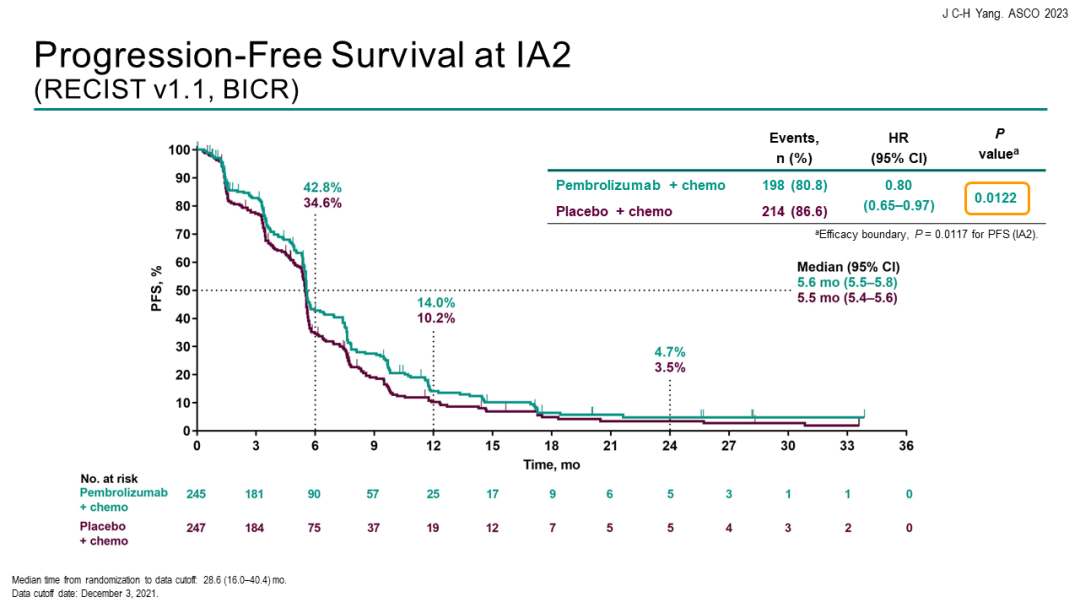
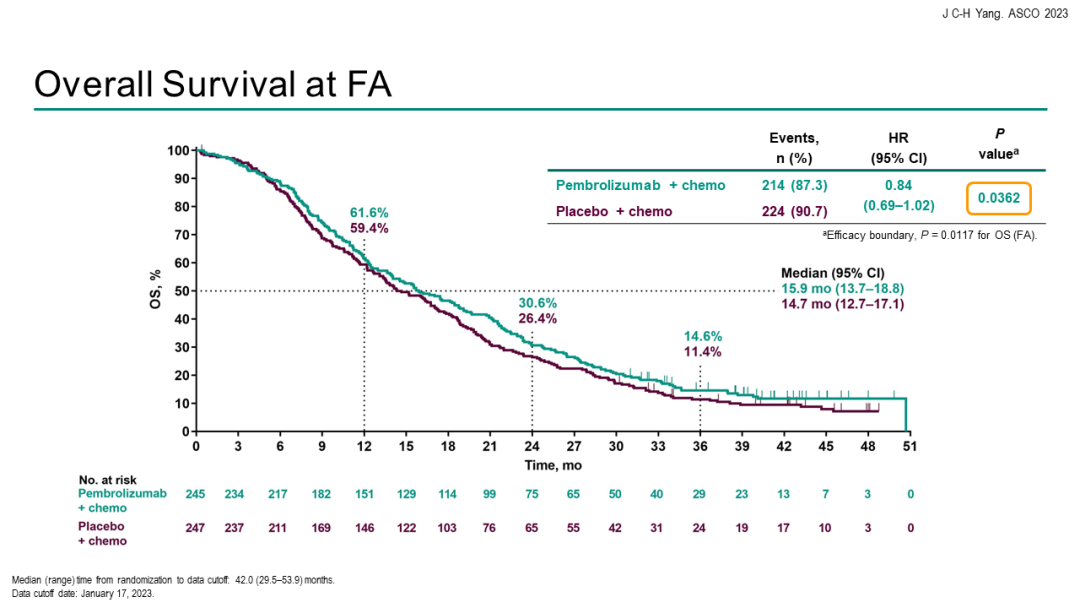
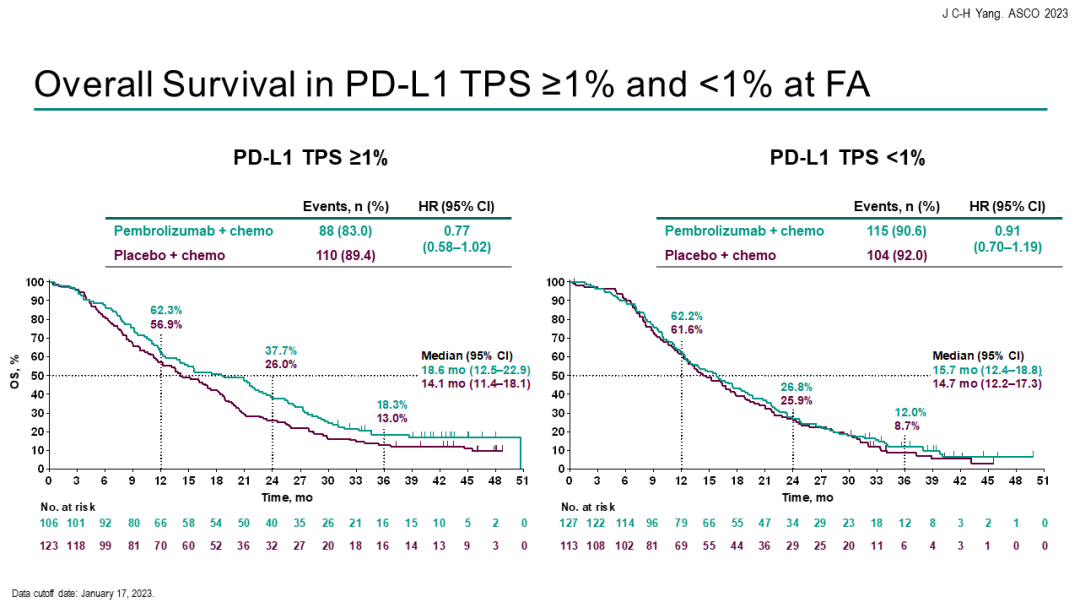
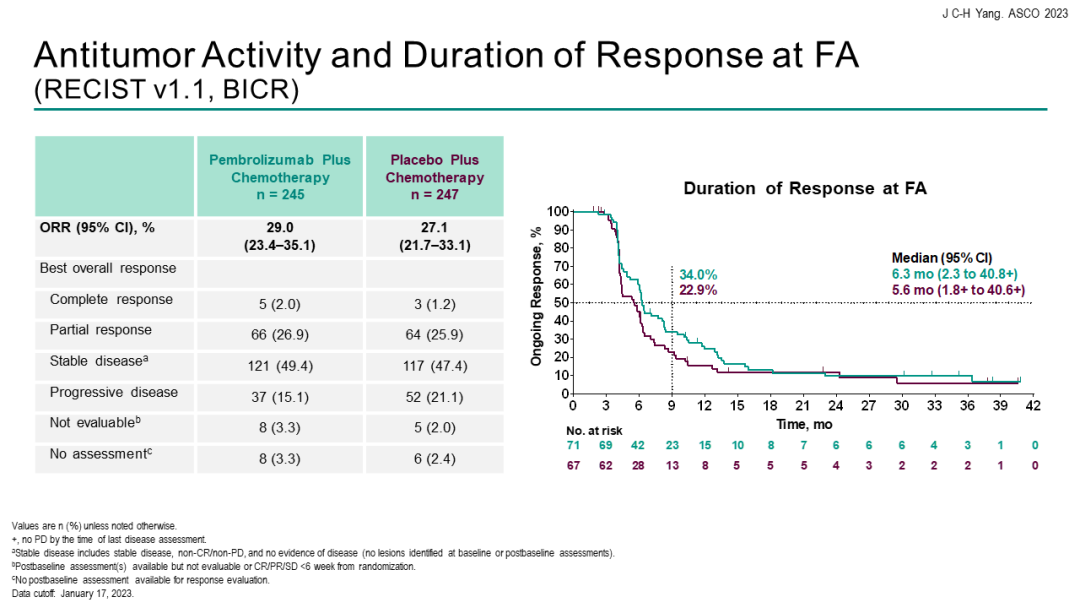
TROPION-Lung02研究[4]:是一项正在进行的全球性、开放性、六队列Ib期研究,旨在评价两种给药剂量(4 mg/kg和6 mg/kg)的Dato-DXd与帕博利珠单抗(200 mg)联合治疗伴或不伴四个周期的铂类化疗(卡铂或顺铂)在既往未经治疗或预治疗无AGA(例如:EGFR、ALK、ROS1、NTRK、BRAF、RET、MET或其他已知AGA)的晚期或转移性NSCLC患者中的安全性和疗效。TROPION-Lung02的主要终点是剂量限制性毒性和治疗期间出现的不良事件(TEAE)。次要终点包括ORR、DoR、PFS、OS等。
EGFR-TKI耐药
左右滑动查看更多


参考资料
[1]Tsuboi M, Herbst R S, John T, et al. Overall Survival with Osimertinib in Resected EGFR-Mutated NSCLC[J]. New England Journal of Medicine, 2023.
[2]Herbst RS, Wu YL, John T, et al. Adjuvant Osimertinib for Resected EGFR-Mutated Stage IB-IIIA Non-Small-Cell Lung Cancer: Updated Results From the Phase III Randomized ADAURA Trial. J Clin Oncol. 2023 Apr 1;41(10):1830-1840. doi: 10.1200/JCO.22.02186.
[3]H. Wakelee, M. Liberman, T. Kato, et al. Perioperative Pembrolizumab for Early-Stage Non–Small Cell Lung Cancer. NEJM.ORG.June 3, 2023. DOI: 10.1056/NEJMoa2302983
[4]https://mp.weixin.qq.com/s/JCS-irXnHI_FJ_a2t67axw,第一三共微信官网



来源 | e药安全
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言