FDA 批准 Selpercatinib 用于不限癌种治疗携带RET基因融合的局部晚期或转移性实体瘤患者
2022-09-26 MedSci原创 MedSci原创
2020年5月8日,美国食品药品监督管理局(FDA)批准了Retevmo(selpercatinib 40毫克、80毫克胶囊),该药物是首个被批准专门用于治疗转染重排基因(RET)融合阳性的转移性非小
2020年5月8日,美国食品药品监督管理局(FDA)批准了Retevmo(selpercatinib 40毫克、80毫克胶囊),该药物是首个被批准专门用于治疗转染重排基因(RET)融合阳性的转移性非小细胞肺癌(NSCLC)的成年患者,和需要系统性治疗的携带RET突变的晚期或转移性甲状腺髓样癌成人和12岁及以上的儿童患者,以及需要系统性治疗和放射性碘治疗(如适用)难治的RET融合阳性的晚期或转移性甲状腺癌成人和12岁及以上的儿童患者。
2021年11月9日,中国国家药监局药品审评中心(CDE)公示显示,礼来(Eli Lilly and Company)在中国提交了塞尔帕替尼(LOXO-292, Retevmo)胶囊的上市申请,并获得受理。
此次,美国FDA已加速批准Retevmo(selpercatinib)扩展适应症,不限癌种治疗携带RET基因融合的局部晚期或转移性实体瘤患者。这些患者接受前期系统性治疗后疾病进展或者没有其它满意的替代治疗选择。基于客观缓解率(ORR)和缓解持续时间(DOR),该适应症获得了加速批准。该适应症的继续批准可能取决于验证性临床试验中获得的临床获益证据。
美国FDA还授予Retevmo治疗RET基因融合的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的完全批准。FDA拓宽了Retevmo的适应症范围,纳入局部晚期疾病患者,并将2020年5月NSCLC加速批准转为完全批准。
这两项批准得到了关键性临床试验LIBRETTO-001数据 (NCT03157128) 的支持。在不限癌种患者队列中(n=41)(非小细胞肺癌和甲状腺癌以外),Retevmo达到44%的总缓解率,中位缓解持续时间为24.5个月,67%的患者缓解持续时间超过6个月。不同癌症类型患者的疗效结果请见下图:
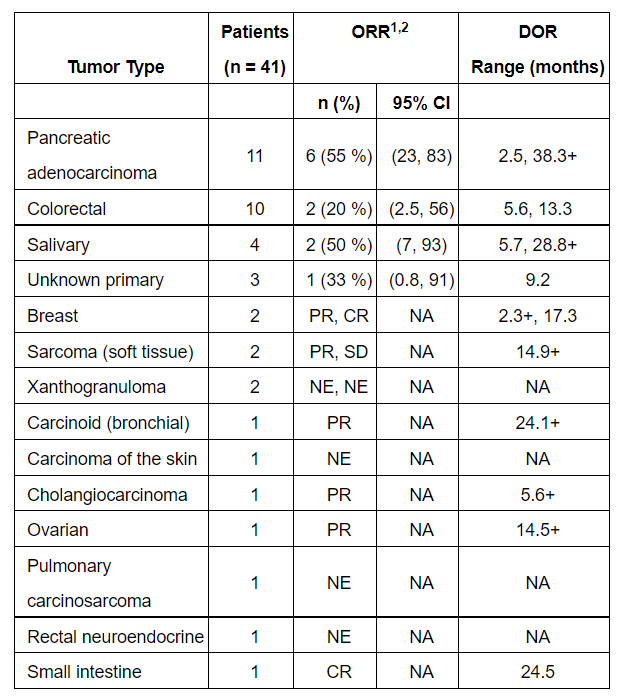
图片来源:参考资料[1]
在接受含铂化疗或初治RET融合阳性NSCLC患者中的疗效结果请见下表:
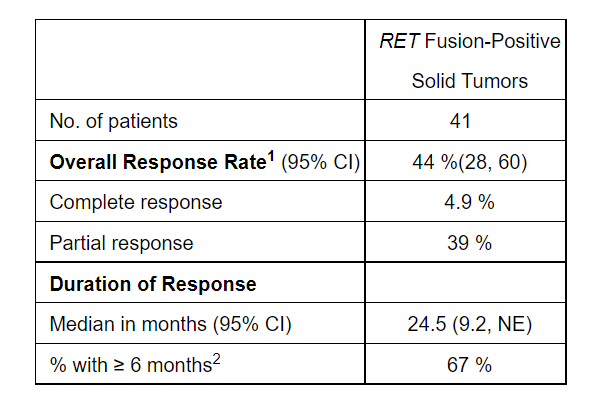
图片来源:参考资料[1]
Selpercatinib 在所有患者人群中的总体缓解率 (ORR) 为 44%(95% CI,28%-60%),其中 4.9% 的患者实现了完全缓解,39% 的患者获得了部分缓解。该药物的中位缓解持续时间 (DOR) 为 24.5 个月(95% CI,9.2 - 无法评估),67% 的患者的缓解持续至少 6 个月。
达到反应的肿瘤类型是胰腺腺癌、结直肠癌 (CRC)、唾液腺癌、未知原发性癌、乳腺癌、软组织肉瘤、支气管类癌、卵巢癌、小肠癌和胆管癌。
在 11 名胰腺腺癌患者中,该药物的 ORR 为 55%(95% CI,23%-83%),DOR 范围为 2.5 个月至 38.3 个月以上。在 10 名 CRC 患者中,使用 selpercatinib 的 ORR 为 20%(95% CI,2.5%-56%),DOR 范围为 5.6 个月至 13.3 个月。在唾液癌患者(n = 4)中,ORR 为 50%(95% CI,7%-93%),DOR 范围为 5.7 个月至 28.8+ 个月。在 3 名原发性癌症未知的患者中,该药物的 ORR 为 33%(95% CI,0.8%-91%),DOR 为 9.2 个月。
在整个疗效人群中,中位年龄为 50 岁(范围为 21-85 岁),54% 的患者为女性。此外,68% 的患者是白人,24% 是亚洲人,4.9% 是黑人。 7% 的患者是西班牙裔或拉丁裔。关于 ECOG 体能状态,95% 的状态为 0 或 1,5% 的状态为 2。大多数患者 (95%) 患有转移性疾病。 90% 的患者之前接受过全身性治疗,之前接受过 2 条线的中位数(范围,0-9)。值得注意的是,32% 的患者接受了 3 种或更多的先前治疗。
关于安全性,至少 25% 的患者最常见的不良反应包括水肿、腹泻、疲劳、口干、高血压、腹痛、便秘、皮疹、恶心和头痛。
“在LIBRETTO-001试验中,selpercatinib在RET驱动的多种癌症类型患者中表现出有临床意义和持久的缓解,包括需要新治疗选择的胰腺癌、结肠癌和其他癌症,”LIBRETTO-001合作研究者,MD安德森癌症中心的Vivek Subbiah博士说,“这些数据和美国FDA对不限癌种适应症的批准强调了对各种癌症类型患者进行常规、全面基因组检测的重要性。”
通过利用下一代测序,97.6% 的患者检测到 RET 融合,其中 2.4% 的融合是使用 FISH 鉴定的。
参考资料:
- FDA approves selpercatinib for locally advanced or metastatic RET fusion-positive solid tumors. News release. FDA. September 21, 2022. Accessed September 21, 2022. https://bit.ly/3f8Wzr7
- Retevmo. Prescribing information. Eli Lilly and Company; 2022. Accessed September 21, 2022. https://bit.ly/3Sk1wvq
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#FDA# 批准 #Selpercatinib# 用于#不限癌种#治疗携带#RET基因#融合的局部晚期或转移性#实体瘤#患者。这是又一个不限癌种的治疗获批!!相信这是大趋势,未来依据靶点治疗,越来越不限癌种,这也给一些少见的瘤种带来治疗机会!
123