Radiology:人工智能在预测胰腺癌CT淋巴结转移方面的价值
2023-01-08 shaosai MedSci原创 发表于山东省
最近,人们对应用深度学习进行癌症成像数据的LN转移预测越来越感兴趣。
 据预测,到2030年,胰腺导管腺癌(PDAC)将成为癌症相关死亡的第二大原因,在高达80%的PDAC患者中出现胰腺周围淋巴结(LNs)阳性。
据预测,到2030年,胰腺导管腺癌(PDAC)将成为癌症相关死亡的第二大原因,在高达80%的PDAC患者中出现胰腺周围淋巴结(LNs)阳性。
众所周知,术前对LN状态的评估是至关重要的。就预后而言,LN转移是PDAC生存率的独立预测因素,没有病理证实的淋巴结转移(pN0)的患者5年生存率为40%,而病理证实的转移性患者(pN1和pN2)则为10%。与标准的手术切除相比,包括剥离LN等扩大切除范围的术后可能会导致生活质量下降,且没有生存获益。到目前为止,美国国家综合癌症网络(NCCN)关于LN剥离的最佳范围的指南还没有实现。对于新辅助治疗,在可切除的PDAC患者中,化疗和手术的最佳顺序仍有争议。NCCN指南建议考虑对大面积区域性LN进行新辅助治疗。
然而,术前对LN转移进行准确的预测具有挑战性。CT被推荐为评估PDAC的LN转移的一线影像方式。然而,一项荟萃分析显示,使用CT评估胰腺癌和胆囊周围癌的区域外LN转移,其敏感性为25%,阳性预测值为28%。
最近,人们对应用深度学习进行癌症成像数据的LN转移预测越来越感兴趣。与上述研究类似,对人工划定肿瘤的依赖和未能考虑到LN特征限制了这些方法的临床转化。
近日,发表在Radiology杂志的一项研究开发并验证一个基于深度学习的全自动术前人工智能工具,该工作可用于CT成像的肿瘤和LN分割,并可实现PDAC患者LN转移的预测。
本项回顾性研究在2015年1月至2020年4月期间,对所有在本机构经手术切除、病理证实的PDAC患者进行了多排CT检查。建立了三个模型,包括AI模型、临床模型和放射组学模型。CT确定的LN转移是由放射科医生诊断的。进行多变量逻辑回归分析以建立临床和放射组学模型,这些模型的性能是根据其鉴别力和临床效用来确定的,Kaplan-Meier曲线、log-rank检验或Cox回归被用于生存分析。
总共纳入734名患者(平均年龄,62岁±9[SD];453名男性)。所有患者被分成训练组(n = 545)和验证组(n = 189)。734名患者中,有LN转移的患者(LN阳性组)占340名(46%)。在训练集中,人工智能模型在预测LN转移方面显示出最高的性能(AUC,0.91),而放射科医生和临床及放射组学模型的AUC分别为0.58、0.76和0.71。在验证集中,人工智能模型在预测LN转移方面表现出最高的性能(AUC,0.92),而放射科医生和临床及放射组学模型的AUC分别为0.65、0.77和0.68(P<0.001)。AI模型预测的LN转移阳性与较差的生存率有关(危险比,1.46;95% CI:1.13,1.89;P = .004)。
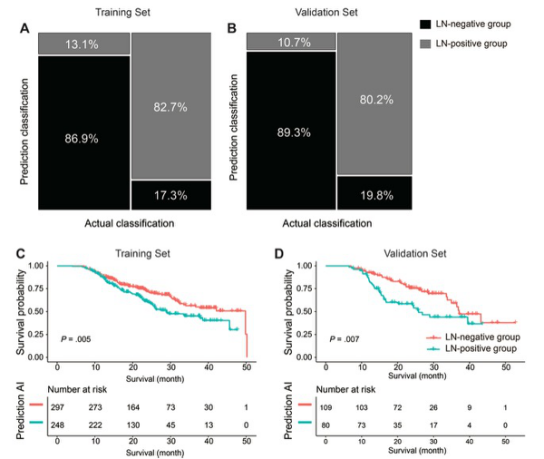
图 人工智能(AI)模型的分类和生存预测。(A) 训练集的镶嵌图。(B) 验证集的镶嵌图。(C) 预测人工智能模型的Kaplan-Meier生存曲线显示,在训练集中,淋巴结(LN)阴性组的患者生存期明显长于LN阳性组。(D) 预测AI模型的Kaplan-Meier生存曲线显示,在验证集中,LN阴性组患者的生存期明显长于LN阳性组患者
本项研究表明,本研究提出的人工智能(AI)模型是一种结合了淋巴结(LN)和肿瘤图像特征的全自动无创工具,在预测胰腺导管腺癌(PDAC)患者CT下的LN转移方面显示出良好的准确性。同时,人工智能模型的表现优于放射科医生、临床模型和放射组学模型,可以进一步为PDAC患者的个体化诊断和治疗提供临床上的有益信息。
原文出处:
Yun Bian,Zhilin Zheng,Xu Fang,et al.Artificial Intelligence to Predict Lymph Node Metastasis at CT in Pancreatic Ductal Adenocarcinoma.DOI:10.1148/radiol.220329
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言