大爆发!连发Nature和Cell,董欣年课题组在植物抗病领域取得重要突破!
2022-08-09 iPlants iPlants
董欣年课题组在植物抗病领域取得重要突破!一篇研究的结构解释了二十多年 NPR1 研究的数据。另一篇揭示了分子模式激活的免疫反应(PTI)信号通路中一个全新的蛋白翻译起始模块(Module)。
2017年5月18日,Nature杂志同一期在线发表了两篇来自美国杜克大学董欣年课题组的研究论文,分别是与华中农业大学王石平课题组题为"ORF-mediated translation allows engineered plant disease resistance without fitness costs"的研究论文,该研究采取双盲实验,通过利用uORF(上游开放阅读框)在翻译水平上精准调控NPR1的表达,能够在不影响作物产量的前提下,大大增强植物本身的免疫系统,并同时对抗多种病原体。另外一篇是题为“Global translational reprogramming is a fundamental layer of immune regulation in plants”的研究论文。该研究提出了全基因组范围的翻译重编程调控是植物免疫应答中的一种新分子机制,是PTI免疫反应的早期激活事件。继两篇Nature后,董欣年组揭示了翻译调控在ETI免疫反应中的作用!
2020年,该课题组又在一周内连续发表了Nature和Cell文章,在植物抗病领域取得重要突破,分别是:1. 2020年8月12日,Nature杂志在线发表了来自美国杜克大学董欣年课题组和美国华盛顿大学郑宁课题组合作题为“Structural basis of salicylic acid perception by Arabidopsis NPR proteins”的研究论文。 该研究通过结构生物学揭示了植物水杨酸受体NPR蛋白对水杨酸感知的分子机制。2. 2020年8月16日,Cell杂志在线发表了来自美国杜克大学董欣年课题组题为“formation of NPR1 Condensates Promotes Cell Survival during the Plant Immune Response”的研究论文。该研究揭示了植物中的NPR1通过靶向底物的泛素化和通过水杨酸诱导的NPR1聚合物(SINCs)的形成来促进细胞存活。大爆发!一周发Nature和Cell,董欣年课题组在植物抗病领域取得重要突破!
近期,董欣年团队又在两个月内连发Nature和Cell文章,这是继上次连发高水平文章后,又一在植物抗病领域取得重要突破:
1. 2022年5月12日,Nature杂志发表了来自美国杜克大学Pei Zhou和董欣年课题组合作题为"Structural basis of NPR1 in activating plant immunity"的研究论文,该研究通过低温冷冻电镜等方法成功解析了NPR1及其与转录因子 TGA3 的复合物的结构,解决了该领域一个重要的问题。

水杨酸SA是植物的防御激素,对于植物免疫至关重要。拟南芥的NPR1和NPR3/NPR4被认为是SA的受体。NPR1作为转录共激活子发挥功能,相反NPR3/NPR4作为转录共抑制因子发挥作用。SA结合刺激NPR1的转录激活活性并抑制NPR3 / NPR4的转录抑制活性,从而导致防御相关基因的诱导。受体被多个转录因子TGA2,TGA5和TGA6募集到SA反应基因的启动子上(见下图)。但是它们是如何感知SA和传递激素信号仍然是未知的。
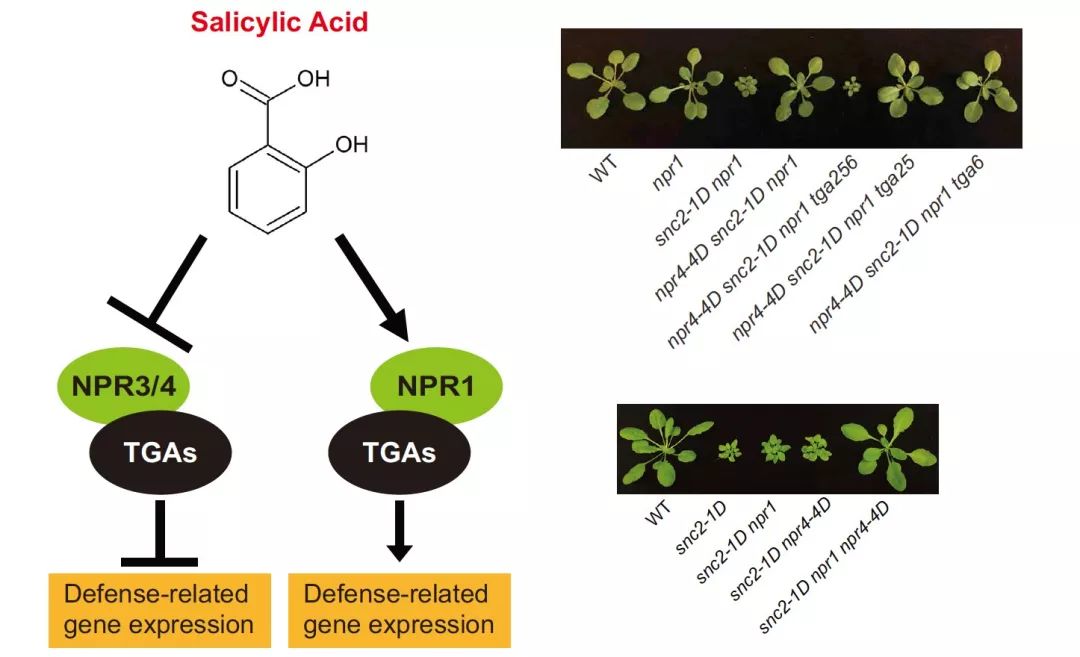
图. NPR1和NPR3/NPR4的作用模型(Cell, 2018,1454-1467)
该研究使用昆虫细胞表达和纯化了拟南芥全长NPR1,发现NPR1主要是以同源二聚体形式存在。通过低温电子显微镜解析得到3.8 Å 的分辨率的NPR1二聚体结构,其整体形状类似于一只滑翔的鸟,具体为二聚体的中心是核心 BTB 结构域,它由一个三链 β-折叠 (B1-B3) 和两侧是五个螺旋 (A1-A5)组成。另外,NPR1的BTB 结构域在 N 末端包含一个额外的二聚化螺旋结构。C 末端到 BTB 结构域,NPR1 包含一个独特的四个螺旋,成为BHB结构域。 此外,BHB 之后是四个锚蛋白重复序列(ANK)和一个无序的水杨酸-结合域(SBD) (见下图)。最后,晶体结构分析揭示了 BTB 中独特的锌指基序,用于与锚蛋白重复序列相互作用并介导 NPR1 寡聚化。
该研究在 0.2 mM SA 存在下, NPR1-SA复合物的电镜结构分析揭示了在 SA 结合状态下,NPR1 二聚体的 ANK 的 C 末端的SBD 发生了折叠并与锚蛋白重复序列(ANK)相互作用。SBD与ANK相互作用是 NPR1 促进防御基因转录所必需的,这为水杨酸直接调节 NPR1 的活性提供了结构证据。
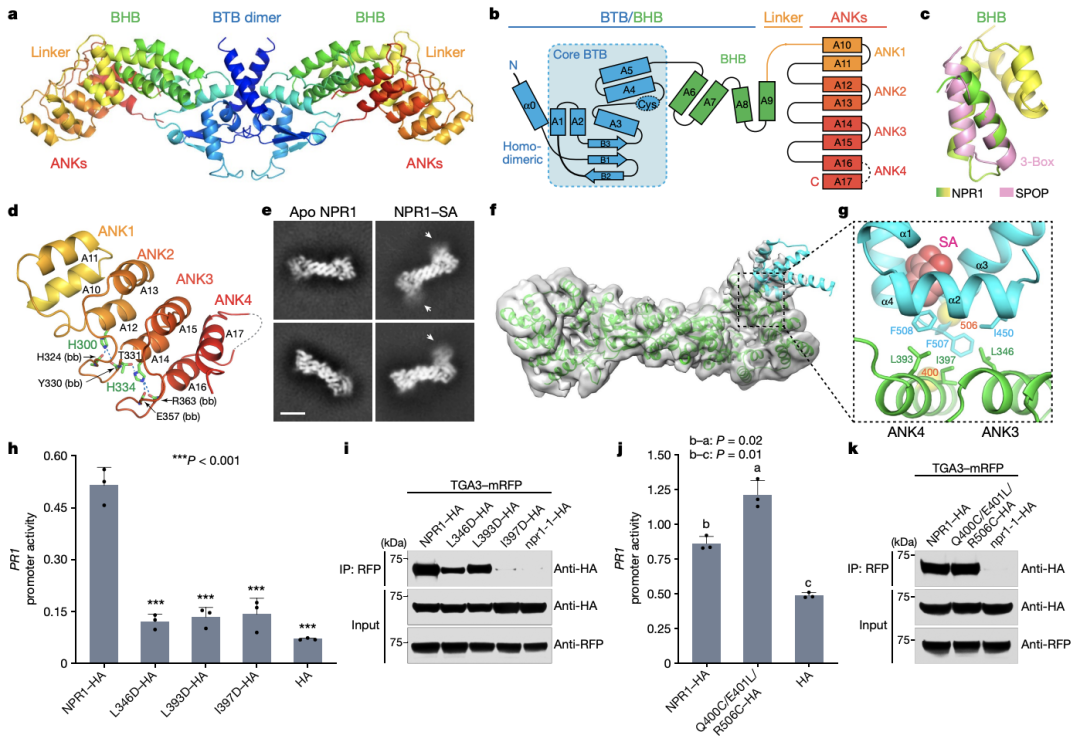
NPR1 和 NPR1-SA 的结构分析
此外,该研究还解析了TGA32-NPR12 –TGA32复合物的结构,并结合DNA 结合测定和遗传数据表明二聚体 NPR1 通过桥接两个与脂肪酸结合的 TGA3 二聚体形成复合体来激活转录。NPR1-TGA 复合物的逐步组装表明可能与其他转录因子形成异质寡聚复合物,揭示了 NPR1 如何重新编程防御转录组。
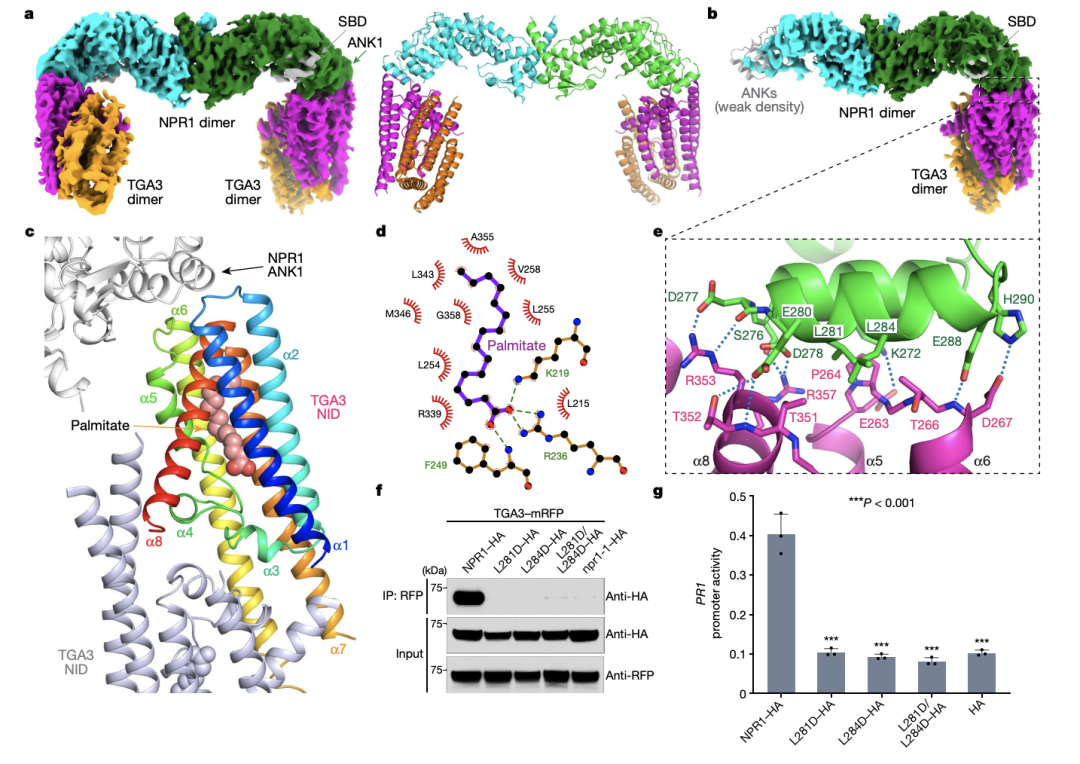
NPR1-TGA3 复合物的结构和功能
综上所述,该研究的结构解释了二十多年 NPR1 研究的数据。SBD 和 TGA转录因子之间缺乏直接相互作用表明,SBD-ANK 对接构象可以实现翻译后修饰,促进未知转录调节因子的募集。TGA32-NPR12 –TGA32的结构解析复合物及其组装中间体提高了 NPR1 重新编程防御转录组以响应广泛的生物和非生物胁迫的可能性,这不仅通过 TGA 同源二聚体的参与,而且还通过复合物中的异源转录激活因子、抑制因子和脂质代谢物的参与。
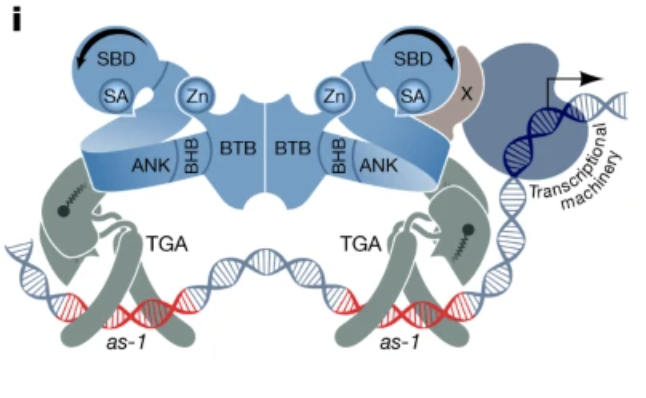
2. 2022年7月30日,Cell杂志发表了来自美国杜克大学董欣年(Xinnian Dong)团队揭示了分子模式激活的免疫反应(PTI)信号通路中一个全新的蛋白翻译起始模块(Module)——PABP/R-motif介导的非帽结构依赖的胁迫相关蛋白的翻译。这一发现为真核生物蛋白翻译重编程提供了不同于经典的eIF2a磷酸化通路的理论模型,对研究其他真核生物蛋白重编程具有普遍的借鉴意义。

真核生物的mRNA翻译起始(Translation initiation)是一个极其复杂的过程。在没有胁迫的条件下,绝大多数真核mRNA的翻译起始依赖于其位于5’端的m7G帽结构(Cap structure)。为了起始翻译,eIF2-GTP-Met-tRNAi三聚体与40S核糖体亚基进行组装形成43S前起始复合物(43S preinitiation complex, PIC),其中eIF2包含三个蛋白eIF2α、eIF2β和eIF2γ。43S PIC随后被eIF4F起始复合体招募到位于mRNA 5’端的m7G帽子结构启动对mRNA从5’端到3’端的扫描,直至遇到合适的起始密码子,其中eIF4F复合体包括 m7G帽结构结合蛋白eIF4E、支架蛋白eIF4G和解旋酶eIF4A。起始密码子的识别会招募60S核糖体亚基,形成80S起始复合体开始蛋白的合成。值得注意的是,与3’端poly(A)结合的PABP(Poly(A)-binding protein)可以促进43S PIC的招募过程。
在遭遇胁迫时,真核生物通常通过eIF2α磷酸化抑制经典的m7G帽结构依赖的翻译,同时选择性地翻译胁迫必须的调节蛋白(Stress regulators),从而实现体内蛋白翻译的重编程(Reprogramming)。然而,在植物的PTI信号通路中,通过敲除GCN2完全阻断eIF2α磷酸化并没有发现其对翻译重编程的显著影响,暗示了在植物的PTI信号通路中存在全新的蛋白翻译重编程机制。
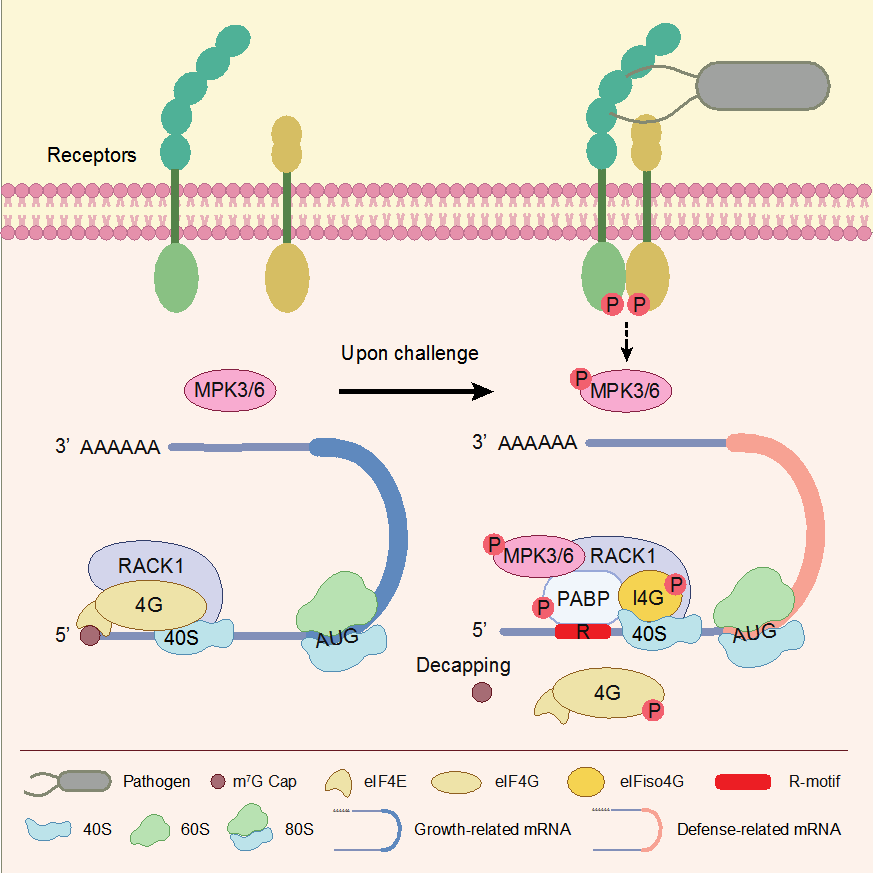
植物PTI信号通路中蛋白翻译重编程模式
王金龙等的研究发现,病原菌侵染可以促进DCP蛋白(Decapping protein)去除mRNA 5’端的m7G帽结构来抑制经典的帽结构依赖的蛋白翻译(Cap-dependent translation),而在5’端先导序列(Leader sequence)含有R-motif(Purine-rich element)的抗病相关mRNA,则可以利用R-motif作为m7G帽结构的代替者(Cap surrogate)——一个新式的胞内IRES(Internal ribosome entry site),结合PABP蛋白来选择性地启动自身的翻译。在正常生长条件下,不含有R-motif的生长相关的mRNA通过m7G帽结构依赖的方式进行翻译。当PTI信号被激活后,PABP会选择性地结合激活后的eIFiso4G(eIF4G异构体)促进含有R-motif的抗病相关mRNA的翻译。
值得注意的是,从经典的m7G帽结构依赖的蛋白翻译到R-motif介导的非帽结构依赖蛋白翻译的转变,是通过PTI信号通路中的关键激酶MPK3/6 来实现的。当PTI信号被接受后,MPK3/6会被激活,诱导mRNA去除5’端的帽子结构,并磷酸化eIF4G来抑制生长相关mRNA的翻译;同时磷酸化PABP增强其与R-motif之间的结合,激活eIFiso4G蛋白,促进含有R-motif的抗病相关mRNA的翻译。
本研究揭示了不同于经典的eIF2α磷酸化介导的蛋白重编程机制,同时因为R-motif同样广泛存在于果蝇、小鼠和人体的胁迫相关mRNA的5’端前导序列中,本研究发现的蛋白翻译起始调控机制可能同样广泛存在于其他真核生物体中。
相关论文信息:
https://doi.org/10.1016/j.cell.2022.06.037
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#植物#
47
#Cell#
70
#CEL#
33
#Nat#
29