香港城市大学周智航/杨梦苏揭示赖氨酸羟化酶促进癌细胞局限迁移和转移的分子机制
2023-02-06 iNature iNature 发表于上海
细胞外基质过度沉积和硬度增加是实体瘤的典型特征,如肝细胞癌和胰腺导管腺癌。这些条件为肿瘤细胞的迁移和转移创造了有限的空间。限制迁移的调控机制尚不清楚。
细胞外基质过度沉积和硬度增加是实体瘤的典型特征,如肝细胞癌(hepatocellular carcinoma,HCC)和胰腺导管腺癌(pancreatic ductal adenocarcinoma,PDAC)。这些条件为肿瘤细胞的迁移和转移创造了有限的空间。限制迁移的调控机制尚不清楚。
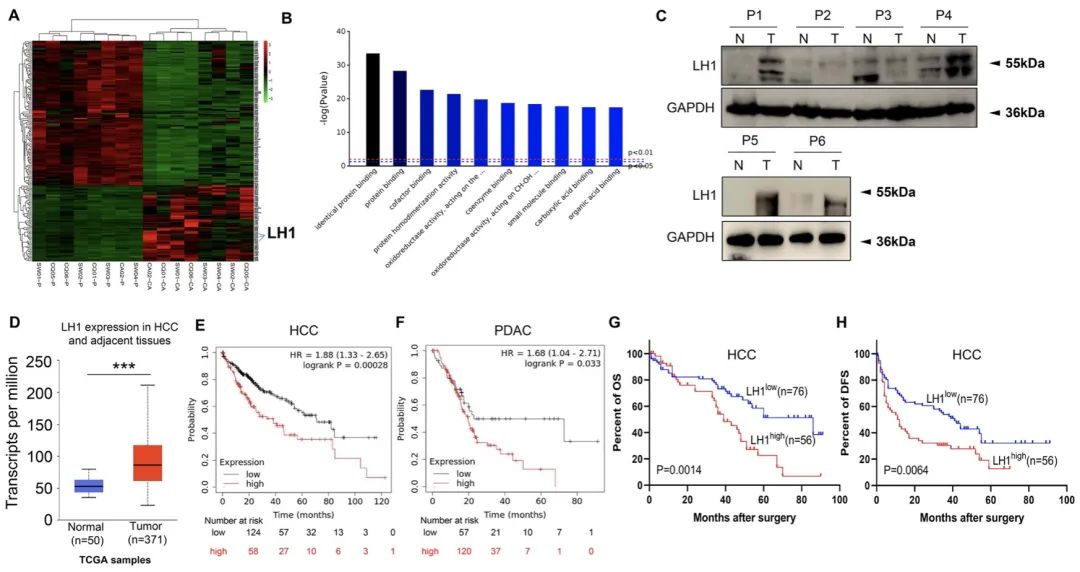
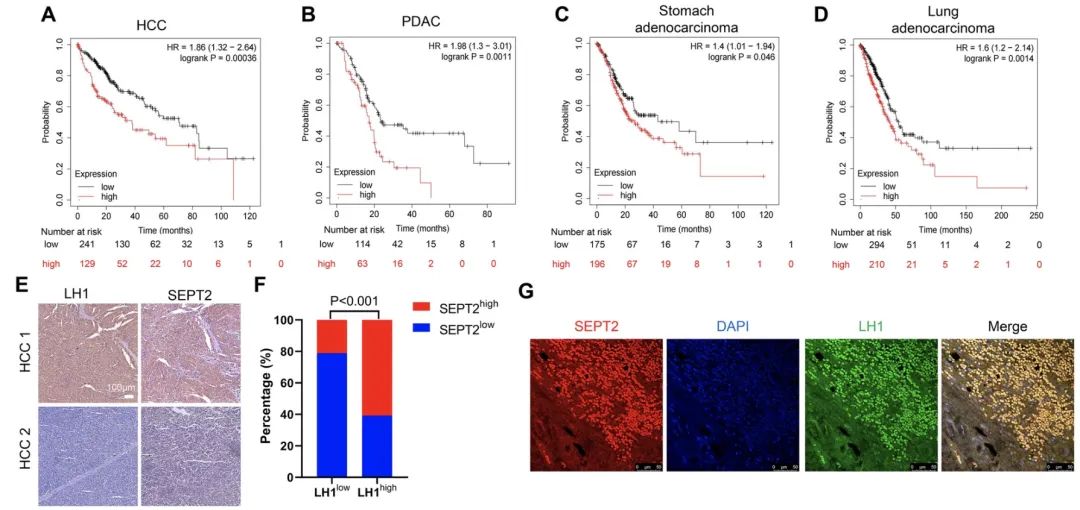
2023年1月31日,香港城市大学周智航与杨梦苏在Molecular Cancer杂志在线发表题为“Lysyl hydroxylase LH1 promotes confined migration and metastasis of cancer cells by stabilizing Septin2 to enhance actin network”的研究论文,该研究表明赖氨酸羟化酶1 (Lysyl hydroxylase 1,LH1)促进癌细胞在集体和单细胞水平上的受限迁移。此外,LH1增强了三维仿生模型中的细胞侵袭和更硬环境中的球体形成。LH1高表达与HCC和PDAC患者预后不良相关,同时也促进了体内转移。
机制上,LH1结合并稳定Septin2 (SEPT2)以增强肌动蛋白聚合,这取决于羟化酶结构域。最后,LH1和SEPT2均高表达的亚人群预后最差。总之,这项工作揭示了LH1在HCC和PDAC局限迁移转移中的新的分子机制,为肿瘤的诊断和治疗提供了新的策略。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







