慢性乙型肝炎相关肝癌风险预测模型全面总结
2021-08-04 雨露肝霖 健康界
晚期肝癌的预后通常较差,应积极监测肝癌的发生与发展,而在肝癌早期阶段进行更优化的治疗,有利于改善患者的预后,因此对慢乙肝患者进行肝癌风险预测,具有重要的意义。HBV感染最终发展为肝癌的危险因素很多,包
晚期肝癌的预后通常较差,应积极监测肝癌的发生与发展,而在肝癌早期阶段进行更优化的治疗,有利于改善患者的预后,因此对慢乙肝患者进行肝癌风险预测,具有重要的意义。HBV感染最终发展为肝癌的危险因素很多,包括高龄、男性、肝硬化、糖尿病、高HBV DNA水平、ALT升高、HBeAg阳性等,研究者们利用这些危险因素进行多因素整合,建立了多种适合不同慢乙肝人群的肝癌风险预测模型,有利于提高肝癌的早期诊断。以往曾系统归纳和总结了近几年来的乙型肝炎相关的肝癌风险预测模型,最近肝霖君整合相关资源,重新整理和归纳了慢性乙型肝炎相关肝癌风险预测模型,和大家分享。
在肝癌预测模型的临床应用中,我们发现针对不同人群,各模型的预测准确度是有差异的,特别是对于未治疗和核苷经治人群。由于核苷经治的慢乙肝人群数量大,近几年来陆续出现了多个针对核苷经治的慢乙肝患者的肝癌风险预测模型。因此我们按照这两类人群进行了模型分类,有利于临床中根据不同患者类型进行肝癌风险的评估,提升预测的准确度,造福更多患者。

01 未经治疗的人群
未经治疗的人群的大多数模型已在之前进行过具体的介绍,未介绍的几个模型我们更新在列表的后面。我们发现对于未经治疗的患者,预测因素一般较为广泛且复杂,既包含宿主因素,也包括病毒因素和肝纤维化/肝硬化等相关因素。为了临床上更方便应用,逐步开始探索简单易检测的预测模型。
2005年,第一个肝癌风险预测模型(IPM)发表,适合于所有慢性肝脏疾病。到2009年,第一个适用于慢乙肝患者的肝癌风险预测模型(GAG-HCC)出现,之后研究者利用REVAL-HBV队列研究了非肝硬化慢乙肝人群的肝癌风险模型(REACH-B),随后伴着肝硬度测量(LSM)技术的发展,可通过瞬时弹性检测技术来测定肝硬度值,因此肝脏硬度值开始被纳入肝癌风险预测模型中(LSM-HCC、mREACH-B)。随着抗病毒治疗的可及性增高,存在大量的接受过抗病毒治疗的慢乙肝人群,而以往的预测模型对这类人群的适用度并不高,因此开始陆续出现了合适接受抗病毒治疗的慢乙肝患者的肝癌风险预测模型(PAGE-B),并且在亚洲人群中进行推导(mPAGE-B),随后代谢疾病(如糖尿病)对慢乙肝患者的肝癌风险的影响开始被学者关注,并纳入近期的肝癌风险预测模型中(CAMD、REAL-B)。
相关评分模型在线使用:
D²AS评分模型(HCC risk estimated in the D²AS model,2017)
该评分模型利用971例HBV DNA升高(> 2000 IU/mL )且ALT正常或轻度升高(< 80 U/L)的韩国无肝硬化慢乙肝患者进行推导,中位随访4.5年,该模型包括年龄、性别和HBV DNA指标。该评分从507名患者的验证队列中得到验证,推导队列的D²AS评分在3年和5年的时间相关AUROC分别为0.895和0.884,验证队列中分别为0.889和0.876。推导队列和验证队列的拟合优度比较结果显示出D²AS的一致性(推导队列为0.861,验证队列为0.878),且显著优于REACH-B、年龄和ALT。

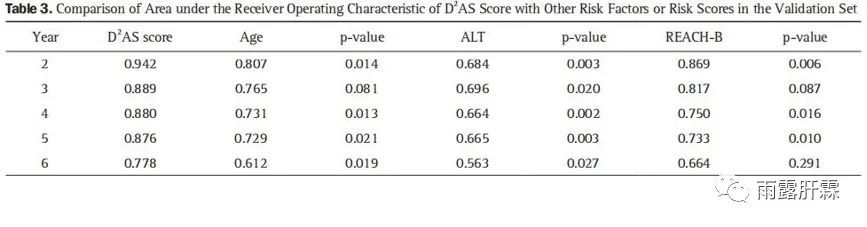
RWS-HCC评分模型(Real-world risk score for hepatocellular carcinoma,2016)
该研究为538名新加坡慢乙肝患者的真实世界研究,随访4.9年,用于预测慢乙肝患者在真实世界中发生肝癌的风险。评分指标包括年龄、性别、AFP和肝硬化。RWS-HCC评分中 ≥ 4.5分显示未来10年有显著HCC发生风险,AUROC为0.915,敏感度为88.1%,特异性为83.0%,准确度为83.4%。其中阴性预测值(NPV)为98.8%,表明其在鉴别低风险肝癌患者中的实用性。在REACH-B、GAG-HCC和CU-HCC队列的3353名受试者中进一步验证了该模型,AUROC分别为0.767、0.830和0.902。3个验证队列的准确率分别为88.2%、79.1%和90.6%,NPV维持在97.0%,97.9%和93.0%。
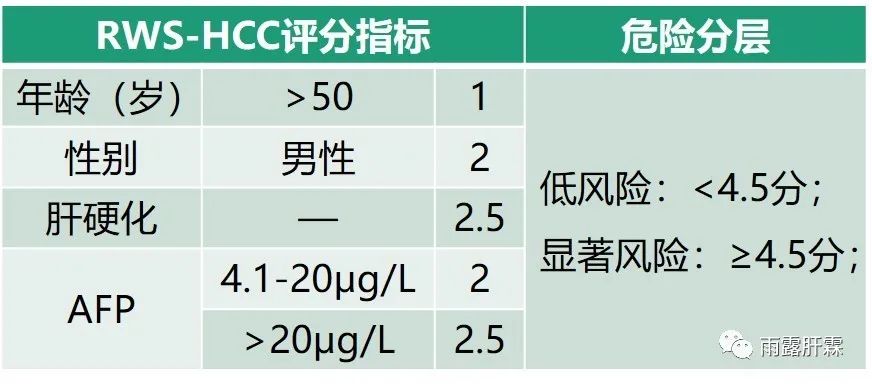
LSPS评分模型(Liver stiffness value x platelet count/ spleen diameter,2014)
该研究纳入227名韩国接受肝活检和肝硬度值检测的慢乙肝患者,中位随访61个月,18例患者发生HCC。其中HCC组的LS值、脾脏长度和血小板计数显著高于非HCC组(P均 < 0.05)。多因素分析,LSPS是HCC发生的独立预测因素(P < 0.001)。通过LSPS值将患者分为三组,LSPS < 1.1、1.1-2.5和 > 2.5组,LSPS值越高的患者HCC发生风险更高。相比其他非侵入性评分方式ASPRI、LS值、FIB-4和APRI等,LSPS预测5年HCC发生的AUROC值最高,为0.834。

02 接受NA治疗的人群
由于核苷治疗人群数量多,且有大量研究发现核苷长期治疗的慢乙肝患者肝癌风险虽然相比未治疗有所降低,但仍然处在较高水平。因此对这部分的人群的肝癌预测和监测变得尤为重要,近几年也出现了多个针对核苷经治人群的肝癌风险预测模型。由于核苷治疗主要是针对病毒的抑制作用,因此我们也发现对于核苷经治人群的肝癌预测模型中均无病毒因素。之前未介绍的模型我们将在表格后进行详细介绍。
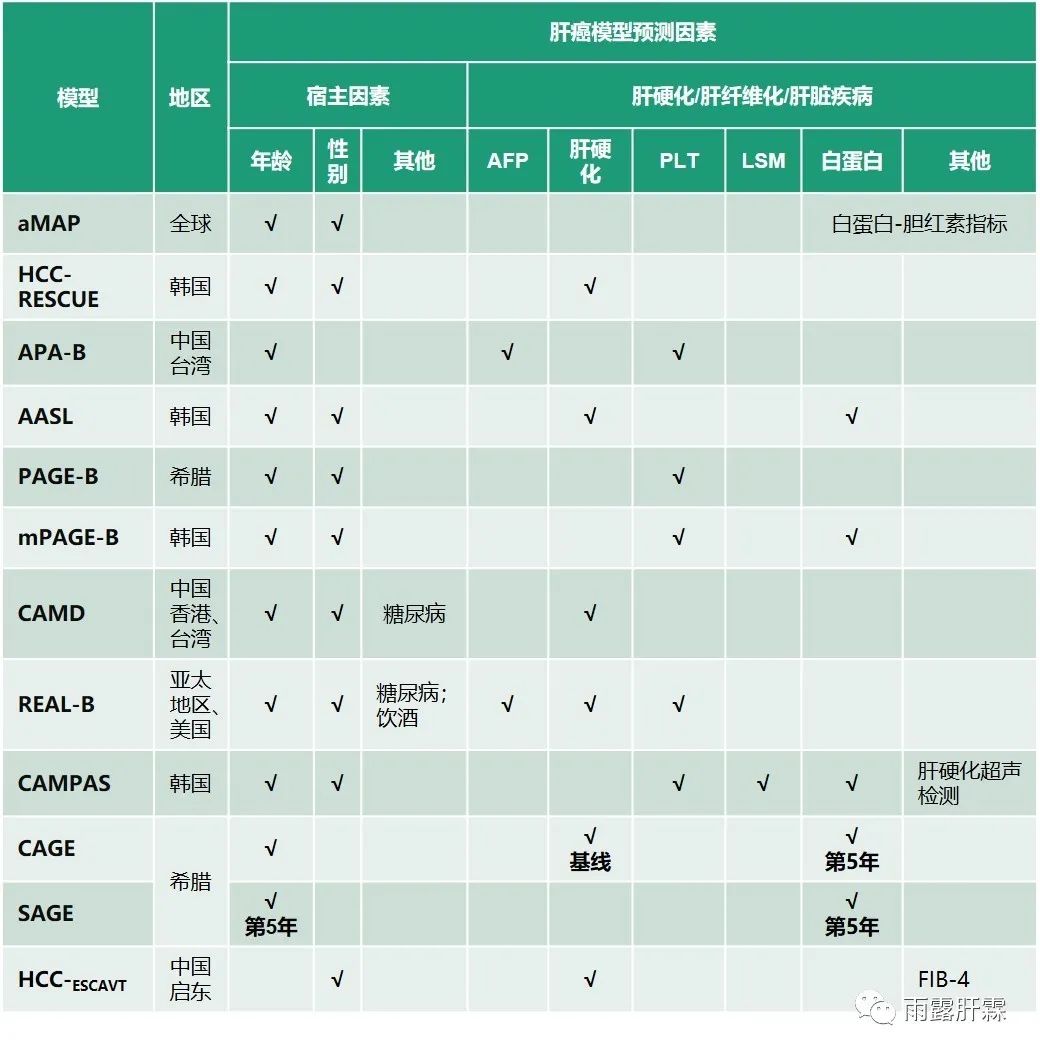
AASL-HCC评分模型(Age、Albumin、Sex、Liver cirrhosis,2019)
AASL-HCC评分模型以1242名ETV/TDF治疗的慢乙肝患者为研究对象,以944例患者为推导队列,随访51.3个月,基于多变量Cox比例风险模型建立而成。该模型以298例患者为验证队列,随访46.8个月,使用Harrells C-statistic进行验证。该模型以年龄、白蛋白、性别和肝硬化作为评分指标,分为低风险组≤ 5分,中等风险组6-19分和高风险组≥ 20分。该模型在推导队列和验证队列之间的3年、5年和总随访的C-statistic无显著性差异。与CU-HCC、GAG-HCC、REACH-B和PAGE-B模型相比,AASL-HCC评分模型预测10年HCC发生的准确性更高,AUROC为0.814。
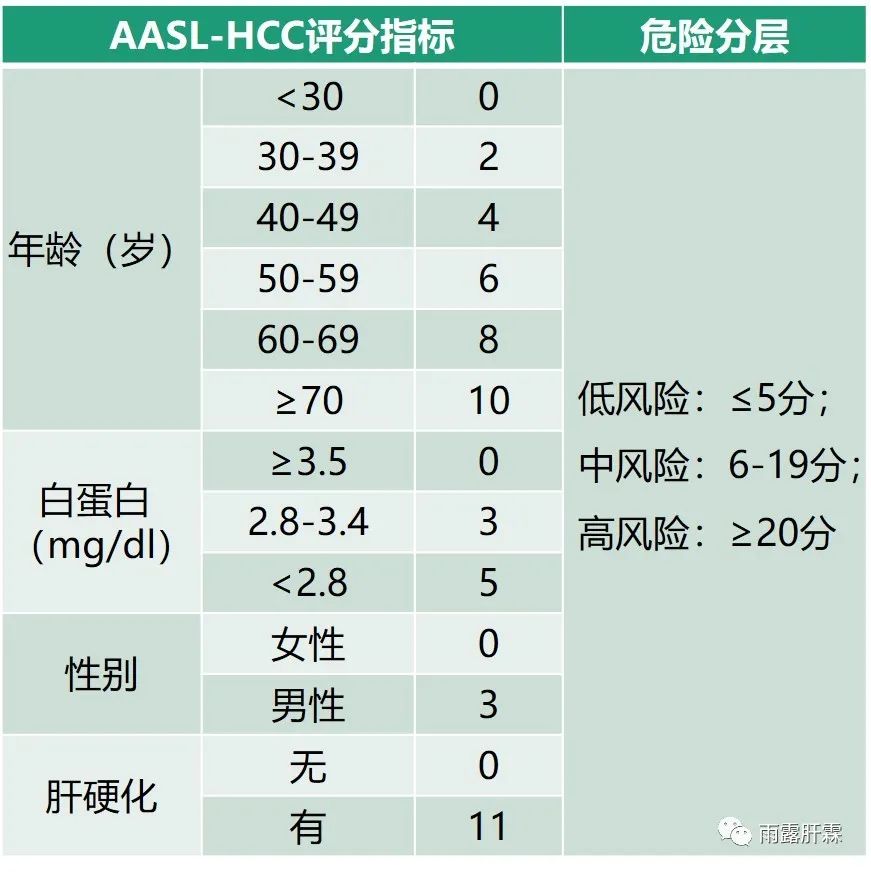
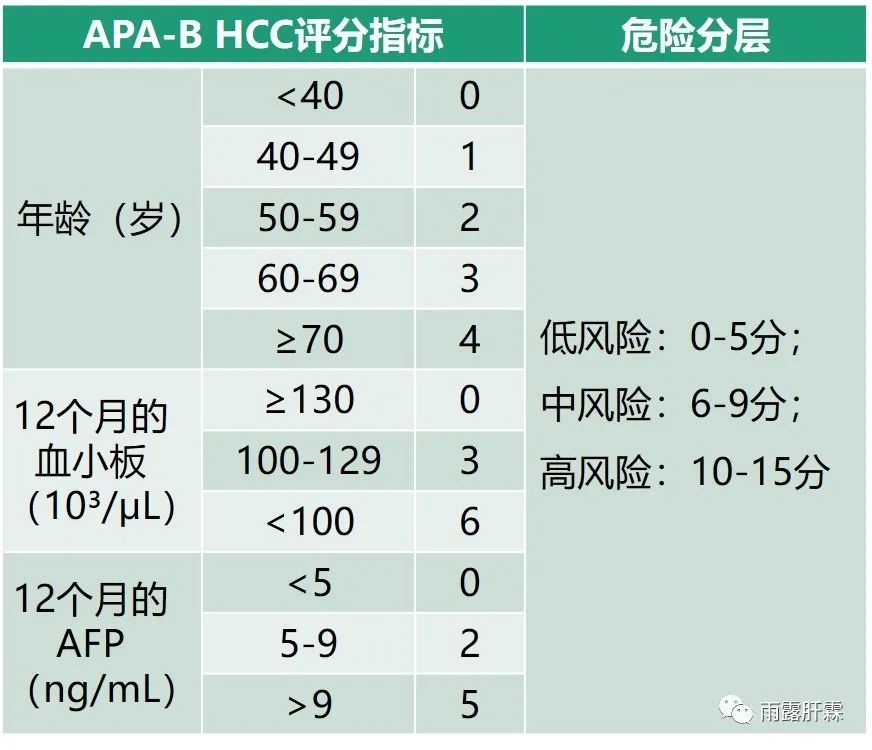
APA-B HCC评分模型(Age、PLT、AFP,2017)
共随访49.1个月,在883名韩国ETV治疗的初治慢乙肝患者的推导队列中进行多因素分析,发现年龄、血小板计数和治疗12个月的AFP水平是肝癌的独立预测因素,将这些预测因子的Cox比例风险回归系数转换成风险评分,建立APA-B评分模型,总风险评分范围为0-15。该模型将442名韩国ETV治疗的初治慢乙肝患者的验证组患者分为低(0-5分)、中(6-9)和高(10-15)风险组,其C-statistics为0.85。且分析发现该模型的C-statistics显著高于CU-HCC、REACH-B I、REACH-B II和PAGE-B模型。
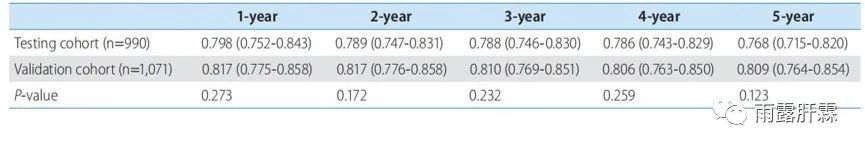
HCC-Rescue评分模型(HCC-Risk Estimating Score in CHB patients Under Entecavir,2017)
该研究前瞻性纳入2061例ETV治疗的初治慢乙肝患者,患者人群分为两组,990例的推导队列组,随访2.1年,和1061例的验证队列组,随访3.5年。推导队列组用于评估HCC发展的危险因素。分析结果将年龄、性别和肝硬化指标建立HCC-Rescue风险预测模型,该模型将患者分为低风险组≤65分,中等风险组65-84分,高风险组≥85分。该模型的推导队列和验证队列中时间相的预测1-5年肝癌发生风险的AUROC无显著性差异。

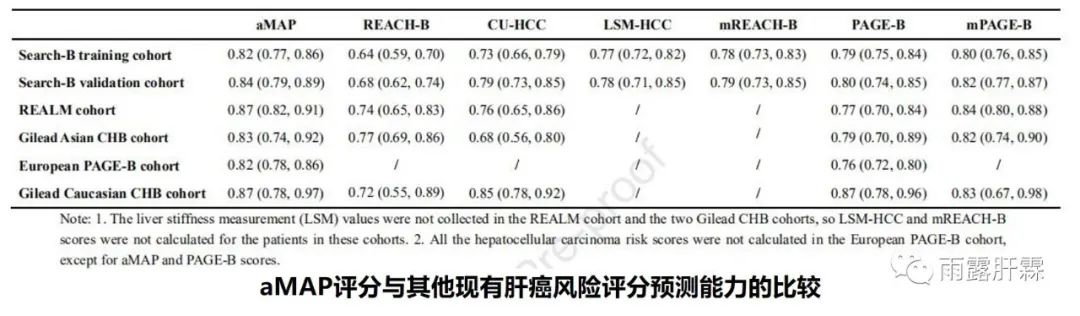
aMAP评分模型
(Age、Male gender、ALBI、PLT,2020)
该研究纳入全球11个前瞻性长期随访队列的17,374名的慢性肝病患者,包括13,088例NA经治慢乙肝(CHB)患者(10578例为亚洲人;2510例为白种人),3566例经治丙肝(HCV)感染患者和720例非病毒性肝病(NVH)患者。将患者分为1个推导队列(3688例亚洲CHB患者)和9个包括不同病因和种族的验证队列(包括3个CHB亚洲人队列、2个CHB白种人队列、3个HCV队列和1个NVH队列,共13686人)。其中aMAP评分模型指标包括年龄、性别、白蛋白-胆红素评分(ALBI)和血小板指标,在不同病因的肝炎患者和不同种族的肝炎患者中评估HCC风险均表现出色(C指数:0.82-0.87)。在慢乙肝相关推导队列中,aMAP评分的C指数 显著高于其他现有HBV相关HCC风险评分模型,如REACH-B、CU-HCC、LSM-HCC、mREACH-B、PAGE-B和mPAGE-B(P值均<0.05)。且在各种不同队列中,aMAP评分模型的预测能力也优于其他现有预测模型。
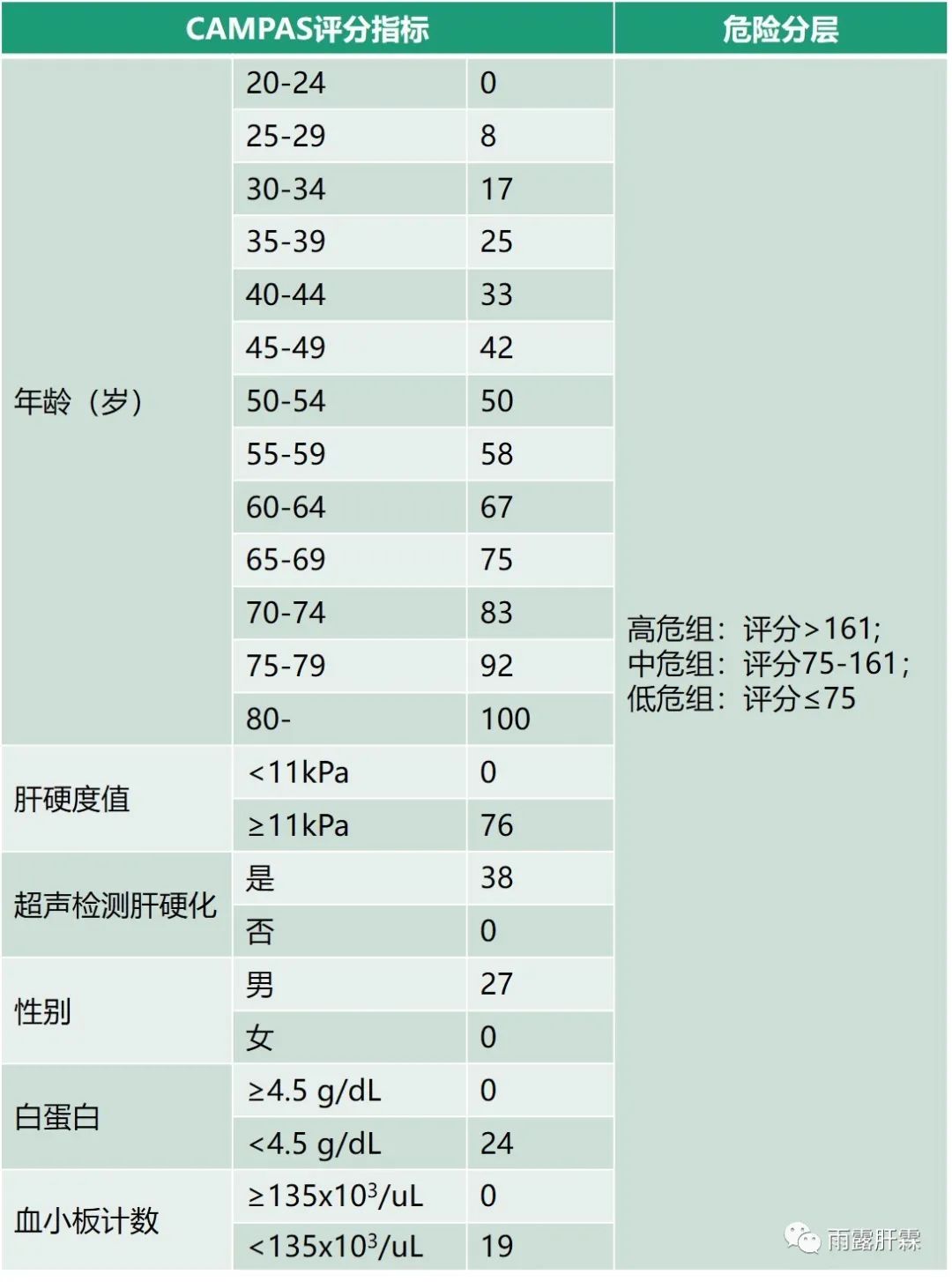
CAMPAS评分模型(Cirrhosis、Age、Male Sex、PLT、Albumin、Liver stiffness,2020)
该研究纳入接受非侵入性肝纤维化检测数据(例如瞬时弹性成像[TE])且NA治疗获得良好病毒学控制的1511例慢乙肝患者,随访期间,9.5%的患者发展为HCC。CAMPAS评分模型包括肝硬化的超声检查、年龄、男性、血小板计数、白蛋白和肝硬度。根据评分模型将患者分低危组(≤ 75)、中危组(75-161)和高危组(> 161),中危组和高危组的患者肝癌发生风险更高(P = 0.001)。韩国庆北国立大学医院纳入252例患者验证CAMPAS模型的效果,Harrell C-statistics为0.847(95%CI 0.744-0.929)。外部验证队列的校准图还显示了HCC发生的实际概率与CAMPAS模型计算的预测概率之间的极好的一致性。总体Harrell C-statistics显著高于mPAGE-B、PAGE-B和REACH-B(所有P值 < 0.001)。 但是,CAMPAS模型与mREACH-B之间没有显著性差异(P = 0.425)。
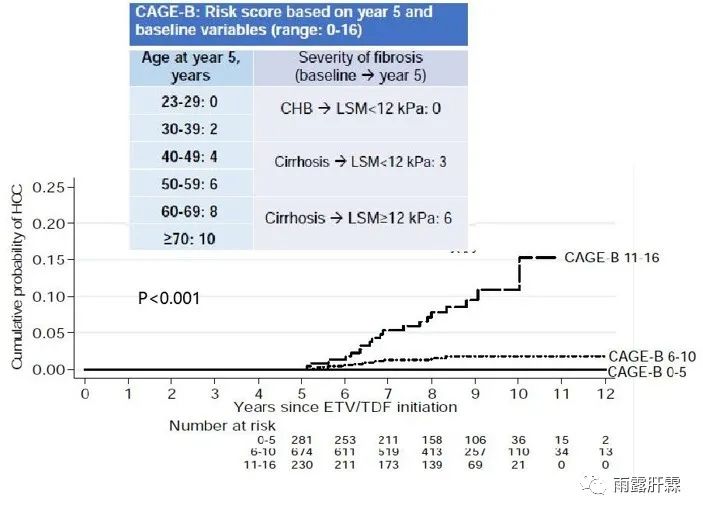
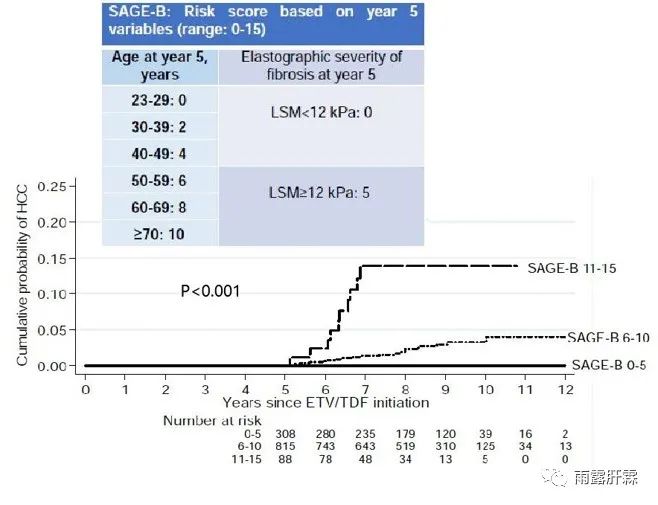
CAGE/SAGE评分模型(2020)
该研究分析PAGE-B队列中1951例成年白人慢乙肝B患者,纳入其中1427例患者(NA治疗下接受了5年以上的随访,且在治疗5年内无肝癌发生)。从治疗开始中位随访时间为8.4年。多因素分析发现,年龄较大、基线肝硬化及第5年LSM ≥ 12 kPa与5-12年的肝癌风险增加独立相关。基于此建立两项HCC评分模型。CAGE-B评分模型包括基线肝硬化、第5年LSM和年龄指标。其中,低(0-5)、中(6-10)和高(11-16)CAGE-B评分的患者的12年累积HCC发生率分别为0%、1.8%和15.4%。SAGE-B评分模型包括第5年时的年龄和LSM指标。其中,SAGE-B得分低(0-5),中(6-10)和高(11-16)的患者的12年累积HCC发生率分别为0%、4.0%和13.8%。
HCC-ESCAVT评分模型(2020)
2006-2016年期间,纳入769例患者作为推导队列,1061例患者作为验证队列,所有患者经ETV/TDF治疗获得HBeAg清除。对推导队列进行多因素分析,发现男性、肝硬化和FIB-4指标是HCC发生的独立危险因素(均P < 0.05),基于此建立了HCC-ESCAVT 评分模型,预测3年、5年和10年HCC发生风险的AUC分别为0.791、0.771和0.790,且在验证队列中表现相似。该模型将患者分为低风险组(0-1分),中等风险组(2-4分)和高风险组(5分)。该模型的预测HCC发生的准确性的AUC高于GAG-HCC模型(P < 0.05),与CU-HCC、PAGE-B和mPAGE-B模型相似(均P < 0.05)。

肝霖君有话说
迄今为止,国内外已有很多研究模型来预测慢乙肝相关肝癌发生风险。肝霖君重新整理了更完整和更新的肝癌预测模型供大家参考,希望随着肝癌模型的不断改进和完善,广泛的运用于临床工作中,指导越来越多的未治疗和接受核苷治疗的慢乙肝患者进行肝癌的监测和预防,提升对肝癌的早期诊断能力,及时对慢乙肝相关肝癌高风险人群给予干预治疗,最终有效降低慢乙肝患者肝癌发生风险。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#癌风险#
45
#乙型肝炎#
38
#预测模型#
37
#慢性乙型肝炎#
55
#风险预测#
62
#风险预测模型#
43
肝癌,接下来就要细分了,对于体质好的病人,能否将PD-1类+抗血管新生+放疗等相结合,甚至有必要用TACE进行减负
63
梅斯里提供了很多疾病的模型计算公式,赞一个!
44