ASCO 前沿:CAR-T疗法治疗复发/难治性淋巴瘤重大突破汇总
2020-06-03 MedSci原创 MedSci原创
ASCO 前沿,CAR-T疗法治疗复发/难治性淋巴瘤重大突破汇总。
ASCO 前沿 | CAR-T疗法治疗复发/难治性淋巴瘤重大突破汇总

一、CD19/22双重靶向的CAR-T细胞疗法AUTO3与Keytruda联合,治疗复发/难治性弥漫性大B细胞淋巴瘤(r/r,DLBCL)患者完全缓解率达55%(摘要号8001)
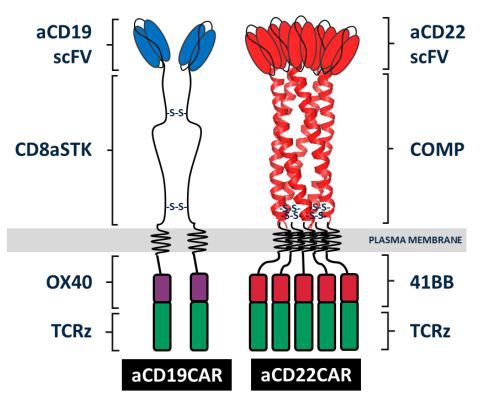
二、同种异体CAR-T疗法ALLO-501和ALLO-647联合治疗复发/难治性大B细胞或滤泡性淋巴瘤(R/R,LBCL/FL)的首次人体数据,客观响应率达78%(摘要号8002)
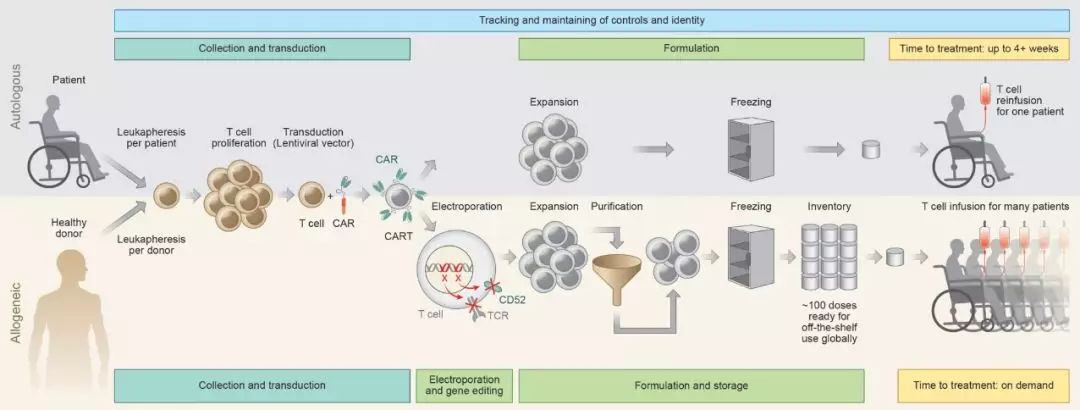
三、Yescarta治疗复发/难治性惰性非霍奇金淋巴瘤(R/R,iNHL)患者的II期研究,完全缓解率达79%(摘要号8008)

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#CAR-#
40
#ASC#
43
#难治性#
35