Nature:强大AD相关基因,让大脑漏了!科学家研究了245名志愿者的大脑,首次发现APOE4引起的血脑屏障破损的机制
2020-05-24 奇点糕 奇点网
APOE4是与阿尔茨海默病关系最密切的基因。
APOE4是与阿尔茨海默病关系最密切的基因。
近日,南加州大学Berislav V. Zlokovic教授领衔的研究团队,将二者的关系拉的更近了。
Zlokovic团队研究了245名志愿者的大脑,首次揭示APOE4导致大脑血脑屏障(BBB)破损的机制。他们还发现,这种破损会使有毒物质渗透到大脑负责记忆和其他认知功能的区域,更重要的是,APOE4导致的血脑屏障破损与β样淀粉蛋白和tau蛋白无关,独立对认知产生了影响。
这项重要的研究成果发表在顶级期刊《自然》杂志上,让我们对阿尔茨海默病有了新的认知,也为科学家提供了新的治疗靶点。

▲ 论文首页截图
我们已经有半年的时间没写过阿尔茨海默病的研究进展了。这主要是因为这个疾病太难了。
就拿APOE4来说,科学家好早就发现它与阿尔茨海默病有关,与常见的APOE3相比,哪怕只携带单拷贝的APOE4,就与阿尔茨海默病风险增加3倍有关;如果是纯合的APOE4,那患病风险直接飙升15倍。
遗憾的是,这么多年以来,还没人确切知道APOE4究竟是如何导致阿尔茨海默病的。

▲ 血脑屏障(图源:见水印)
提起阿尔茨海默病,我们最先想到的应该是β淀粉样蛋白和tau蛋白,不过靶向这两个蛋白的药物接连的失败,以及从其他角度展开的越来越多的研究成果,都表明一个问题:β淀粉样蛋白和tau蛋白不是阿尔茨海默病的全部。
在其他方面的研究成果中,血脑屏障的改变逐渐引起科学家的注意。
有些研究表明,血脑屏障的变化是阿尔茨海默病的早期标志物,甚至有研究发现,血脑屏障的损坏程度与阿尔茨海默病的严重程度密切相关。
遗憾的是,血脑屏障受损的确切原因目前也是未知的。不过也有越来越多的研究发现,APOE4与血脑屏障受损之间有关系。
作为“血脑屏障受损导致认知障碍和痴呆症”假说的先驱,Zlokovic打算在人体内探索一下APOE4与血脑屏障以及阿尔茨海默病之间的关系,把扑朔迷离的相关性关系,变成因果关系。

▲ Berislav V. Zlokovic(图源:南加州大学)
为此,Zlokovic团队招募了245名志愿者,通过动态对比增强磁共振成像(DCE-MRI)技术,分析了所有参与者血脑屏障的通透性。
他们发现,与认知正常的APOE3纯合志愿者(ε3/ε3)相比,在认知正常的APOE4携带者(ε3/ε4或ε4/ε4)体内,海马体(HC)和海马旁回(PHG)的血脑屏障受损程度增加。而且,这种增加与脑脊液(CSF)中β淀粉样蛋白和磷酸化tau蛋白的差异无关。
相较之下,即使是具有认知障碍的APOE3携带者,海马体和海马旁回的血脑屏障也没有太大的变化。
他们还观察到一个现象,APOE4携带者的海马体和海马旁回的体积,也会随着认知障碍而缩小,但是APOE3携带者没有表现出这种变化。
即使在控制年龄、性别、文化程度,脑脊液中β淀粉样蛋白和磷酸化tau蛋白水平,以及海马体和海马旁回的体积,这些混杂因素之后,APOE4携带者的海马体和海马旁回血脑屏障的受损,依旧与认知障碍高度相关;但是在APOE3纯合子中没有发现这种相关性。
他们还有个发现是血脑屏障受损先于脑萎缩,并且与全身性血管危险因素无关。
由于β淀粉样蛋白和tau蛋白也与血管异常和血脑屏障受损有关,研究人员要证明APOE4与血脑屏障受损之间存在独立关系,就得与β淀粉样蛋白和tau蛋白撇清关系。
为了搞清楚这个问题,Zlokovic团队基于正电子发射断层扫描(PET)研究了志愿者中的170人。最终的数据表明,APOE4携带者海马体和海马旁回血脑屏障的受损,与β淀粉样蛋白和tau蛋白这两个阿尔茨海默病风险因素无关。
与此同时,他们还发现,APOE4携带者的血脑屏障破坏,始于负责记忆编码和其他认知功能的内侧颞叶。
基于以上研究,研究人员基本可以确定,APOE4与血脑屏障受损与认知障碍之间是一条独立的线路,不受其他因素(尤其是β淀粉样蛋白和tau蛋白)的影响。
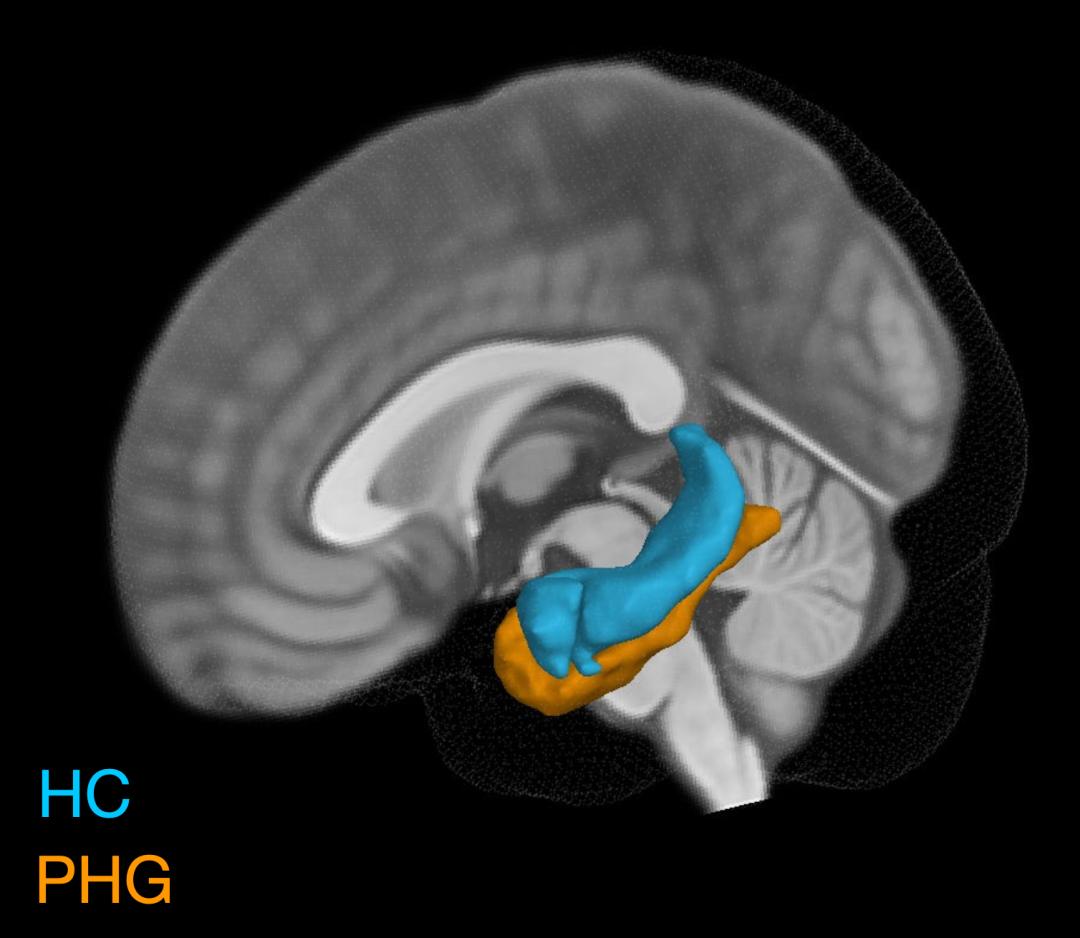
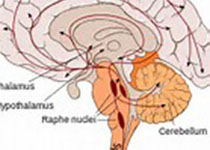
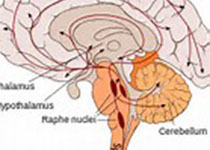
▲ 海马体(HC)和海马旁回(PHG)
那么APOE4究竟是如何导致血脑屏障受损的呢?
Zlokovic团队深入分析发现,APOE4携带者的脑脊液中可溶性血小板源性生长因子受体-β(sPDGFRβ)的水平升高,这与海马体和海马旁回的血脑屏障通透性增加相关。
而之前有研究表明,sPDGFRβ水平的升高,意味着脑毛细血管周细胞损伤与血脑屏障受损和认知障碍有关[9]。而这个过程又与促炎性亲环蛋白A-基质金属蛋白酶9(CypA–MMP9)途径有关。
基于此,研究人员将关注点放在了CypA-MMP9途径上。
研究人员分析志愿者的脑脊液发现,与APOE3纯合志愿者相比,APOE4携带者脑脊液中的CypA和MMP9水平均升高。基于人诱导多能干细胞的研究,证实了在人体内的发现。

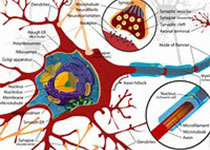
▲ APOE4导致血脑屏障受损的分子机制
在结合之前的小鼠研究,研究人员认为,APOE4激活了CypA-MMP9途径,这可能加速了血脑屏障的分解,最终导致神经元和突触功能受损。
由于之前小鼠的研究还发现,在APOE4小鼠体内阻断CypA-MMP9途径,可以恢复血脑屏障的完整性。
因此,CypA抑制剂在APOE4携带者体内可能也有类似的效果。这或许能改善脑血管完整性,并减少相关的神经元和突触缺陷,从而减缓认知障碍的进展。
实际上,此类药物已经用于治疗非神经性疾病。期待研究阿尔茨海默病的科学家做个回顾性分析,看看此类药物的使用是否与认知障碍之间存在相关性。
总的来说,这个研究揭示了APOE4导致血脑屏障破损的机制,以及确定了这种破损与认知障碍之间的关系。不过,APOE4诱发的血脑屏障破损究竟是如何导致阿尔茨海默病的,还需要更深入的研究,以揭示背后的分子机制。
原始出处:Montagne A, Nation D A, Sagare A P, et al. APOE4 leads to blood–brain barrier dysfunction predicting cognitive decline[J]. Nature, 2020: 1-6.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#志愿者#
42
#相关基因#
36
#Nat#
52
#45名志愿者#
47
#45名志愿者#
36
#血脑屏障#
40
#APOE4#
34
#APOE#
29
机制研究离临床仍然有距离,不过与临床结合思考,仍然有帮助的,不能仅仅是纯临床思维,转化思维同样重要
52
学习
80