BMJ: 期刊文章和临床试验注册中心报告漏报主要危害数据
2014-11-03 MedSci MedSci原创
为了测定临床试验方案、临床研究报告和主要的公开资源(期刊文章和试验注册)之间的数据在疗效和重大危害方面是否有矛盾的地方,以及临床研究报告本身是否矛盾,采用度洛西汀治疗重度抑郁症的研究作为研究对象。研究者从不同数据来源提取主要疗效分析和主要危害的数据并进行比较。9个随机的度洛西汀安慰剂对照试验(共2878个病人)用于重度抑郁症提交给欧盟药品管理局(EMA)审批。研究者于2011年5月从EMA获得包含
为了测定临床试验方案、临床研究报告和主要的公开资源(期刊文章和试验注册)之间的数据在疗效和重大危害方面是否有矛盾的地方,以及临床研究报告本身是否矛盾,采用度洛西汀治疗重度抑郁症的研究作为研究对象。
研究者从不同数据来源提取主要疗效分析和主要危害的数据并进行比较。9个随机的度洛西汀安慰剂对照试验(共2878个病人)用于重度抑郁症提交给欧盟药品管理局(EMA)审批。
研究者于2011年5月从EMA获得包含试验方案附件的临床研究报告(共13729页)。期刊文章通过相关文献数据库以及联系发表者-礼来制药得到证实。临床试验结果从Clinicaltrials.gov网站和厂商的在线临床试验注册中心搜索而得。
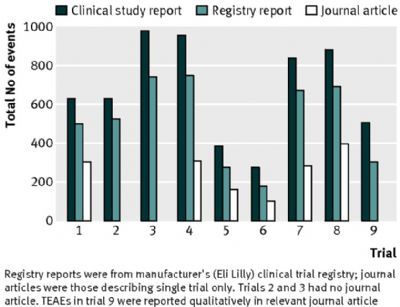
临床研究报告全面的描述了主要的疗效分析和主要危害(死亡数(包括自杀),企图自杀,严重不良事件和由于不良事件导致中止)。试验方案和临床研究报告之间以及临床研究报告自身在主要疗效分析人数方面存在小的矛盾。此外,研究者还发现在研究报告中关于7个严重不良事件和8个不良事件导致的中止的报告数据存在矛盾信息但没有明显的偏见。在每个试验中,在期刊文章和礼来临床试验注册中心报告中分别有平均406(177-645)和166(100-241)个治疗的紧急不良事件(用药后出现不良事件或恶化)没有报道。
结论:临床研究报告中有大量关于主要危害的数据没有出现在期刊文章和试验注册中心报告中。在试验方案和临床研究报告之间存在矛盾,临床研究报告本身也有矛盾。临床研究报告应作为药物的系统评价的数据来源,但需要和试验方案及自身进行检查,确保其准确性和一致性。
原位出处
Emma Maund, Britta Tendal, Asbjrn Hróbjartsson, Karsten Juhl Jrgensen, Andreas Lundh, Jeppe Schroll, Peter C Gtzsche. Benefits and harms in clinical trials of duloxetine for treatment of major depressive disorder: comparison of clinical study reports, trial registries, and publications. BMJ. 2014 Jun 4;348:g3510. doi: 10.1136/bmj.g3510.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#BMJ#
29
#注册#
39