Lancet Oncol:Ivosidenib显著改善晚期mIDH1胆管癌患者的生存率
2021-01-16 MedSci原创 MedSci原创
Tibsovo(Ivosidenib)艾伏尼布(AG-120) , 是靶向异柠檬酸脱氢酶1(IDH1)突变的口服、强效的抑制剂。而IDH1突变在多种肿瘤中均有发生。2018年7月20日获FDA批准上市
Tibsovo(Ivosidenib)艾伏尼布(AG-120) , 是靶向异柠檬酸脱氢酶1(IDH1)突变的口服、强效的抑制剂。而IDH1突变在多种肿瘤中均有发生。2018年7月20日获FDA批准上市,由Agios Pharmaceuticals上市销售,商品名为Tibsovo,被批准用于治疗患有复发性或难治性急性骨髓性白血病(R/R AML)的成人患者,成为首个获得FDA批准治疗IDH1突变的R/R AML的药物。在中国大陆授权基石药业进行推广。
2020年05月13日 《柳叶刀·肿瘤学》(The Lancet Oncology)发布论文Ivosidenib (AG-120)在治疗IDH-1突变的化疗后进展的胆管癌的lll期临床试验ClarlDHy中获得的积极结果,ivosidenib显著提高患者的无进展生存期(PFS)2.7个月,延长OS至10.8个月,降低63%疾病进展或死亡风险。此前结果在2019年ESMO上也有部分公布,见:2019年ESMO:Ivosidenib显著改善晚期mIDH1胆管癌患者的生存率
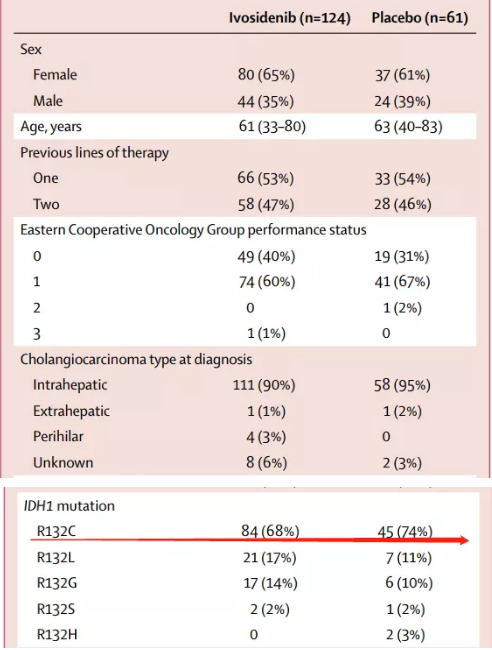
ClarlDHy试验是一多中心、随机、双盲、与安慰剂对照的多中心研究。胆管癌患者入组情况:胆管癌患者曾接受过1-2次全身性治疗;有185名胆管癌患者处于疾病继续进展期,携带IDH1基因突变;其中70%的胆管癌患者表现为R132C,171名(92%)胆管癌患者同时患有转移性疾病,86名(46%)胆管癌患者曾接受过两种先前的治疗。
胆管癌患者临床用药:按2:1的比例随机分为ivosidenib组(124)和安慰剂组(61)。ivosidenib组的胆管癌患者患者每天口服500 mg ivosidenib;安慰剂治疗组的胆管癌患者每天口服安慰剂。
该试验的主要研究终点为无进展生存期(PFS),次要研究终点为总生存期(OS)、客观反应率(ORR)、反应持续时间和反应时间(由研究者和研究中心评估);无进展生存期(由研究者审查);药代动力学和药效学。
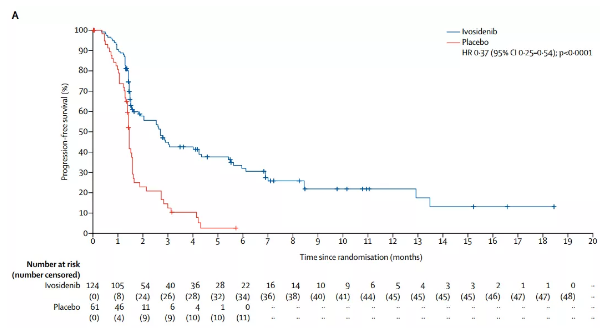
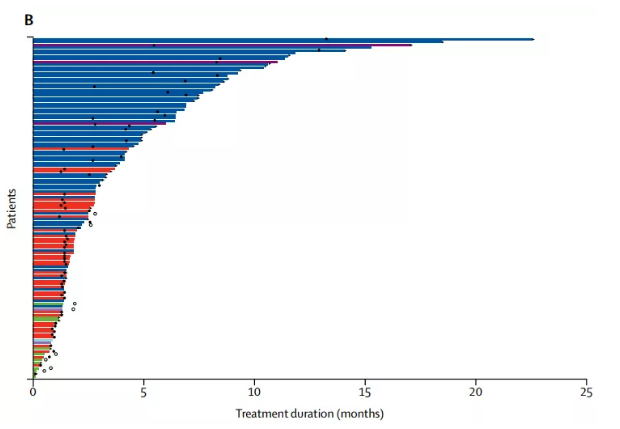
主要终点PFS方面,ivosidenib组:安慰剂组分别为2.7个月:1.4个月(HR=0.37,95% CI:0.25-0.54,p<0.001)。Tibsovo组胆管癌患者32%的6个月的无进展生存率,22%的12个月无进展生存率。2.7个月的无进展生存率降低了胆管癌患者63%的死亡风险。对一线治疗以上的胆管癌患者而言,令人欣慰。
试验结果(Tibsovo组VS安慰剂组):
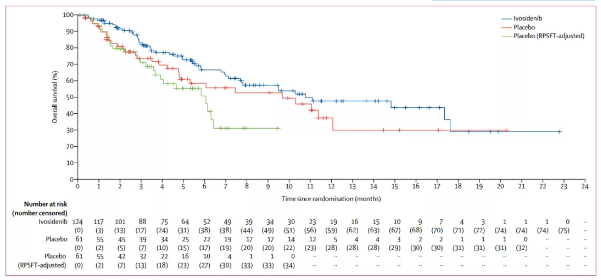
中位总生存期OS方面,ivosidenib组:安慰剂组分别为10.8个月 : 9.7个月(HR=0.69,95% CI:0.44-1.10, p=0.06)。
ivosidenib组与安慰剂组的数据相差不大,是因为61名安慰剂组的胆管癌患者中后期有35名患者口服ivosidenib治疗,因此安慰剂组显示的OS偏高。如果假设安慰剂组中的部分患者没有换为接受Tibsovo治疗,模型分析显示安慰剂组的中位OS只有6个月(HR=0.46,95% CI:0.28-0.75,p<0.001)。6个月的OS为67%,12个月的OS为48%。
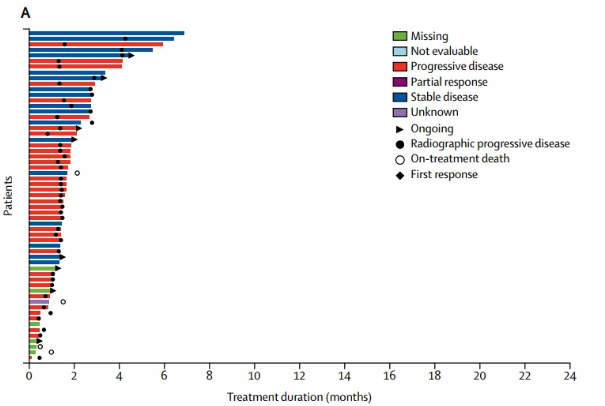
其它终点:
- 疾病控制率:53% vs 28%。
- ORR:2% vs 0%,不要看这个数据较低,而是因为其作用机制与索拉非尼治疗晚期肝癌有些相似,它通过阻止肿瘤进展从而使患者生存获益(抑制肿瘤细胞增殖,让患者达到基本稳定的状态),这也很好的解释了该药的DCR并不低的原因。
- 中位持续时间:2.6个月(IQR 1.4–6.0) vs 1 6个月(1.1–2.7)
-
- 3级及以上不良事件发生率:30% vs 22%。常见不良反应主要是恶心、腹泻、乏力、咳嗽等,心电图上的 QT 间期延长似乎是比较特异的不良反应。在病人报告的生活质量方面,治疗组更优。这些胆管癌患者在接受干预后1个周期左右生活质量就出现了明显下降,而治疗组患者的生活质量下降幅度更小一些。
目前NCCN指南已更新,将Ivosidenib纳入mIDH1胆管癌患者的二线治疗。
原始出处:
Abou-Alfa, G. K. et al. Ivosidenib in IDH1-mutant, chemotherapy-refractory cholangiocarcinoma (ClarIDHy): a multicentre, randomised, double-blind, placebo-controlled, phase 3 study. Lancet Oncol. (2020) doi:10.1016/S1470-2045(20)30157-1.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#胆管癌#
80
#Oncol#
31
#Ivosidenib#
28
#Lancet#
30
#IDH1#
44
#生存率#
0
#胆管#
26
学习了
67
顶刊就是不一样,质量很高,内容精彩!学到很多
36
谢谢梅斯分享这么多精彩信息
41