Lancet oncol:派姆单抗联合西妥昔单抗治疗复发性/转移性HNSCC的疗效和安全性
2021-05-13 Nebula MedSci原创
派姆单抗联合西妥昔单抗在复发性或转移性头颈部鳞状细胞癌患者中展现出了令人期待的临床活性,值得进一步研究
派姆单抗(PD-1抑制剂)和西妥昔单抗(EGFR抑制剂)作为单药和联合细胞毒性化疗用于复发或转移性头颈部鳞状细胞癌(HNSCC)均展现出治疗活性。鉴于每种药物的单药活性和独特的作用机制,Assuntina等旨在评估PD-1阻断联合EGFR抑制用于复发性或转移性HNSCC 抗肿瘤活性。
这是一项在USA的4个学术中心开展的开放标签的非随机的多臂的2期试验,招募了年满18岁的对铂耐受的或不适用铂类的复发性或转移性HNSCC患者,且要求既往未接受过免疫或EGFR抑制治疗。所有受试者接受派姆单抗(200 mg/3周,静滴)联合西妥昔单抗(起始剂量 400 mg/m2,后改为250 mg/m2·周),21天/疗程。主要终点是总缓解率。
最佳缓解情况
2017年3月22日-2019年7月16日,队列1共招募了33位受试患者。这33位受试患者都至少接受了一剂派姆单抗。中位随访持续时间为7.3个月(范围 3.9-10.9个月)。第6个月时,总缓解率为45%(95%CI 28-62),有15位患者获得了部分缓解。
无进展生存期和总生存期
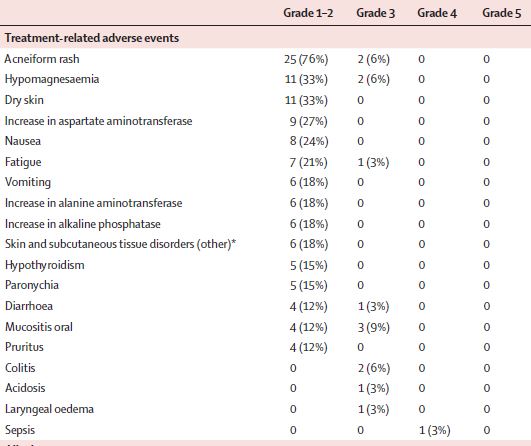
最常见的3-4级治疗相关不良反应事件有口腔粘膜炎(9%,3/33),5位(15%)患者发生了严重的治疗相关的不良反应事件。无治疗相关死亡事件发生。
治疗相关不良反应事件
总而言之,派姆单抗联合西妥昔单抗在复发性或转移性头颈部鳞状细胞癌患者中展现出了令人期待的临床活性,值得进一步研究。
原始出处:
Assuntina G Sacco, et al. Pembrolizumab plus cetuximab in patients with recurrent or metastatic head and neck squamous cell carcinoma: an open-label, multi-arm, non-randomised, multicentre, phase 2 trial. The Lancet Oncology. May 11, 2021. https://doi.org/10.1016/S1470-2045(21)00136-4
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#Oncol#
35
#西妥昔#
35
#Lancet#
27
#疗效和安全性#
28
#复发性#
24
#SCC#
30
#派姆单抗#
48
#转移性#
34
#HNSCC#
31
学习了,谢谢分享
54