印度监管机构:批准Favipiravir抗病毒片剂治疗COVID-19的临床试验
2020-05-01 Allan MedSci原创
制药公司Glenmark今日宣布,它已获得印度监管机构(DCGI)的批准,可开展Favipiravir抗病毒片剂治疗COVID-19患者的临床试验。
制药公司Glenmark今日宣布,它已获得印度监管机构(DCGI)的批准,可开展Favipiravir抗病毒片剂治疗COVID-19患者的临床试验。该产品是日本Fujifilm公司Avigan®的通用版本。Favipiravir已显示出抗流感病毒的活性,并已在日本被批准用于治疗新型流感病毒感染。在过去几个月中,在COVID-19爆发后,已经在中国、日本和美国开展了Favipiravir治疗COVID-19的多项临床试验。
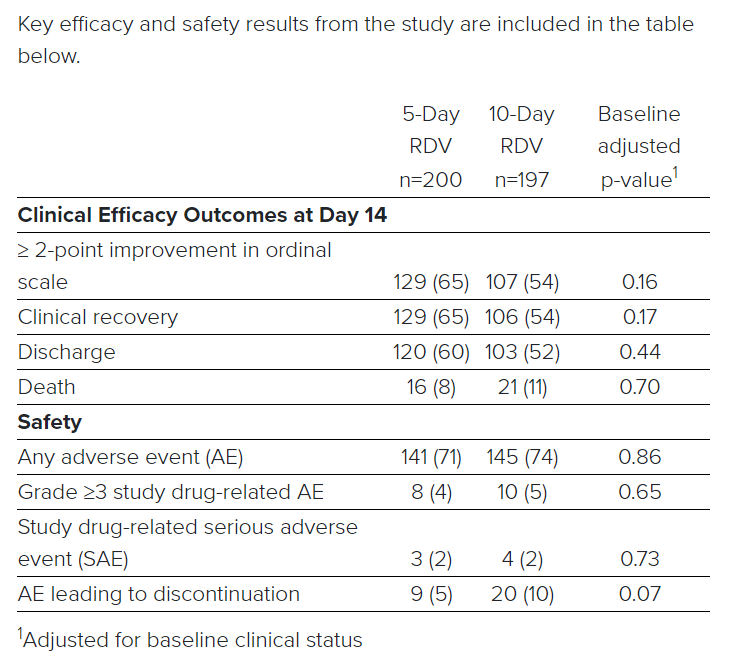
截止到目前,Glenmark是印度第一家获得监管机构批准开展COVID-19临床试验的制药公司。根据批准的临床试验方案,150例轻度至中度COVID-19患者将按1:1的比例随机分组,分为Favipiravir组和标准治疗组。治疗持续时间最长为14天,而随机分组后的总研究持续时间最长为28天。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#VIP#
36
#Favipiravir#
20
#抗病毒#
20
#监管#
23