Development:DNA甲基化影响造血干祖细胞产生的新机制
2022-05-16 国家血液系统疾病临床医学中心 网络
这一发现丰富了我们对体内HSPC产生机制的认识,为体外诱导获得可移植的造血干祖细胞提供新的思路。
在脊椎动物胚胎造血发育过程中,造血干祖细胞(hematopoietic stem and progenitor cells,HSPCs)由生血内皮细胞(hemogenic endothelial cells,HECs)通过内皮-造血转化(Endothelial-to-hematopoietic-transition,EHT)产生[1, 2]。在这个过程中,HECs通过改变细胞形态并调控动脉程序以获得造血特性[3, 4]。鉴定激活造血过程或抑制动脉特性的调控因子是解析HSPC产生机制的关键,对体外诱导造血干细胞具有重要的临床指导意义。
DNA甲基化在调控基因表达、维持基因组印记、X染色体沉默和调控胚胎发育等方面起着重要作用[5-8]。以往的研究报道了在胚胎发育过程中,DNA甲基化对HSPC产生十分重要[9]。然而,全基因组水平的DNA甲基化修饰调控HSPC细胞命运决定的机制尚不清楚。
近日,中国医学科学院血液病医院(中国医学科学院血液学研究所)王璐研究员与朱平研究员合作在《Development》杂志在线发表了题为“DNA methylation safeguards generation of hematopoietic stem and progenitor cell by repression of Notch signaling”的研究论文,该研究利用斑马鱼模型,描绘了HSPC产生过程中DNA甲基化的动态图谱,揭示了DNA甲基化通过抑制Notch相关基因促进造血干祖细胞产生的新机制。

研究人员选取造血干细胞产生的关键时间点(36 hpf),分选内皮细胞(endothelial cells,ECs)、HECs和HSPCs,利用全基因组亚硫酸氢盐测序(WGBS)和转录组测序(RNA-seq)技术进行深入分析。基于WGBS数据,研究人员鉴定了细胞类型特异的差异甲基化区域(DMRs),描绘了HSPC产生过程中DNA甲基化的动态图谱。进一步通过敲除和敲低DNA甲基化转移酶1(Dnmt1)降低甲基化水平,发现HSPC产生缺陷,说明Dnmt1对HSPC发育至关重要。
随后,通过WGBS和RNA-seq联合数据分析,鉴定出DNA甲基化与转录水平呈现负相关的基因主要富集于血管发育相关通路,尤其是Notch信号通路相关基因;体内实验证明缺失Dnmt1后动脉内皮基因的表达上升。进一步研究发现,DNA甲基化修饰通过抑制Notch信号通路,降低动脉内皮基因表达,促进HSPC产生,而在Dnmt1缺失后,Notch相关基因甲基化降低,表达增强,进而导致Notch活性升高,抑制HSPC产生。
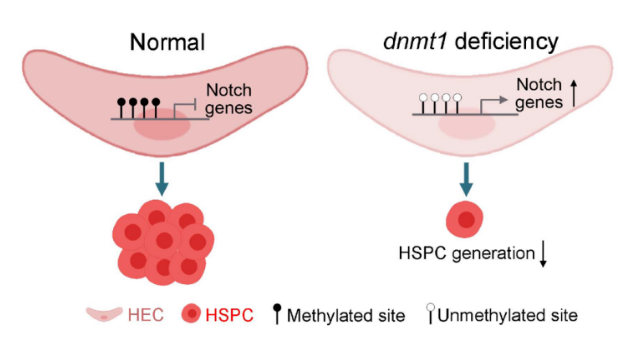
该研究使用多组学技术和功能实验评估了HSPC产生过程的整体DNA甲基化水平动态变化,证明Dnmt1通过抑制Notch信号通路调控HSPC产生。这一发现丰富了我们对体内HSPC产生机制的认识,为体外诱导获得可移植的造血干祖细胞提供新的思路。
中国医学科学院血液病医院(中国医学科学院血液学研究所)王璐研究员、朱平研究员为共同通讯作者。中国科学院动物研究所博士生李妍和中国医学科学院血液病医院(中国医学科学院血液学研究所)博士生唐晁为共同第一作者。该项目获得国家自然科学基金、国家重点研发计划、中国医学科学院医学与健康科技创新工程等基金的支持。
参考文献
1. BERTRAND J Y, CHI N C, SANTOSO B, et al. Haematopoietic stem cells derive directly from aortic endothelium during development [J]. Nature, 2010, 464(7285): 108-11.
2. BOISSET J C, VAN CAPPELLEN W, ANDRIEU-SOLER C, et al. In vivo imaging of haematopoietic cells emerging from the mouse aortic endothelium [J]. Nature, 2010, 464(7285): 116-20.
3. GAMA-NORTON L, FERRANDO E, RUIZ-HERGUIDO C, et al. Notch signal strength controls cell fate in the haemogenic endothelium [J]. Nat Commun, 2015, 6(8510.
4. LIZAMA C O, HAWKINS J S, SCHMITT C E, et al. Repression of arterial genes in hemogenic endothelium is sufficient for haematopoietic fate acquisition [J]. Nat Commun, 2015, 6(7739.
5. BIRD A. DNA methylation patterns and epigenetic memory [J]. Genes Dev, 2002, 16(1): 6-21.
6. CEDAR H, BERGMAN Y. Programming of DNA methylation patterns [J]. Annu Rev Biochem, 2012, 81(97-117.
7. LUO C, HAJKOVA P, ECKER J R. Dynamic DNA methylation: In the right place at the right time [J]. Science, 2018, 361(6409): 1336-40.
8. WANG L, LIU Z, LIN H, et al. Epigenetic regulation of left-right asymmetry by DNA methylation [J]. Embo j, 2017, 36(20): 2987-97.
9. LIU X, JIA X, YUAN H, et al. DNA methyltransferase 1 functions through C/ebpa to maintain hematopoietic stem and progenitor cells in zebrafish [J]. J Hematol Oncol, 2015, 8(15.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Dev#
55
#造血#
67
#祖细胞#
43
学习
62