BMS获得欧盟委员会对CAR-T疗法Breyanzi的支持
2022-02-03 Allan MedSci原创
CHMP 的积极意见是基于 I 期单臂 TRANSCEND NHL 001 试验的结果,以及中期 TRANSCEND WORLD 研究的额外数据。
弥漫大B细胞淋巴瘤(DLBCL)是成人淋巴瘤中最常见的一种类型,并且是一组在临床表现和预后等多方面具有很大异质性的恶性肿瘤。其发病率占非霍奇金淋巴瘤(NHL)的31%~34%,在亚洲国家一般大于40%。我国2011年一项由24个中心联合进行、共收集10 002例病例样本的分析报告指出,在中国DLBCL占所有NHL的45.8%,占所有淋巴瘤的40.1%。
欧洲药品管理局近日表示,其人用药品委员会 (CHMP) 对百时美施贵宝申请 Breyanzi (lisocabtagene maraleucel) 治疗侵袭性淋巴瘤采取了积极意见。具体而言,靶向CD19的 CAR-T 疗法 Breyanzi 被推荐用于成人弥漫性大B细胞淋巴瘤(DLBCL)、原发性纵隔大B细胞淋巴瘤(PMBCL)和3B级滤泡性淋巴瘤(FL3B)的三线治疗。
该公司负责细胞疗法开发的 Anne Kerber 表示,CHMP 的支持代表了“一个重要的里程碑,它承认 Breyanzi 是一种差异化细胞疗法,有可能解决患者未满足的医疗需求”。该疗法去年在美国和日本获批用于某些形式的淋巴瘤患者,并在 2021 年第三季度创造了 3000 万美元的销售额。
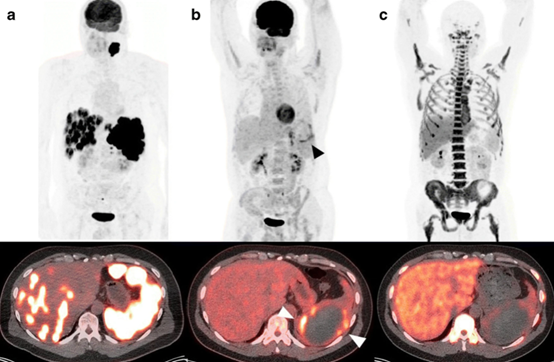
CHMP 的积极意见是基于 I 期单臂 TRANSCEND NHL 001 试验的结果,以及中期 TRANSCEND WORLD 研究的额外数据。百时美施贵宝表示,两者都评估了患有复发性或难治性 DLBCL、PMBCL 和 FL3B 的患者,包括具有一系列组织学和高危疾病的患者。治疗在住院和门诊进行,Breyanzi 在 TRANSCEND NHL 001 的 192 名接受治疗的患者中产生了 73% 的总缓解率(ORR),其中 54% 的患者达到了完全缓解(CR)(图1)。同时,响应者的中位响应持续时间长达 16.7 个月。

图1. TRANSCEND NHL 001 试验中患者的缓解情况
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#CAR-#
24
#BMS#
35
#欧盟委员会#
38
建议批准该口服抗病毒药物用于治疗不需
45
文章写的太棒了
48