摘要
宫颈神经内分泌癌占所有侵袭性宫颈癌的不到2%,分为低级别(类癌和非典型类癌)和高级别(小细胞和大细胞)神经内分泌癌。越来越多的数据表明,宫颈神经内分泌癌可能与人乳头瘤病毒感染(HPV)有关,尤其是HPV18,而且大多数宫颈神经内分泌癌p16免疫组化染色呈阳性。突触蛋白和CD56是宫颈神经内分泌癌最敏感的免疫组化标志物。尽管没有确切的相关基因突变,但PIK3CA、KRAS和TP53是神经内分泌肿瘤中最常见的基因突变。宫颈神经内分泌癌是一种侵袭性极强的肿瘤,极易累及淋巴结并发远处转移。年龄、淋巴结转移、吸烟、小细胞神经内分泌癌所占比率和肿瘤大小是独立的预后因素。总的来说,宫颈神经内分泌癌5年生存率为36%,平均总生存率在22-25个月之间。目前宫颈神经内分泌癌的治疗方案通常是参考小细胞肺癌的治疗以及根据有限的回顾性研究制定的。治疗方法多为综合治疗,包括手术、化疗和全身化疗。最常用的化疗方案是顺铂和依托泊苷的联合用药。在复发性疾病的情况下,拓扑替康、紫杉醇和贝伐单抗的联合治疗已彰显良好的效果。多中心肿瘤注册登记研究,如神经内分泌宫颈肿瘤注册登记研究(NECTUR),是评估肿瘤治疗模式和疗效的一个良好途径。(Salvo G, etal. Int J Gynecol Cancer 29:986–995)
背景
神经内分泌肿瘤是女性生殖道的一类比较罕见的疾病,宫颈是最常见的原发部位之一1。Albores-Saavedra在1972年首次描述了这类肿瘤,它占所有侵袭性宫颈癌的1.4%,在美国每年约有200例新发病例被明确诊断2,3。2014年世界卫生组织(WHO)将宫颈神经内分泌肿瘤分为低级别(以前称为类癌和非典型类癌)和高级神经内分泌癌(以前称为小细胞癌和大细胞癌),见表1。在宫颈神经内分泌癌中,小细胞神经内分泌癌最常见,约占80%,其次是大细胞神经内分泌癌约占12%,其他组织学类型如未分化神经内分泌肿瘤约占8%。
宫颈鳞癌和腺癌主要扩散方式是局部蔓延,但高级别神经内分泌癌与它们不同,即使在早期临床查体发现病灶仅局限于宫颈,它发生淋巴和血源性转移的发生率也很高。这些肿瘤常累及淋巴血管,与HPV18感染密切相关,诊断时淋巴结转移的风险增加,40%的临床期IB1宫颈神经内分泌癌盆腔淋巴结病理结果为阳性,而临床期IB1期宫颈鳞癌淋巴结阳性率为10%-15%3,4。另外,小细胞宫颈神经内分泌癌患者诊断大多已是晚期5,6。以盆腔外转移疾病作为首发诊断的也很常见,特别是在肺和肝中,并且常常与复发的高风险有关7,8。患有小细胞神经内分泌癌患者的中位总生存率的不到2年5 ,6, 9–11。
到目前为止,相关文献中的147项研究报告了总共3538例神经内分泌宫颈癌患者,只有9项研究病例数大于50例3。目前仍缺乏前瞻性研究,这也导致具体的化疗方案的制定与应用有一定的局限性,并且初始治疗呈多模式方法,包括手术、放疗和化疗12 13。在MD安德森癌症中心有神经内分泌宫颈癌的注册研究登记。所有的神经内分泌宫颈癌患者都由同一小组医生治疗。本篇综述的目的是总结关于这种疾病的最新和最相关的信息,并提供诊断和治疗方法。此外还将探讨这种疾病特别之处以求帮助世界各地的医生更好地治疗这一罕见疾病。

病因
宫颈鳞状细胞癌、腺癌和腺鳞癌与人乳头瘤病毒(HPV)之间的关系已得到很好的证实和探讨14 15。对于宫颈神经内分泌癌与HPV之间的关系目前尚未明确确定,但越来越多的研究数据表明它们之间可能存在关联。Alejo等人对49例颈部神经内分泌肿瘤的HPV DNA检测和基因型分布及其与组织学和免疫组化特征的关系进行了探讨16。作者发现86%的神经内分泌肿瘤具有HPV DNA。98%的病例报告单次感染(1例HPV型)。神经内分泌癌中HPV16阳性率为55%,HPV18阳性率为41%,其他类型的HPV阳性率为4%。神经内分泌癌中HPV18的发生率是其他组织学的4倍(41%)(P<0.001)。作者认为,神经内分泌癌和腺癌中较高的HPV18比率表明与其他HPV类型相比,HPV18对腺细胞和神经内分泌细胞的影响更大。同时,他们还发现神经内分泌癌合并腺细胞病变的发病几率要比合并鳞状细胞病变的更高。神经内分泌癌表现出明显的淋巴结转移,这也是HPV18感染相关恶性肿瘤的一个特点17
几乎所有的鳞状细胞癌(97%)和一半的腺癌都表现出p16阳性染色18。Alejo等人的研究发现,p16强阳性染色是神经内分泌癌一种特殊的表现。在86%的神经内分泌癌病例中p16蛋白呈过度表达16。所有类癌、非典型癌和大细胞神经内分泌癌均为p16阳性,小细胞癌中79%为p16阳性。总的来说,89%的病例观察到p16和HPV检测结果一致。在Kuji等人的一项研究中评估了37例高级别神经内分泌癌,发现72%的人有高风险的HPV感染(HPV16占14%,HPV18占86%)19。Castle等人发表了包括32项包含403例小细胞神经内分泌癌病例和9项研究包含45例大细胞神经内分泌肿瘤的荟萃分析20,发现85%的小细胞癌是HPV阳性(HPV16和/或HPV 18:78%)。在五项研究的亚组分析中,包括75例小细胞癌患者,免疫组化检测p16阳性率为93%,HPV阳性率为100%。大细胞神经内分泌癌HPV阳性率为88%(HPV16和/或HPV 18,86%)。
研究探讨宫颈神经内分泌癌与人乳头状瘤病毒感染的可能关系具有重要意义,因为应用人乳头状瘤病毒疫苗有可能预防这些癌症。它也为使用免疫疗法或治疗性疫苗防治患有此类疾病的女性提供了可能。
免疫组化
免疫组化染色常被用于神经内分泌肿瘤的诊断。最常用的神经内分泌染色剂是嗜铬粒蛋白A、突触蛋白、CD56和神经元特异性烯醇化酶。对于大细胞神经内分泌癌,除了HE染色观察形态学外,嗜铬粒蛋白A是有助于明确诊断的最特异的标志物。小细胞神经内分泌肿瘤的标记阳性率在33%到100%之间。在Tempfer等人发表的最新系统综述中,13个最常见的免疫组化标记物是突触蛋白(79%)、神经元特异性烯醇化酶(69%)、嗜铬粒蛋白(66%)和CD56(61%)。突触蛋白和CD56是最敏感的神经内分泌标志物,但CD56缺乏特异性。嗜铬粒蛋白是最特殊的神经内分泌标志物,但缺乏敏感性,小细胞神经内分泌癌的阳性率约为50%。
在Alejo等人的研究中,至少一种免疫组织化学标记物(嗜铬粒蛋白、CD56和/或突触生长素)的阳性率为65%,其中CD56最常见(62%),其次是嗜铬粒蛋白(39%)和突触生长素(26%)16。同样,其他研究者发现CD56是神经内分泌分化最敏感的标志物(62%),其次是嗜铬粒蛋白A(39%)和突触蛋白(26%)21,22。嗜铬粒蛋白的阳性可能与间断性胞浆免疫反应性密切相关,后者仅在高倍放大镜下可见。小细胞神经内分泌癌可能只有局部阳性(常间断细胞质染色),甚至是广谱细胞角蛋白阴性。如前所述,由于高风险HPV感染的存在,大多数宫颈高级神经内分泌癌p16染色呈弥漫性阳性21。
胰岛素瘤相关蛋白1(INSM1)对神经内分泌肿瘤的特异性可能比嗜铬粒蛋白A或突触生长素更高23。在最近的研究中,37例高级神经内分泌病例用神经内分泌标记物和INSM1染色。在86%的病例中,嗜铬粒蛋白A和突触生长素均表达。在95%的病例中检测到INSM1,INSM1蛋白似乎是一种有用的新的神经内分泌标记物,它可能与高级别神经内分泌癌的发生有关。
在一项包含有24例患者大细胞和小细胞神经内分泌宫颈癌的病理报道中,MD安德森癌症中心研究了HER-2/neu、表皮生长因子受体(EGFR)、血管内皮生长因子(VEGF)、环氧合酶-2(COX-2)、雌激素受体和孕酮受体的免疫组化表达和预后作用。23例(96%)表达VEGF,8例(33%)表达EGFR,10例(42%)表达HER-2/neu,7例(29%)表达COX-2。这些因子在大、小细胞神经内分泌癌中的表达无明显差异。只有HER-2/neu表达与存活率相关,表明HER-2/neu表达阴性的患者存活率明显低于肿瘤阳性的患者,分别为14.2个月和33个月(p=0.03)24。
另外,免疫组化染色可能有助于确定转移性小细胞癌的起源部位。一些研究表明,33%-84%的小细胞宫颈癌对甲状腺转录因子-1(TTF-1)呈弥漫性核阳性21 25-27。Liu等人用免疫组织化学比较了23例宫颈小细胞神经内分泌癌和56例肺小细胞癌神经内分泌标记物、TTF-1、p53和Ki-67的不同表达28。肺小细胞癌组织中TTF-1的表达明显高于宫颈癌组织(P=0.003)。尽管两种肿瘤具有相似的形态学特征,但它们具有不同的免疫组化表达谱。两者对CD56和嗜铬粒蛋白A的阳性率相似,但宫颈小细胞神经内分泌癌中突触蛋白的表达明显高于小细胞肺癌(P=0.007)。
免疫组化染色对于宫颈神经内分泌癌诊断十分重要,但应注意,使用标准标记物时,阳性染色可能低至33%,并且染色可能只在病灶处呈局灶阳性。如果诊断仍不明确,应考虑新的标记物,因为它们显示较高的阳性率,比如NMS-1和VEGF。
分子和免疫谱检测
小细胞宫颈癌是一种罕见的肿瘤,并且没有一个确定的分子学突变事件。研究探讨基因突变为该类疾病的治疗提供了个体化治疗机会,尤其是在目前针对复发性疾病有限的治疗方法可供选择的大背景下。高风险HPV可能参与了众多肿瘤发生的早期阶段,其他的分子生物学驱动事件的发生、发展促进小细胞癌的中晚期进展。对致癌驱动因素的鉴定有助于更好地了解神经内分泌肿瘤的演变史。在最新的系统综述中,最常见的突变是p53(26%)、kras(12%)、pik3ca(18%)和c-myc(53%)基因。超过30%的病例中发现杂合子基因丢失13。
Frumovitz等人鉴定了44例单纯或混合型小细胞宫颈癌患者29。所有患者均采用50个癌症相关基因的新一代突变热点序列进行突变分析。24例患者(55%)共鉴定出35个突变。大多数患者(63%)有1个突变,29%有2个突变,8%有3个突变。在所有44例患者中,最常见的突变是pik3ca(n=8;18%)、kras(n=6,14%)和tp53(n=5,11%)。大于7%以上的标本中未发现其他突变。在24名发生突变的患者中,21名(88%)至少发生了一次突变,并且目前存在一类针对该突变的生物制剂。尽管在小细胞宫颈癌患者中未发现常见突变,但近一半患者至少有一个可用于靶向治疗的基因突变靶点。这对于治疗选择有限的复发性疾病患者非常重要。突变分析可能有助于选择一期试验或甚至是“适应症外”治疗的患者。
MD安德森癌症中心的研究小组最近评估了高级神经内分泌宫颈癌标本中PD-L1受体和失配修复蛋白(MLH1、MSH2、MSH6和PMS2)的存在。在23个检测PD-L1表达的样本中,22个(96%)的受体呈阴性。在25个评估微卫星不稳定性(MSI)的标本中,所有(100%)都显示了不匹配修复蛋白的触觉表达。这些研究表明此类复发患者应用PD-1/PD-L1抑制剂药物的疗效较差。
诊断、分期和影像学
宫颈神经内分泌癌的分期采用国际妇产科联合会(FIGO)用于其他宫颈恶性肿瘤的分期系统。2018年FIGO分期系统允许影像学和病理学证据改变肿瘤分期31。鉴于诊断时淋巴结转移率和远处转移率较高,这对于宫颈神经内分泌癌是一个重要的改变。妇科肿瘤学会(SGO)指南建议,考虑到神经内分泌肿瘤中远处转移的高发病率,影像学评估应包括计算机断层扫描(CT)或正电子发射断层扫描(PET/CT)扫描32。
对于局限于宫颈的病变,除临床检查外,盆腔磁共振成像被认为是评估大于1mm肿瘤大小和局部疾病扩展的最好的成像方法33。对于考虑早期宫颈癌的女性,建议行盆腔磁共振成像检查,以确定是否适合手术治疗。另一种选择是经直肠超声检查,尽管此检查在大多数医疗中心并不常用。但对于宫颈癌的其他组织学亚型(鳞状癌、腺癌或腺鳞状癌),由专业放射科医生进行评估时,经直肠超声与MRI检测宫旁浸犯的准确率分别为98.9%和94.7%(p≤0.219)。在检测小肿瘤(<1 cm3)方面,经直肠超声被认为优于MRI(分别为90.5%和81.1%(p≤0.049)。在评估宫颈锥切术后残留肿瘤时,经直肠超声也优于MRI(分别为93.7%和83.2%,P≤0.006)34。
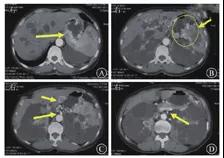
MD安德森癌症中心的经验是进行一次全面的妇科检查,包括直肠阴道检查和PET/CT扫描,进行初始放射学分级。对于考虑局限于宫颈的疾病患者,建议术前行盆腔MRI或超声检查,以评估局部病变侵犯范围。对于那些接受初始放射治疗的患者,采用盆腔核磁共振以制定放射治疗方案。有肺或肝转移或神经症状的情况下进行脑部成像。建议医生使用FIGO 2018系统对患者进行分级,因为根据肿瘤大小、淋巴结扩散和远处转移,FIGO 2018系统可能将患者分为更“真实”或更准确的阶段。考虑到淋巴结状态和远端器官受累,这使得患者可以进行更精确的治疗,并对预后进行更明确的讨论(图1)。

疾病预后
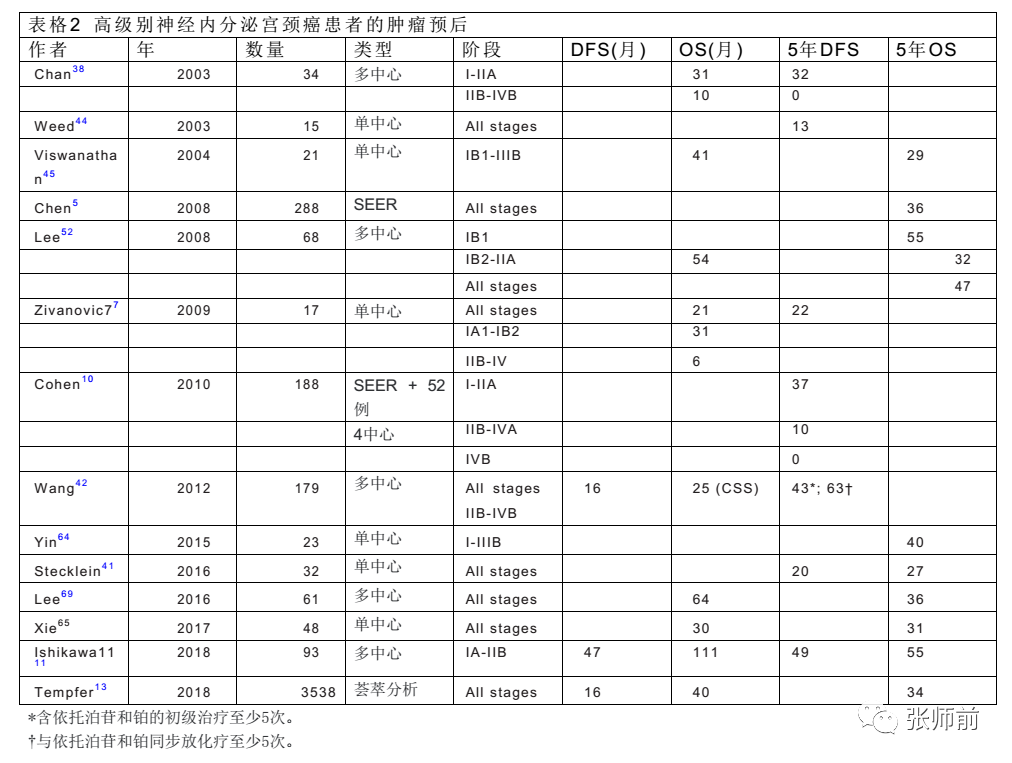
数项研究报告年龄5、淋巴结转移11 ,35–37、种族8、吸烟38、小细胞组织学比率、LVSI11和肿瘤大小35 ,36, 38是宫颈神经内分泌癌的独立预后因素。然而,在大多数研究中,分期是最常见的不良预后因素7, 5, 35–37, 39。总体而言,尽管有多种治疗方案,但宫颈神经内分泌癌患者的预后仍然很差,5年生存率为36%,平均总生存率在22-25个月之间5。早期(I-II)和晚期(IIII-V)区别,其5年总生存率分别为31%-51%和0%-7%,分别为7,38,40(表2)。
初始治疗
疾病早期
在最近发表的一篇系统性综述中,纳入了3538名神经内分泌患者,最常见的初始治疗是根治性手术加上化疗,无论是作为新辅助化疗还是术后辅助化疗(40/48项研究)13。目前仍没有标准的化疗方案,但铂类联合依托泊苷是最常用的治疗方法(24/40项研究)。放射治疗方案也普遍用于疾病的早期阶段(15/48项研究)。SGO32和GCIG都建议对宫颈神经内分泌肿瘤的所有阶段进行多模式治疗,大多数患者接受手术、放疗和化疗的联合治疗41。对于早期疾病(肿瘤≤4 cm)和影像学阴性淋巴结,建议主要采用根治性子宫切除术和盆腔淋巴结切除术,随后用铂类和依托泊苷进行化疗以及考虑加用额外的放射治疗32。
手术治疗
对于比较外科手术和化疗治疗早期、可切除的宫颈神经内分泌癌的疗效目前尚无前瞻性研究。Ishikawa等人对93例宫颈I-II期高级神经内分泌癌患者的研究显示,中位总生存期为111个月,无病生存期为47个月11。不同患者之间的治疗方式存在显著差异,但大多数患者(88;95%)接受了根治性手术,而5例患者(5%)接受放疗。在接受手术的患者中,37例(40%)行根治性手术和盆腔淋巴结切除术联合术后化疗,14例(15%)只接受了手术,25例(27%)手术联合辅助放化疗,或术前实施新辅助化疗。未接受手术作为主要治疗的患者的死亡风险比(HR)为4.74(95%可信区间1.01-15.9)。接受根治性手术的患者总生存率高于接受直接放疗的患者(p=0.043)。作者发现,大多数临床医生倾向于根治性手术,随后辅以依托泊苷+铂类或伊立替康+铂类方案作为I-II期高级别神经内分泌宫颈癌的最佳治疗方案。他们还得出结论,即使是在早期疾病中,局部复发和远处转移也经常发生,因此需要更有效的治疗策略。
Wang等人回顾了146例I-II期疾病患者42。其中,116例(79%)接受了手术作为其主要治疗的一部分(有/无辅助治疗的初次手术、新辅助化疗加根治性子宫切除术或围手术期化疗加根治性子宫切除术)。其余30名患者没有接受手术,而是接受了化疗或不化疗的放射治疗。作者发现,与未接受手术的女性相比,接受根治性手术的女性有更差的无失败生存率(41%对61%,p=0.086)和癌症特异性生存率(48%对62%,p=0.122)的趋势。根据MD安德森癌症中心对I-IIA期临床淋巴结阴性患者的研究,接受直接化疗的患者的中位无事件生存率明显高于接受手术的患者(中位未达到18个月,p=0.04)。基于多个回顾性研究的相互矛盾的结果,早期神经内分泌肿瘤手术的价值似乎仍不明确,但肯定的是,没有辅助化疗和/或放疗的单独手术不适合任何宫颈高级别神经内分泌癌患者。
化疗
不同于手术对宫颈神经内分泌癌的治疗作用,化疗对此类疾病的的治疗地位已经确立。尽管没有标准的化疗方案,但由于其病理表现和临床行为与小细胞肺癌相似,几乎所有小细胞宫颈癌患者都接受铂类和依托泊苷作为其初步治疗的一部分13。对于早期疾病,SGO和GCIG指南建议完全手术切除的患者需要接受辅助化疗3241。Zivanovic等人报告了11例早期疾病患者(IA2-IB2期)7。11例患者中,7例复发,86%的患者有远处复发。接受化疗的患者3年无复发生存率为83%,未接受化疗的患者3年无复发生存率为0%(p=0.03)。接受化疗的患者的3年总生存率估计为83%,未接受化疗作为初始治疗的患者的3年总生存率估计为20%(p=0.36)。Ishikawa等人11发现,接受依托泊苷铂或伊立替康铂辅助化疗的41名患者的无病生存率有所提高(HR 0.27,95%可信区间0.10-0.69)。此外,手术后辅助化疗可减少盆腔复发,OR值为0.37(95%可信区间0.13-0.99,p=0.047)。当给予辅助化疗时,总生存率也有改善的趋势,但在统计学上并不显著(HR 0.39,95%可信区间0.15-1.01)。Lee等人报道了术后给予化疗的有利证据43,并得出结论:早期疾病患者首选的治疗方式是先行根治性手术,后行辅助化疗。关于辅助化疗的周期数,Pei等人回顾性地评估了92例I-II期小细胞癌患者44,发现顺铂和依托泊苷辅助化疗至少5周期与改善5年无复发生存率相关。这与采用其他治疗形成了鲜明对比(68%:21%,P<0.001)。多变量分析显示,结节性疾病(P<0.003)、参数延长(P<0.03)、依托泊苷+顺铂周期(顺铂-依托泊苷<5个周期:P<0.001,无化疗:P<0.004)是疾病复发的独立预后因素。
盆腔外照射
Lee等人报道的一项回顾性研究,包括68例IB1-IIA期宫颈神经内分泌癌患者,表明在辅助化疗后进行根治性子宫切除术可能足够,因为接受化疗的患者似乎没有更好的结局43。在日本一项多中心研究中,接受术后放疗的患者(16%)与未接受放疗的患者(25%)相比,术后盆腔复发的风险较低,但差异没有达到显著性(OR 0.61,95%可信区间0.16至2.01)11。来自MD 安德森的癌症中心数据显示,首次复发最常见的部位是骨盆外:肺部38%,肝脏34%,25%表现为癌性病变38。25%的患者有脑转移,且始终处于并发肺或肝转移的状态。如果患者接受放射治疗,只有21%的患者再次复发。
对于早期疾病,化疗似乎是治疗的一个关键组成部分,但对于联合手术和化疗的作用,仍缺乏令人信服的数据。
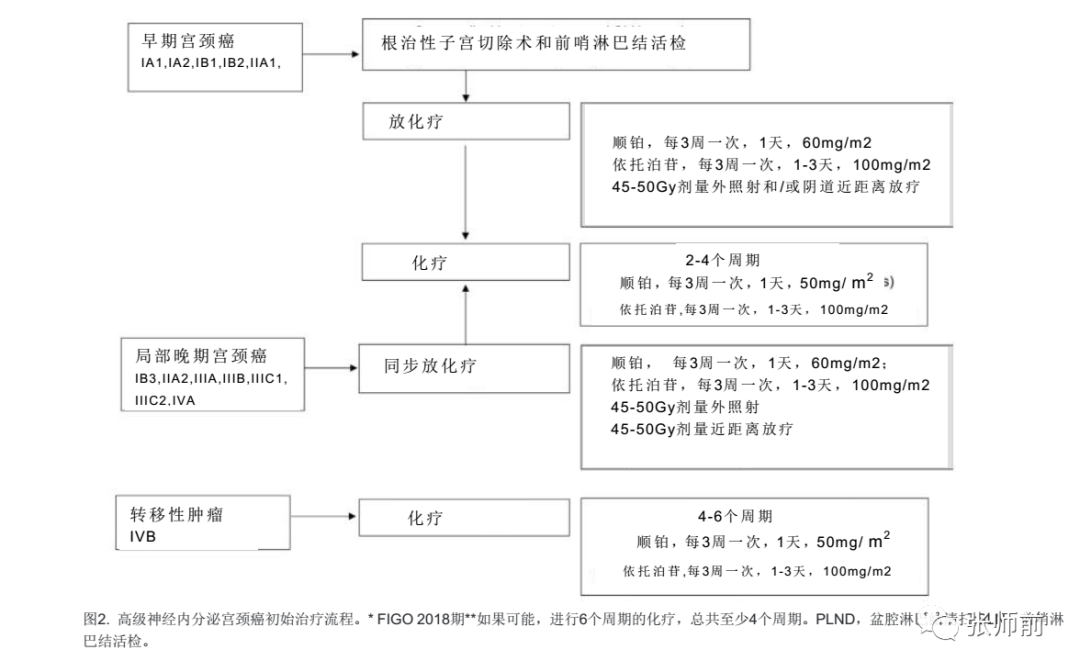
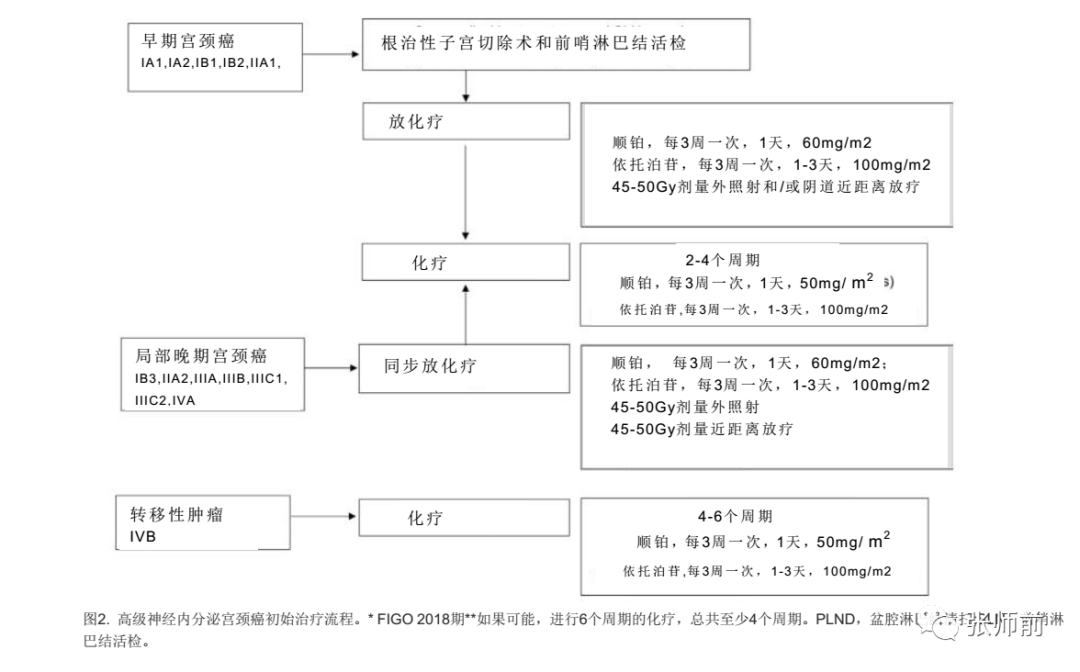
在MD安德森癌症早期疾病中心(肿瘤≤4cm)和术前影像学阴性淋巴结的方案是开放性根治性子宫切除术和前哨淋巴结活检。术后建议包括同时使用顺铂和依托泊苷进行辅助化疗。化疗方案包括顺铂60 mg/m2在第1天和依托泊苷100 mg/m2在第1-3天每21天。将依托泊苷的剂量从120降低到100,是因为同时进行放疗可能会增加化疗毒副作用。患者接受两个周期的先期化疗,并在放射治疗完成后再接受两到四个周期。理想情况下的目标是患者能够接受总共六个周期化疗。为了降低术后放疗的治疗发病率,推荐仅在双侧盆腔淋巴结完成示踪定位时才进行前哨淋巴结切除和不完全淋巴结切除(图2)。
预防性头颅放射治疗
由于小细胞宫颈癌的治疗来源于小细胞肺癌的文献,在小细胞肺癌中,预防性脑照射通常用于隐匿性转移,因此,MD安德森癌症中心已经探讨了这种方法在宫颈小细胞肿瘤中的应用。Wilde at al在2003年报告中提到,25%(2/8)明显早期小细胞宫颈癌患者发生脑转移,因此他们提出了预防性头颅辐射45。然而,SGO关于对无症状小细胞癌患者的初步评估指南既不推荐常规的脑部CT也不建议进行颅脑放射治疗。在他们14年的回顾性经验中,没有发现颅骨转移35。来自MD安德森癌症中心的数据表明,当发现其他器官转移时,大部分发现脑转移(7/8患者,86%)46, 47。
作为初始治疗方案的一部分,MD安德森癌症中心不推荐为无神经系统症状患者进行预防性全脑放射治疗。
保留生殖力的手术
由于在宫颈神经内分泌癌的患者平均年龄约为37岁(范围24-77岁),因而保留生育能力成为患者和医生共同关心的问题46。这类群体患者面临的两个主要问题是卵巢 (激素和生殖功能)和子宫去留。由于它涉及卵巢保存和维持局部晚期疾病患者卵巢功能的问题,可以考虑卵巢移位术。然而,即使这样做,在盆腔放疗和/或近距离治疗后,只有大约65%的患者保留了卵巢功能。此外,特别是在神经内分泌肿瘤患者中,理论上由残留卵巢内微小病灶的风险。
没有数据支持早期疾病患者考虑保留生育能力,如单纯宫颈锥切或根治性宫颈切除术。尽管保留生育能力的手术在早期小细胞宫颈癌患者中有报道,NCCN指南不推荐宫颈神经内分泌癌患者保留子宫生育能力的治疗。考虑到大多数病人可能接受术后放射治疗,保留生育功能手术不应作为为常规术式。
MD安德森癌症中心对此类患者的治疗策略是延迟2到3周开始进行相关治疗,从而有时间进行促排卵和卵子收集。另外,在根治性手术时,如果术中发现卵巢非常正常,那么在计划术后放疗或局部晚期疾病最终放化疗之前进行卵巢移位术也是合理的。对于年轻女性(小于50岁),因为手术和/或放疗提前进入更年期,建议可以使用激素替代疗法。但强烈反对任何保留子宫的手术,如单纯锥切术、单纯宫颈切除术或根治宫颈切除术。
局部晚期宫颈癌
SGO指南推荐局部晚期或不适宜手术宫颈神经内分泌癌的患者进行联合化疗(铂和依托泊苷)和放疗32。最常用化疗方案是顺铂和依托泊苷方案,通常是在第1天顺铂60 ~ 80 mg/ m2,依托泊苷浓度为80 ~ 120 mg/ m2,每21 ~ 28天一个周期53-55。另外,卡铂可替代顺铂。其他方案如紫杉醇和顺铂,紫杉醇和卡铂,以及联合长春新碱,顺铂,博莱霉素也有报道。
Hoskins首次报道顺铂和依托泊苷与放疗同时进行是安全的,同时在完成放射治疗后再给予顺铂和依托泊苷化疗35。化疗后联合放化疗疗结果显示,在IB-IVB期,同步放化疗+顺铂依托泊苷化疗5周期以上明显改善5年无病生存率(63% vs 13%, p=0.025)和总体生存率(75% vs 17%, p=0.016)42。宫颈神经内分泌癌远处复发是最常见的复发类型(28%),临床结局与初始病变程度相关。3年无病生存率为55%,三年后远处复发可能不大39。
Bajaj等发表的一篇摘要报道了73例在美国7个中心接受放化疗的小细胞宫颈癌IB2-IVA期患者55,56。中位数随访时间19个月,66%的患者复发。平均复发时间为10个月。复发与吸烟 (HR 3.32, p<0.01),总放疗剂量(EQD2) <50 Gy vs 71-80 Gy (HR 3.3, p=0.07),无近距离治疗(HR 1.5, p=0.25)有关。15%的患者出现脑复发。近距离治疗(HR 0.05, p<0.01)、总放疗剂量(EQD2) >75 Gy(HR 0.11, p=0.04)、顺铂、依托泊苷与单纯顺铂治疗(HR 0.35, p=0.23)均可降低脑复发率。所有患者的总生存率为48%,得益于辅助化疗后同步放化疗与单纯放化疗比较(HR 0.49, p=0.10)。化疗周期数(顺铂-依托泊苷)与总生存率(HR 0.45, p=0.01)和复发率(HR 0.67, p=0.07)有相关性。接受顺铂-依托泊苷治疗的患者总体生存率较单纯接受顺铂治疗的患者有明显提高(59%对44%),复发率较低(65% VS 74%)。Robin等人在癌症数据库(NCDB)筛选了100名局部晚期非转移性神经内分泌宫颈癌患者,在2004年至2012年间均接受了明确的放化疗57。在多因素分析中,与单纯的体外放射治疗相比,近距离放射治疗的增加与中位生存期的改善相关(49个月vs . 22个月,HR0.48, 95% CI 0.25 ~ 0.88)。接受新辅助化疗的患者与同时接受同步放化疗的患者的总体生存率无差异。
对于IB3-IVA (FIGO 2018)期疾病或不适宜手术的患者,MD安德森癌症中心建议顺铂和依托泊苷进行化疗,随后再进行顺铂和依托泊苷的额外化疗,总共四到六个周期(两个周期进行放疗,两到四个周期在放疗完成后进行)。目标是总共六个周期。对于有IVB期疾病的妇女,建议使用顺铂和依托泊苷进行姑息性化疗(图2)
复发性疾病
初次复发
对于神经内分泌宫颈癌患者,目前尚没有标准治疗方案,缺乏最佳治疗方案的共识,而SGO和GCIG均推荐个体化治疗32、41。通常标准化疗药物选择包括单剂托泊替康、伊立替康、紫杉醇或多西他赛,因为这些方案通常用于治疗复发性小细胞肺癌。MD安德森癌症中心的经验表明,这些单药方案对复发性神经内分泌宫颈癌患者的疗效较差。
对复发性或进展性疾病患者的选择方案是三药联合方案,包括拓扑替康、紫杉醇和贝伐单抗,这种方案采用的是与GOG240研究相同的治疗方案,它是一项针对复发性宫颈癌(鳞状细胞癌、腺癌和腺鳞癌)设计的III期临床试验研究。这种用药方案的基本依据是,首先,以前接受过早期化疗的患者可以接受这种三药方案。其次,由于单剂紫杉醇或拓扑替康均具有足够的抗癌药理活性,且经常用于复发性小细胞肺癌,因此组合可能与单剂方案具有相同的抗癌活性,并且可能比单剂方案更具有抗癌活性。再次,95%以上小细胞宫颈癌在的表达血管上皮生长因子受体,理论上支持贝伐单抗作为一种额外抗癌药物增加疗效24。最后,这三种药物均已被美国食品药品监督管理局批准用于复发性宫颈癌的治疗,不存在索赔方面的担心。三药联合治疗方案的相关治疗效果发表了大宗的对复发性神经内分泌子宫颈癌的报道中59。13名接受拓扑替康、紫杉醇和贝伐单抗治疗的患者与21名接受其他治疗的患者进行比较,这些患者接受了其他方案的大多是以铂类为基础,含或不含紫杉醇的化疗策略。三药联合方案都能够明显改善预后。三药联合方案中位无进展生存期与和其他方案的对比分别为8个月和4个月(HR 0.21,95%CI 0.09至0.54)。三药联合方案的中位总生存期为9.7个月,接受其他方案的患者的中位总生存期为9.4个月(HR 0.53,95%CI 0.23-1.22)。对于三药联合疗法,62%的患者接受了6个月以上治疗,31%接受了12个月以上治疗,而接受其他方案的患者19%患者接受了6个月以上治疗,仅10%的患者接受了12个月以上治疗。
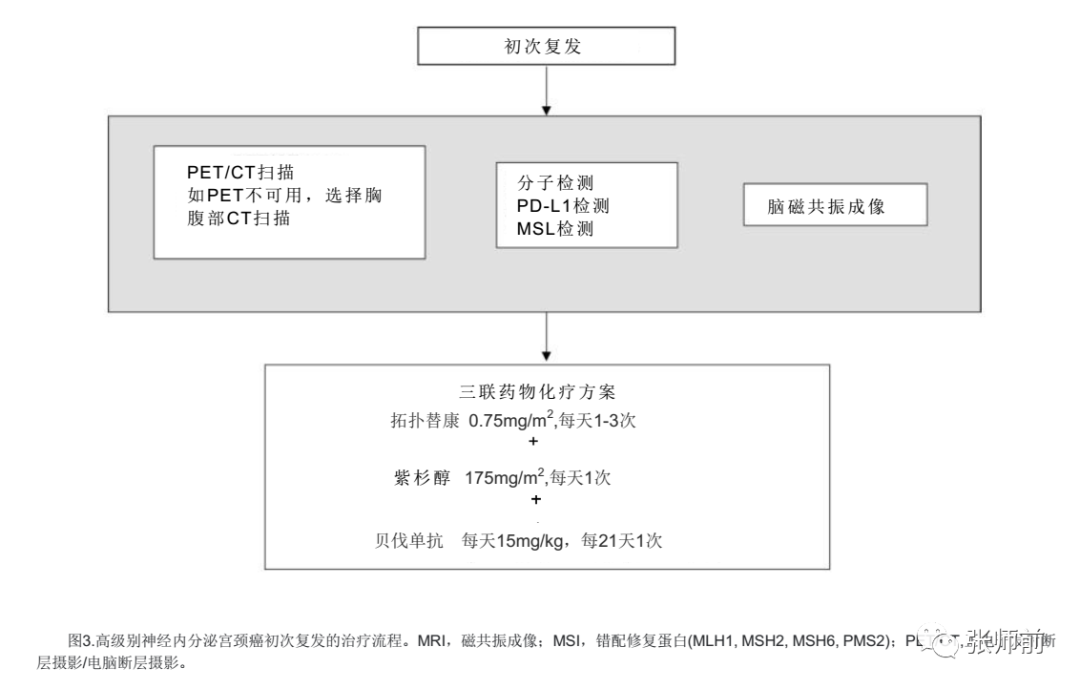
对于初次复发的神经内分泌宫颈癌患者,MD安德森癌症中心通常采用三种药物治疗方案:拓扑替康(第1-3天为0.75 mg/m2)、紫杉醇(第1天为175 mg/m2)和贝伐单抗(第1天为15 mg/kg,21天周期)(“德克萨斯鸡尾酒”疗法)。作为治疗复发性疾病的策略的一部分,初次复发的神经内分泌宫颈癌患者进行分子学检测、PD-L1和失配修复蛋白(MLH1、MSH2、MSH6和PMS2)检测。由于大多数复发患者最终疾病会有进展,这种检测以利于患者进行分类,进而提供针对性方案,见图3。
多次复发
对于神经内分泌宫颈癌多次复发患者,免疫位点抑制剂和靶向治疗可能是有益的;但是基于这种情况的文献报道非常罕见,迄今为止只三例相关病例报道。Paraghamian等对一名复发、转移、PD-L1阴性的小细胞神经内分泌宫颈癌患者使用nivolumab,该患者用药反应良好。Sharabi等报道了一例转移性、化疗难治性神经内分泌宫颈癌患者,由于肿瘤负担过重而导致肠梗阻。液基细胞学检查显示该患者存在一系列的肿瘤突变。患者接受放射治疗并服用了nivolumab,获得了至少10个月的疾病完全缓解。然而,使用免疫位点抑制剂的相关经验令人失望,至今为止还没有正式报道。如上所述,高级别的神经内分泌宫颈肿瘤几乎都是PD-L1阴性的并且均是MSI稳定类型的,因此应谨慎使用免疫位点抑制剂。Lyons等人使用丝裂原激活蛋白激酶1抑制剂 trametinib治疗复发性小细胞神经细胞癌,患者有a-KRAS突变,并在三个周期后出现完全反应。在MD安德森癌症中心,对于使用托泊替康、紫杉醇和贝伐单抗治疗后病情进展的患者,建议进行基于临床试验的靶向治疗。当患者经过靶向治疗或免疫治疗后病情依然进展时,建议进行基于一期临床试验的相关治疗或临终关怀。
随访
对于宫颈鳞状细胞癌、腺癌和腺鳞癌的随访,推荐进行包括盆腔检查在内的体格检查,每3至6个月检查一次,持续2年,然后每6至12个月再检查一次,持续3年。此外,应每年进行一次细胞学检测。对于宫颈神经内分泌肿瘤,SGO指南推荐定期进行包含全身CT或PET/CT扫描检查。
参考文献(略)

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










原文在哪里?
58
#神经内分泌#
46
#分泌#
48
刚遇到一个宫颈大细胞神经内分泌癌的就遇到这篇文章
0
#子宫颈#
50
#内分泌肿瘤#
52
#宫颈#
37