BioNTech新冠mRNA疫苗或将7月前在中国获批,多款国外疫苗引入疫苗进展缓慢
2021-04-29 JACKZHAO MedSci原创
4月28日,当地时间,德国生物科技公司BioNTech创始人兼首席执行官Ugur Sahin在参加德国外国记者协会的一次线上会议时称公司旗下研发的mRNA新冠疫苗BNT162b2或将于7月前在中国获批

4月28日,当地时间,德国生物科技公司BioNTech创始人兼首席执行官Ugur Sahin在参加德国外国记者协会的一次线上会议时称公司旗下研发的mRNA新冠疫苗BNT162b2或将于7月前在中国获批。
此前,《华尔街日报》、《环球时报》英文版援引消息人士报道,中国很有可能在7月份以前批准德国BioNTech和中国复星医药联合开发的新冠疫苗。一旦疫苗获得授权,将会在内地迅速推出,疫苗生产工厂以及冷链配送演习等准备工作正在进行中。
复星医药与BioNTech已与去年3月签订合作协议,复星医药与BioNTech达成战略合作,共同在中国大陆及港澳台地区开发、商业化基于其专有的mRNA 技术平台研发的、针对新型冠状病毒的疫苗产品。
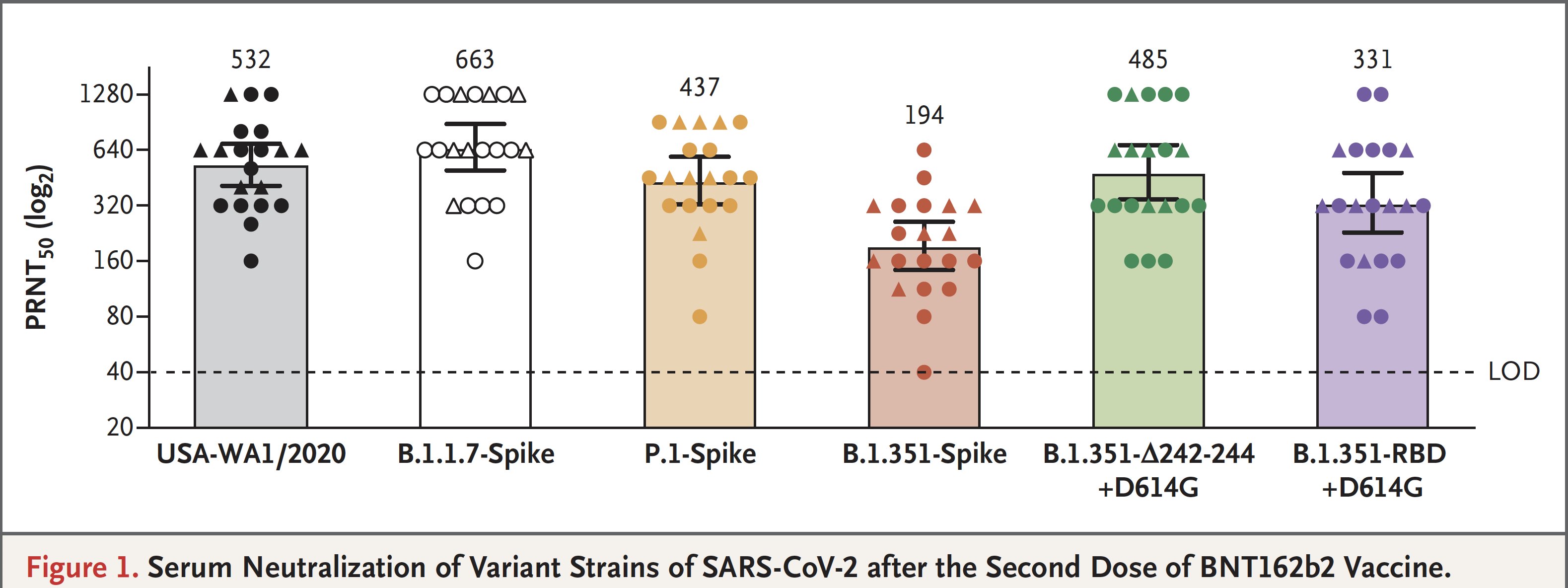 第二剂BNT162b2疫苗后,SARS-CoV-2变异株的血清中和
第二剂BNT162b2疫苗后,SARS-CoV-2变异株的血清中和
BNT162b2是一款mRNA新冠疫苗,携带病毒遗传信息,疫苗注入人体后,产生新冠病毒部分抗原蛋白,诱发人体免疫反应。2020年11月,临床III期数据显示BNT162b2保护率为95%。而以色列研究人员2月进行的总计596618 人的大规模接种疫苗研究称该疫苗在真实世界中有效率为94%。BNT162b2疫苗可以预防工作年龄成人的有症状和无症状感染。并且可以有效应对主要变异为B1.1.7毒株。
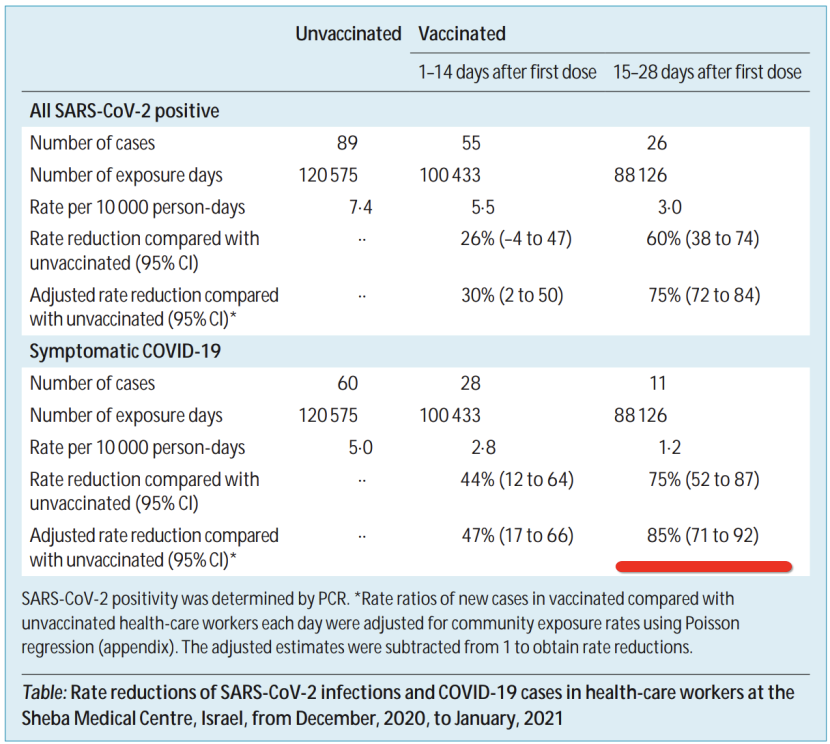
Early rate reductions of SARS-CoV-2 infection and COVID-19 in BNT162b2 vaccine recipients,Published Online February 18, 2021 https://doi.org/10.1016/ S0140-6736(21)00448-7
研究团队观察以色列接种的9000多名医护人员结果发现,在接种第一剂疫苗后的15天至28天内,出现新冠症状的人数减少了85%。特别是,研究人员还观察到了对无症状患者的疗效。接种首剂BioNTech疫苗后所有感染(包括无症状)均减少了75%。
4月21日,BioNTech近期曾与上海市政府、中国区代理商复星医药曾举行线上电话会。Ugur Sahin则称,BioNTech对与上海的合作高度重视、充满信心,将与中国合作伙伴复星医药紧密合作,加快推进新冠疫苗合作。
据梅斯医学了解到,去年11月24日启动的新冠mRNA疫苗BNT162b2 II期临床试验已近尾声。该实验由江苏省疾控中心(江苏省公共卫生研究院)负责,试验泰州中国医药城疫苗工程中心和涟水县疾控中心、泰州市人民医院、涟水县人民医院等多个单位参与其中。
复星医药高级副总裁、全球研发中心总裁兼首席医学官回爱民曾表示,作为全球研发的重要组成部分,BNT162b2在中国的第二阶段临床研究不仅将为该疫苗在中国的上市提供关键数据,也可能对该疫苗在全球其他民族的广泛推广和使用起到积极作用,尤其是在其他亚洲国家和地区。
 复星医药公告
复星医药公告
香港特区政府与今年1月25日批准 BNT162b2在港紧急使用。但在3月24日,该疫苗的接种因包装瑕疵一度暂停,并于4月5日恢复该款疫苗接种。
据了解数款国外疫苗引入进度缓慢
康泰生物3月22日在投资者互动平台表示,公司与阿斯利康的合作方式为技术引进,而非代工生产。公司在完成产品技术转移相关工作后,已经在国内自主实施临床前研究,产品将以国内的疫苗监管要求为标准向相关审批部门报批。康泰生物腺病毒载体新冠疫苗车间,预计产能可达4亿剂/年。历史公告显示,康泰生物2020年8月起与英国阿斯利康签署合作协议,引进腺病毒载体新冠疫苗在国内进行临床开发、产业化。并在2021年底前将该疫苗设计产能扩大至年产至少2亿剂,以满足中国市场的需求。
华兰生物于4月19日晚间发布公告,俄罗斯HV公司向华兰生物子公司华兰疫苗转移Sputnik-V(卫星五号疫苗)新冠疫苗5L/200L培养规模的生产技术,华兰疫苗在该技术基础上进行2500L培养规模的生产技术开发,生产技术开发成功后HV公司向华兰疫苗下达许可产品生产订单,订单数量不低于1亿剂(5000万人份)。
Sputnik-V(卫星五号疫苗)新冠疫苗由伽马勒研究所研发,是世界上第一个基于研究透彻的人类腺病毒载体平台的注册疫苗。“Sputnik V”疫苗已经在超过60个国家注册。俄罗斯的“Sputnik V”注册后临床试验涉及31000多名志愿者,Sputnik V的III期临床研究分析结果显示,在第二剂注射7天后,有效率达91.4%。2020年8月11日,俄罗斯卫星五号疫苗在未发布任何数据的情况下成为全球第一个获得批准注册的新冠疫苗。
而西藏药业计划900万美元(约人民币5889.69万元)豪赌引进引进俄罗斯卫星5号(Sputnik-V腺病毒载体新冠疫苗)暂未有进展披露。
2020年11月,西藏药业全资子公司Top Ridge Pharma Limited曾与俄罗斯Human Vaccine公司展开合作,获得Sputnik-V腺病毒载体疫苗在中国大陆及港澳台地区的注册、开发、生产、进口或商业化产品及向指定区域出口等相关权益许可权。
但相关公告同时指出,由于西藏药业尚不具备腺病毒疫苗的研发生产能力,将另行委托第三方在国内进行疫苗的技术转移和前期研发生产工作
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#Bio#
28
#RNA疫苗#
38
#TEC#
25
#BioNTech#
32
新冠肺炎,疫情何时才能消失
56