Nature子刊:肿瘤逃逸?阻止其分泌类固醇或可延缓肿瘤生长
2020-08-05 转化医学网 转化医学网
早前的研究已经表明,肿瘤可以通过使免疫细胞产生免疫抑制类固醇来逃避免疫系统。近日,来自剑桥大学韦康桑格研究所(Wellcome Sanger Institute)病理科和MRC癌症部门的研究人员发现,
该研究发表在《自然通讯》杂志上,题目为“Tumors induce de novo steroid biosynthesis in T cells to evade immunity”。

研究小组在小鼠身上测试了黑色素瘤和乳腺肿瘤的T细胞,使用单细胞RNA测序来查看每个细胞中到底哪些基因被激活了。研究人员发现,来自肿瘤的T细胞确实会产生类固醇,这可能会降低它们对抗肿瘤的效力。
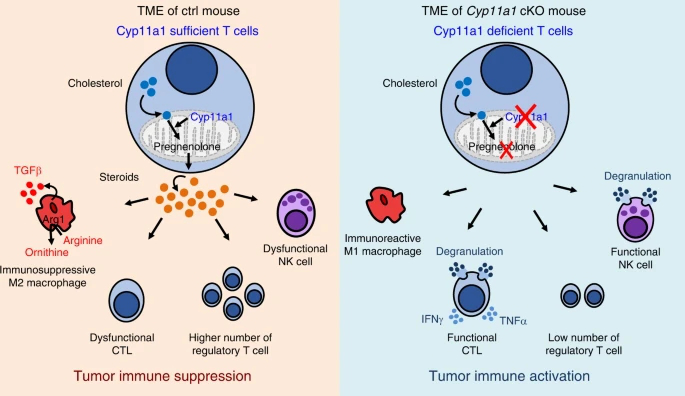
为了测试关闭类固醇的产生,研究人员对T细胞中缺失一个关键类固醇合成基因cyp11a1的小鼠进行了研究。他们发现,尽管正常野生型小鼠的肿瘤发展迅速,但敲除小鼠的肿瘤生长受到抑制,所有肿瘤都小得多,生长速度也慢得多。他们还发现,一种抑制Cyp11a1蛋白活性的药物氨鲁米特(aminoglutethimide)也能减少正常小鼠体内的肿瘤。
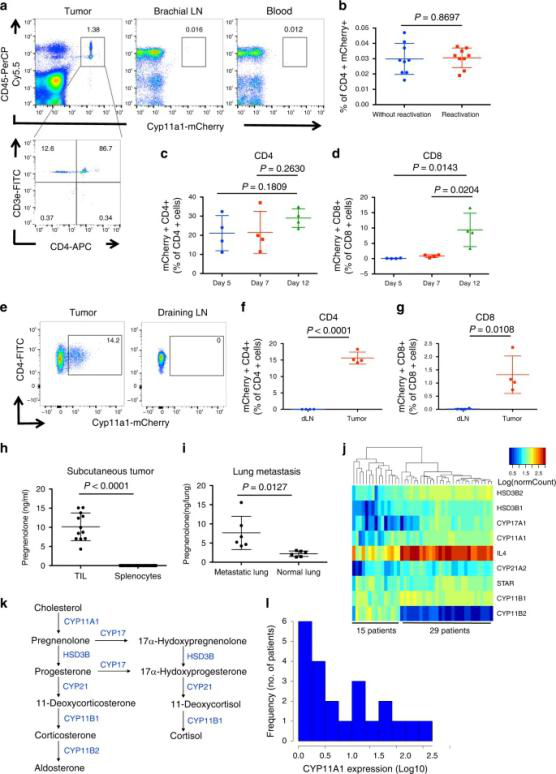

细胞瘤内Cyp11a1+ T细胞在scRNAseq中的基因表达鉴定
来自剑桥医学研究委员会癌症部门的Jacqui Shields博士说:“使用小鼠模型,我们证实了,阻止T细胞产生类固醇对肿瘤的生长有很大的影响,显著地降低了肿瘤的生长。不管是去除关键基因,还是用药物阻止其发挥作用,都会刺激抗肿瘤免疫。这表明类固醇生成途径在设计癌症免疫疗法的药物靶点方面可能是一个真正的竞争者,能够帮助治疗癌症患者。”

T细胞类固醇形成的消融抑制了实验肿瘤的生长和转移
来自韦尔科姆桑格研究所的资深作者萨拉·泰奇曼(Sarah Teichmann)博士表示,“这项研究可能为癌症免疫治疗的新希望铺平道路。虽然这些结果来自小鼠,但来自人类组织的初步数据表明,同样的肿瘤防御也可能发生在人类身上,现在需要进一步的研究来证明人类癌症的直接证据。如果这一点得到证实,未来就有可能以这种免疫抑制途径为目标,创造新的治疗方法来重新启动免疫系统,并帮助拯救生命。”
【1】https://medicalxpress.com/news/2020-07-immune-cell-steroids-tumours-suppress.html
【2】https://www.nature.com/articles/s41467-020-17339-6
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#分泌#
23
#肿瘤逃逸#
27
#Nat#
36
#类固醇#
0