Leukemia:重磅新概念!新手段-全基因组分析识别“Double-hit”多发性骨髓瘤
2018-07-14 不忘初心 肿瘤资讯
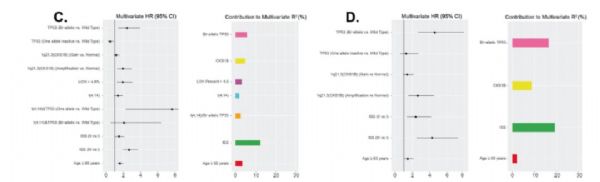
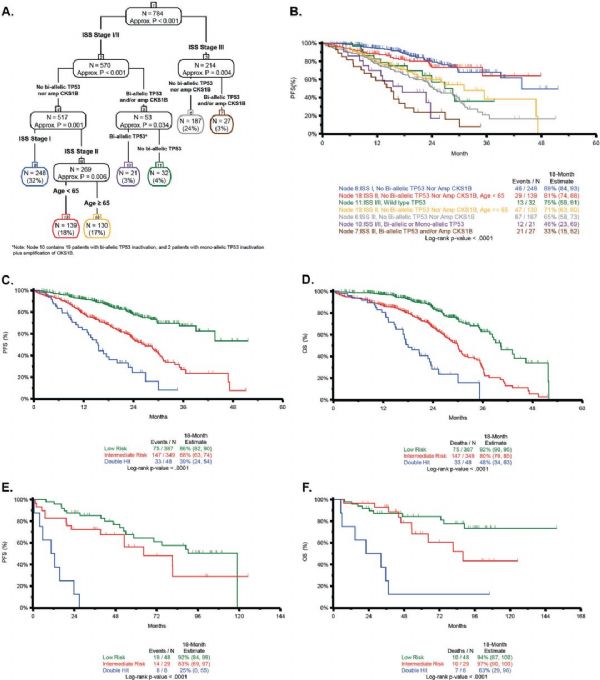
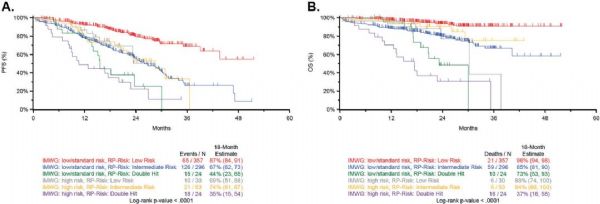
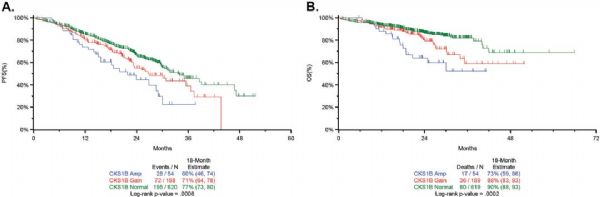
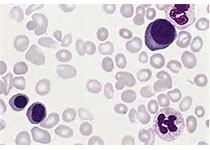
在新诊断多发性骨髓瘤(NDMM)中建立的迄今为止最大的分子和临床数据集全基因组分析中,将具有TP53双等位基因失活和/或CKS1B(1q21)扩增(≥4个拷贝)的国际分期系统(ISS)Ⅲ期MM患者定义为Double-Hit MM占6.1%,中位OS为20.7月。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#多发性#
28
#基因组分析#
32
#全基因组分析#
36
#HIT#
24
学习了谢谢分享学习!!
56
#全基因组#
19
#重磅#
21
好文章.学习了.
61