阿特珠单抗联合贝伐珠能显著改善患者生存质量(IMbrave150研究)
2020-04-02 MedSci MedSci原创
罗氏宣布,评估PD-L1抑制剂atezolizumab(阿替利珠单抗)联合bevacizumab(贝伐珠单抗)治疗既往未接受过系统治疗的不可切除的肝细胞癌(HCC)患者的3期临床研究IMbrave15
罗氏宣布,评估PD-L1抑制剂atezolizumab(阿替利珠单抗)联合bevacizumab(贝伐珠单抗)治疗既往未接受过系统治疗的不可切除的肝细胞癌(HCC)患者的3期临床研究IMbrave150达到了两个共同主要终点,证明与标准疗法sorafenib(索拉非尼)相比,在总生存期(OS)和无进展生存期(PFS)方面达到统计显著和临床意义的改善。
肝细胞癌(HCC)是一种常见的恶性肿瘤,全球每年有超过750,000人患有肝细胞癌,几乎一半的病例在中国,治疗选择有限。
阿替利珠单抗是一种抗PD-L1的人源化IgG1单克隆抗体,通过阻断PD-L1与其受体PD-1和B7-1(也称为CD80)的相互结合,从而解除肿瘤免疫微环境抑制状态和T细胞耗竭,促进肿瘤特异性T细胞活化、增殖和杀伤效应,从而实现清除肿瘤细胞的目的。
贝伐珠单抗是一种血管内皮生长因子(VEGF)抑制剂,除具有已知的抗血管生成作用外,贝伐珠单抗还可通过抑制VEGF相关免疫抑制作用、促进T细胞肿瘤浸润以及启动和激活T细胞对肿瘤抗原的应答以进一步增强阿替利珠单抗激活免疫系统杀灭肿瘤细胞的能力。
在今年的ESMO年会上公布的国际多中心、开放标签的Ⅰb期试验(GO30140)结果显示,在有效性方面,主要终点指标客观缓解率(ORR)达到了36%,表明阿替利珠单抗联合贝伐珠单抗有望成为不可切除HCC患者的一线治疗选择。
胃肠道肿瘤领域世界顶级学术盛会——美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI)将在美国旧金山召开,本次会议将探讨和交流食管癌、胃癌、肝胆癌、结直肠癌、胰腺癌等领域的最新研究成果。2019年ESMO-ASIA大会上,IMbrave 150研究公布的结果显示,与索拉非尼相比,对阿特珠单抗+贝伐珠单抗可显著改善晚期不可切除肝细胞癌患者的总生存期(OS)与无进展生存期(PFS),联合组和索拉非尼组的中位OS分别为未达到和13.2个月(HR=0.58,P=0.0006),中位PFS分别为6.8个月和4.3个月(HR=0.59,P<0.0001),疾病进展和死亡死亡降低41%。
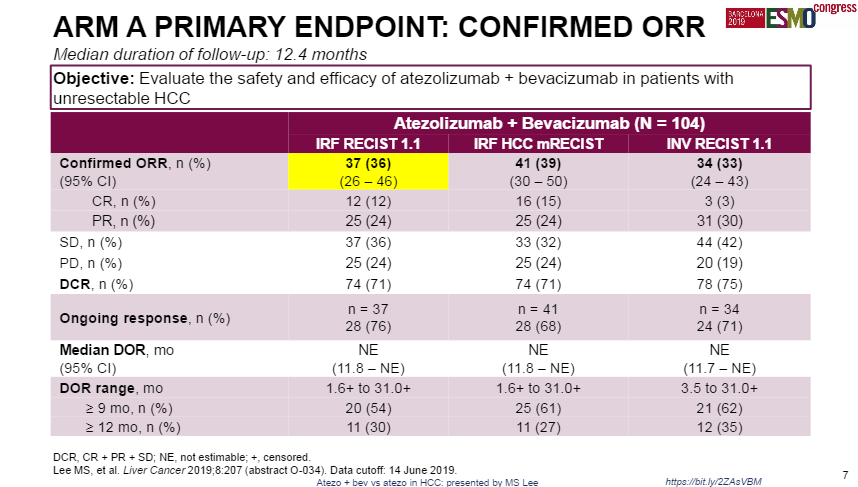
IMbrave150研究是首个在肝癌免疫治疗获得成功的III期研究,此次进一步公布阿特珠单抗+贝伐珠单抗于晚期肝细胞癌的患者报告结局(PRO)。
研究背景
IMbrave150是一项在全球多中心III期临床研究,旨在评估阿特珠单抗+贝伐珠单抗对比标准治疗用于不可切除肝细胞癌患者一线治疗的疗效和安全性。IMbrave150是一项在501名既往未接受过系统性治疗的不可切除的肝细胞癌患者中开展的全球性III期、多中心、开放性研究。患者按照2:1的比例随机接受阿替利珠单抗和贝伐珠单抗联合治疗或索拉非尼治疗。在每个21天周期的第1天经静脉注射给予阿替利珠单抗1200 mg;在每个21天周期的第1天经静脉注射给予贝伐珠单抗15 mg/kg。在每个21天周期的第1-21天口服给予索拉非尼,400 mg/天,每天2次。患者接受联合治疗或对照组治疗,直至出现不可接受的毒性或研究者确定无临床获益。本次会议中公布了患者报告结局(PRO),从患者角度评估了联合治疗的临床获益。
研究方法
患者按2:1比例随机分配接受阿特珠单抗1200mg静脉注射+贝伐珠单抗15mg/kg静脉注射,每3周一次,或索拉非尼400mg口服,2次/日,直至无临床获益或出现不可接受的毒性。治疗前,患者完成EORTC QLQ-C30和EORTC QLQ-HCC18 问卷,治疗期间每3周一次,治疗停止或疾病进展后每3月一次。预先设定的次要终点是患者报告的生活质量(QOL)、机体功能、至恶化时间(连续2次评估显示自基线下降≥10%或评估后3周内死亡)。预先设定的探索性分析包括关键性的PROs中有临床意义的变化(超过基线10%)的TTD和患者比例。
该研究的共同主要终点为独立审查机构(IRF)根据RECIST v1.1评估的OS和PFS。次要疗效终点包括根据RECIST v1.1(研究者评估的[INV]和IRF)和HCC mRECIST(IRF)评估的ORR、至疾病进展的时间(TTP)和缓解持续时间(DOR)以及患者报告结局(PRO)、安全性和药代动力学。
研究结果
从基线开始以及大部分治疗期间,二组的问卷完成率≥92%。与索拉非尼相比,联合组延迟了患者报告的QOL的TTD(中位TTD,11.2和3.6个月;HR,0.63[95%CI:0.46,0.85])、机体功能的TTD(中位TTD,13.1和4.9个月;HR,0.53[95%CI:0.39,0.73])和角色功能的TTD(中位TTD,9.1和3.6个月;HR,0.62[95%CI:0.46,0.84])。患者报告的食欲丧失、疲劳、疼痛和腹泻等表现的TTD中,联合组治疗均较索拉非尼延迟,联合组治疗患者较索拉非尼治疗患者发生有临床意义的恶化的比例更低。
结论
来自IMbrave150研究的高质量PRO结果显示,阿特珠单抗+贝伐珠单抗治疗在关键临床症状方面有较大且一致的获益,这些结果进一步支持一线阿特珠单抗+贝伐珠单抗用于初治不可切除HCC患者能获得总体临床获益。
参考来源:
Abstract-476.Patient-reported outcomes (PROs) from the Phase III IMbrave150 trial of atezolizumab (atezo) + bevacizumab (bev) vs sorafenib (sor) as first-line treatment (tx) for patients (pts) with unresectable hepatocellular carcinoma (HCC). Oral Abstract Session B. ASCO-GI 2020.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#患者生存#
29
#生存质量#
40
#贝伐珠#
28
#贝伐#
39