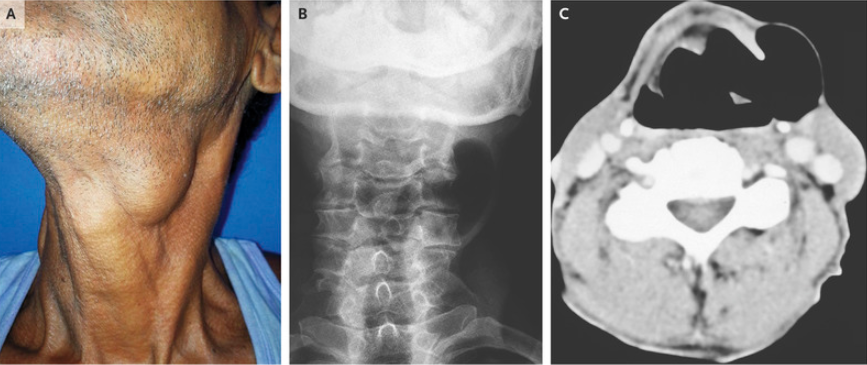
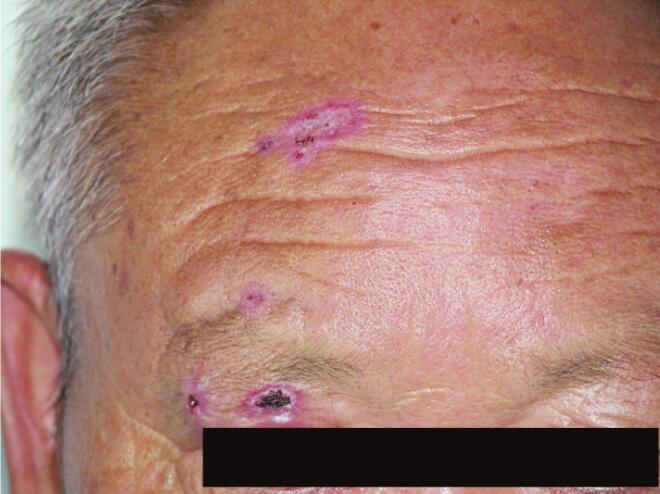
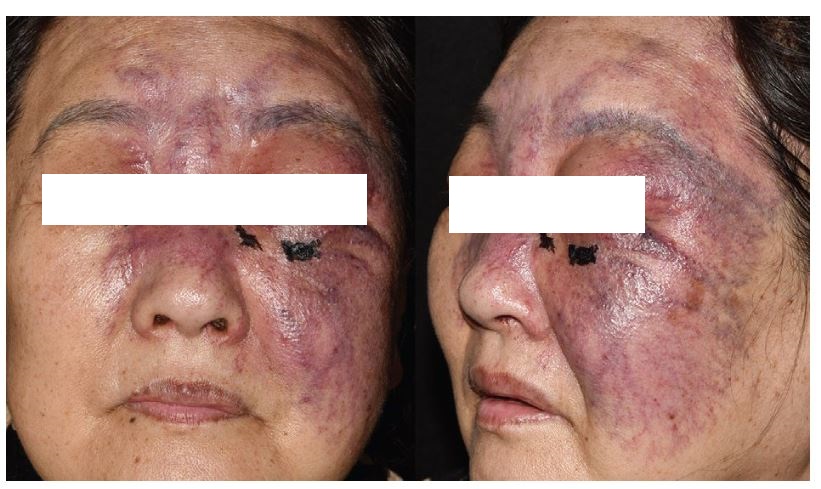
一、病史简介
女性,46岁,江苏人,2019-03-13入中山医院感染病科
主诉:眼部红肿半年余,发热、咽痛、听力下降1月
现病史:
2018年8下旬出现左眼红肿伴流泪,无视物模糊、重影,无脓性分泌物。五官科医院就诊,查WBC 12.7×109/L,N% 79%,Hb 114g/L,CRP 102mg/L;眼部超声:左眼玻璃体混浊,玻璃体后脱离。考虑急性结膜炎,予左氧氟沙星、更昔洛韦、氟米龙滴眼液治疗,症状无缓解。2018年9月上旬左眼肿痛加重,回当地医院予左氧氟沙星0.5g qd iv gtt及地塞米松 5mg qd iv,症状可部分缓解,但易反复,继续不规律使用该方案治疗,每月2-3次,每次2-3天,持续4月。
2019-02-06出现咽痛伴声嘶,当地医院颈部CT:喉部水肿、左甲状软骨外缘隆起、左鼻咽软组织增厚,咽隐窝变浅;胸部平扫CT无殊。予哌拉西林/他唑巴坦2.5g bid×3天,02-09症状加重伴呼吸困难,Tmax 38.1℃,WBC 20.8×109/L,N% 86.8%,HB 94g/L,CRP 259mg/L,PCT 0.17ng/ml;喉镜示声带披裂区高度水肿。考虑II度喉梗阻,予地塞米松15mg qd治疗,水肿缓解,但激素减量后仍有发热,并出现双耳听力下降。
2019-02-15至上海某医院查WBC 20.8*10^9/l,N% 86.8%,HB 96g/l,PCT 0.167ng/ml,CRP 259mg/l,头颅平扫CT无殊,予头孢曲松 2g qd+左氧氟沙星0.5g qd+地塞米松 5mg qd。02-25体温至38.7 ℃,电测听:左耳感音神经性聋,右耳听阈40db;随访眼部超声:左眼球壁水肿。予头孢西丁2g bid+莫西沙星 0.4 qd。02-27腰穿:脑脊液清亮,压力160mmH2O,常规、生化、微生物涂片及培养均未见异常。02-28体温至39℃,调整为美罗培南1q q8h,仍发热,Tmax 38.4℃左右,左眼红肿好转,但进一步出现右眼红肿明显伴分泌物增多,右耳肿胀伴听力丧失。
二、入院检查(2019-3-13)
【体格检查】
T 36.8℃,P 80bpm,R 18次/分,BP 101/71mmHg
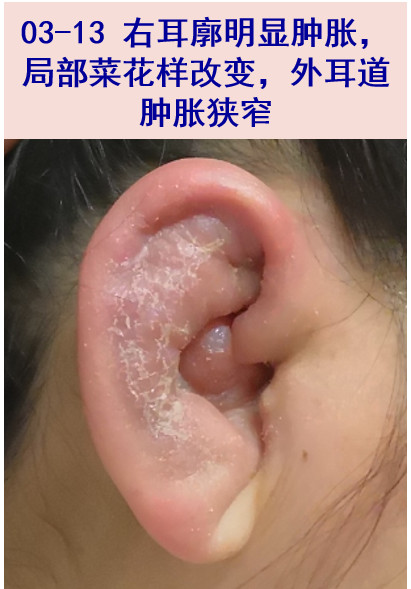
神清,浅表淋巴结未及肿大。右眼红肿,眼裂缩小,内眦处浅红色息肉样增生;右耳廓明显肿胀,局部菜花样改变,有触痛,外耳道肿胀狭窄,少量干性分泌物,右耳听力丧失。左眼及左耳外观基本正常,左耳听力丧失。脑膜刺激征(-)。
【实验室检查】
血常规:WBC 9.4×109/L;N%78.8%;EOS% 0.6%;Hb 80g/L ↓;PLT 732×109/L ↑ ;
炎症标志物:CRP113.6mg/L ↑;ESR 63mm/H ↑;PCT<0.02ng/ml;
生化:ALT/AST 45/25 U/L;Alb 27g/L ↓;Scr 37μmol/L ↓;UA 151μmol/L ↓;IgE 72 IU/ml;抗“O”224 IU/ml ↑;随机血糖 8.4mmol/L;糖化血红蛋白 7.6%↑;
自身抗体:抗β2-糖蛋白1抗体24.1 RU/ml ↑;抗平滑肌抗体(+);余正常;
24小时尿蛋白定量:0.21g ↑;
隐球菌荚膜抗原(-);
T-SPOT A/B:0/0;
【辅助检查】
心电图:正常;
心超:静息状态下正常,未见瓣膜赘生物。

三、临床分析
病史特点:患者中年女性,慢性病程,以单侧眼部及耳部红肿疼痛伴听力下降为主要表现,过程中有发热、咽喉部受累,随后左眼、耳的肿痛转移至右侧,白细胞及CRP明显升高,给予抗感染治疗效果不佳,加用糖皮质激素治疗后症状可部分缓解。诊断和鉴别诊断考虑如下:
感染性疾病:同一时间段内患者以单侧眼耳受累为主,表现为红肿疼痛,可见分泌物,实验室检查CRP及血沉等炎症标志物显着升高,需考虑眼、耳部感染。然而局部及全身广谱抗菌药物治疗无效,后相继出现喉梗阻、发热、听力下降、贫血及蛋白尿,上述症状似乎无法以局部感染解释。由于病变集中于头面部,不排除颅内特殊病原体感染播散所致。但患者神清,无头痛且脑膜刺激征阴性;外院查头颅CT无殊,腰穿脑脊液压力不高,常规、生化及微生物检查均无阳性发现,中枢感染依据不足。
复发性多软骨炎:患者中年女性,同时有眼部和耳廓的红肿,先后出现喉梗阻、听力下降等症状,从典型临床表现可符合复发性多软骨炎。该疾病常累及耳、鼻、喉部及气管等多处软骨,且病程反复,严重者可因气道塌陷而窒息,活动期炎症指标显着升高;同时亦可累及关节、血管、血液系统,造成贫血和系统性血管炎继发肾脏病变,出现蛋白尿。
ANCA相关性血管炎:ANCA相关性血管炎亦可引起肾脏、眼部及耳软骨受累,虽然患者自身抗体中ANCA阴性,仍不能据此排除,如有条件可进一步行相关部位活检进行鉴别。
四、进一步检查、诊治过程和治疗反应
03-13 予哌拉西林/他唑巴坦4.5g q8h+左氧氟沙星0.5g qd抗感染,入院当天仍发热,抽血培养、血NGS;拟送眼部、耳部分泌物微生物检查。
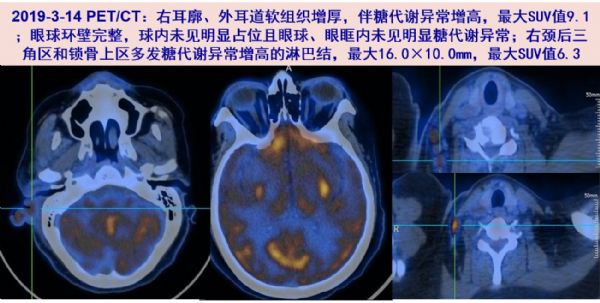
03-14 PET/CT:1.右耳及颈部、锁骨区淋巴结炎性病变可能;两侧乳突炎;2.左肺慢性炎性结节可能;双侧胸腔少量积液;3.肠系膜脂膜炎可能;左肾钙化灶。
03-15 耳鼻喉科会诊:查体见右耳廓红肿增厚伴压痛,外耳道狭窄,鼓膜完整,略浑浊,左耳未见明显异常。鼻腔通畅,鼻甲不肿,咽部粘膜稍充血。考虑耳廓软骨膜炎可能。眼科会诊考虑右侧巩膜炎。建议风湿科会诊。因右眼分泌物少、右耳道无分泌物,未能留取微生物相关检查。
03-16 患者诉头晕,头颅增强MRI:脑实质未见明显异常;两侧乳突炎。
03-18 拟右侧锁骨上淋巴结穿刺,介入超声:右侧锁骨上见多个低回声团块,最大12*5mm,不宜穿刺。

03-19 哌拉西林/他唑巴坦+左氧氟沙星抗感染治疗5天,仍发热,体温波动于37.4-38.1 ℃,右眼红肿及耳廓肿胀无明显好转。请耳鼻喉科、眼科、风湿科及核医学科进行多学科疑难病例讨论。综合分析,考虑复发性多软骨炎可能性大,建议激素冲击治疗,必要时联合免疫抑制剂,建议气道三维CT评估有无气道软骨累及。
03-19起予甲泼尼松龙80mgq8h iv gtt*3天,同时予以丙种免疫球蛋白10g qd iv gtt*3天。03-20体温平,右眼肿胀明显缓解。
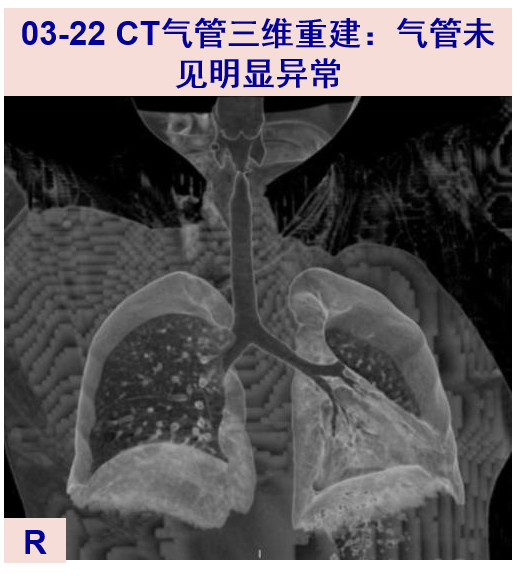
03-22 患者右眼肿胀基本恢复,右耳肿胀明显缓解,调整甲泼尼松龙为40mg qd po并联合沙利度胺50mg qn po。抗感染治疗改为:哌拉西林/他唑巴坦+ SMZ-Co 2# tid po。气道三维重建:气管未见明显异常。
03-25 患者体温平,右眼、右耳肿胀基本消退,仍有听力障碍,较入院时稍有改善,炎症标志物明显下降:WBC 6.44X109/L;NE 57.4%;CRP 4.7mg/L;ESR 69mm/H,予以口服甲泼尼龙40mg qd+ 沙利度胺 50mg qn+ SMZ-Co 2# tid po 出院,建议风湿科随访。
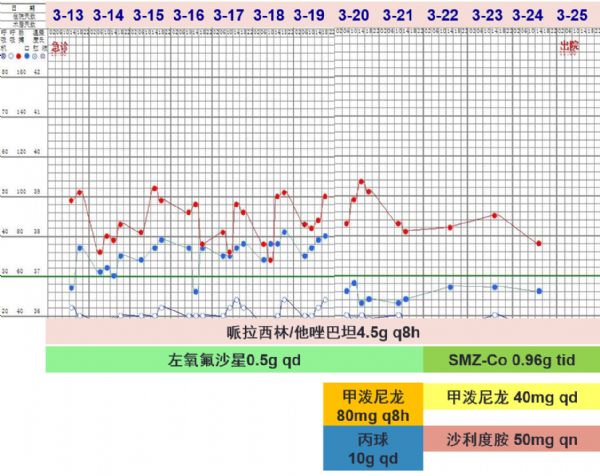
体温及用药情况
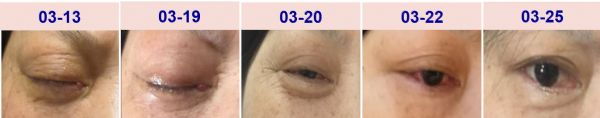
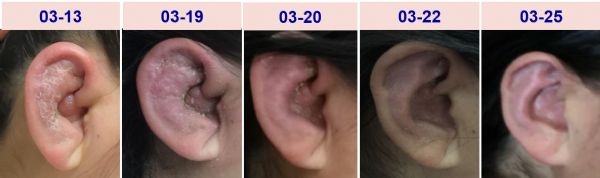
右眼及右耳情况
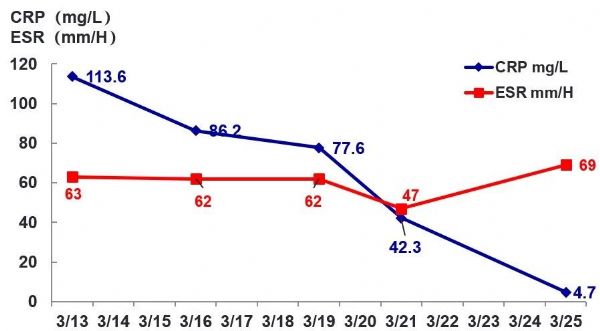
炎症标志物
五、最后诊断与诊断依据
最后诊断:
复发性多软骨炎(累及眼、耳、喉、血管和肾脏)
眼耳继发细菌感染可能
类固醇性糖尿病
诊断依据:
患者中年女性,病程半年余,起病初表现为单侧的眼部红肿,过程中出现发热、咽喉部受累,后演变为对侧眼部及耳部的病变、听力下降至完全丧失,并出现贫血、头晕及蛋白尿,哌拉西林/他唑巴坦+左氧氟沙星抗感染治疗5天无明显疗效,加用糖皮质激素治疗后病情很快好转。因患者存在眼炎、耳软骨炎、喉部及耳蜗和前庭的受损,根据1975年McAdam标准可临床诊断为复发性多软骨炎。由于复发性多软骨炎可累及血管和血液系统,活动期可因系统性血管导致肾脏病变,出现蛋白尿等;亦可出现正细胞性贫血。
六、经验与体会
复发性多软骨炎(replasing polychondritis, RPC)是一种免疫介导的疾病,伴软骨结构及全身其他组织的炎症,尤其是耳、鼻、眼、关节和呼吸道,好发于40-60岁,男女发病率相当。本例患者以眼、耳部红肿为主要表现。RPC眼部受累形式多样,包括巩膜炎、周边溃疡性角膜炎、葡萄膜炎等。RPC耳部的疼痛和压痛很明显,最初的发作易误诊为感染。患者起病时多次就诊于眼科、耳鼻喉科,均以局部感染性疾病处理长达4月,反映临床医生对这种罕见疾病认知不足。RPC的耳部病变具有特征性,受累耳廓可见片状或弥散性红斑,炎症持续发作可最终形成“菜花耳”外观,但无软骨的耳垂不受累,这一点可与该部位普通的软组织感染鉴别。
RPC最危急的情况为累及喉部及气管软骨引起气道梗阻,约半数患者有喉部及气管病变,而1/4有喉部及气管狭窄。本例患者在病程中出现声嘶、呼吸困难,喉部高度水肿引起喉梗阻,虽及时激素治疗,但症状缓解后并未做进一步的气管评估且激素剂量及疗程不足,易导致病情反复甚至加重。气道评估的方法包括肺功能、气管镜及CT等影像学检查。虽然气管镜检查对气道的观察较为直观,但对于可能存在气道显着受损的患者有加重气道梗阻的风险,此时通过CT进行气管支气管图像的三维重建很有价值。考虑到本例患者气道受累可能,因此未行气管镜检查,而以CT气管三维重建进行评估。近年来人们发现PET/CT可提示无症状性的,尚无CT上可见结构改变的软骨受累,对于早期发现气管软骨病变并及时予以干预、改善预后意义重大。
除了气道梗阻外,RPC的另一大主要死因是感染。至少有两方面因素促使感染风险增加:其一是包括激素在内的免疫抑制治疗,其二是疾病导致气道分泌物排出困难继发肺部感染。本例患者接受了大剂量的激素治疗,合并类固醇性糖尿病,同时伴气道受累,不能忽视对于感染风险的评估。
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言