LVIS支架辅助弹簧圈栓塞治疗大脑中动脉支架成形术后假性动脉瘤一例
2020-06-02 李广文 孙玉杰 刘彤晖 中国现代神经疾病杂志 神经科病例撷英拾粹
患者女性,44岁。主因左侧肢体麻木、无力约3年,加重2周,于2018年9月14日入院。患者约3年前无明显诱因出现左侧肢体麻木、无力,遂于2015年11月24日至我院就诊,门诊MRI及MRA检查提示右侧
患者女性,44岁。主因左侧肢体麻木、无力约3年,加重2周,于2018年9月14日入院。患者约3年前无明显诱因出现左侧肢体麻木、无力,遂于2015年11月24日至我院就诊,门诊MRI及MRA检查提示右侧半卵圆中心软化灶,右侧大脑中动脉主干局限性重度狭窄;临床诊断为缺血性卒中,右侧大脑中动脉重度狭窄。常规服用阿司匹林100mg/d联合氯吡格雷75mg/d双联抗血小板治疗21天后改为阿司匹林100mg/d口服,同时长期服用阿托伐他汀20mg/d调脂和稳定斑块,症状逐渐缓解。2周前无明显诱因再次出现左侧肢体麻木、无力且症状进行性加重。为求进一步诊断与治疗,再次至我院复查,以“缺血性卒中,右侧大脑中动脉重度狭窄”收人院。患者自发病以来,精神一般,睡眠、饮食尚可,大小便无异常,体重无明显变化。既往高血压病史3年,长期服用缬沙坦80mg/d,血压控制一般。个人史、家族史无特殊。
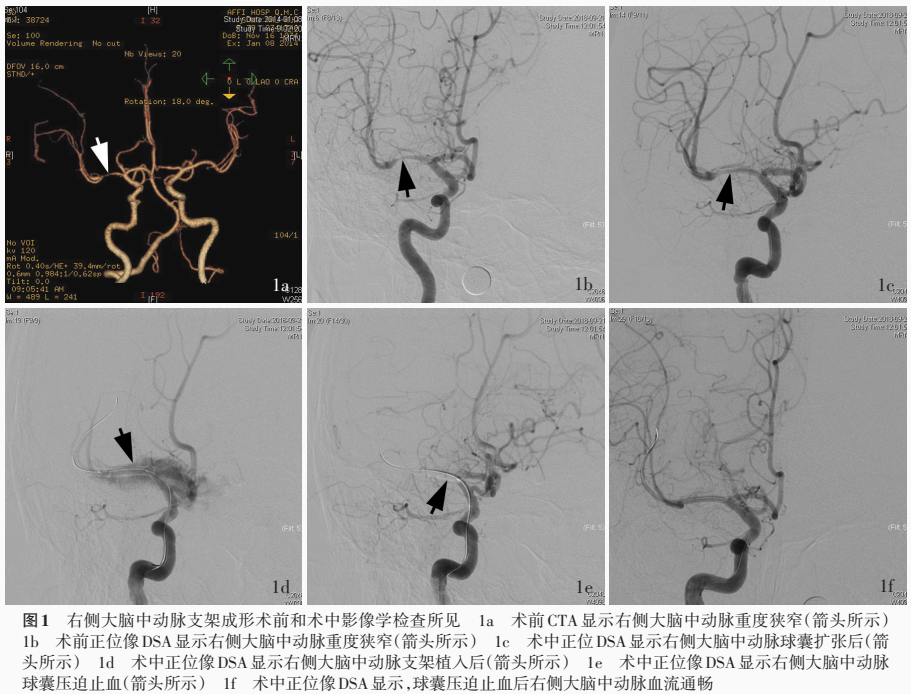
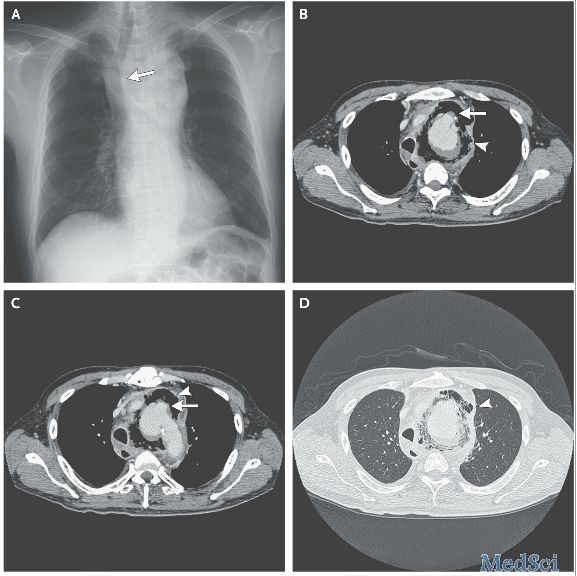
首次入院诊断与治疗经过 体格检查:神志清楚,语言欠清晰,精神一般,高级智能活动正常;双侧瞳孔等大、等圆,直径约3mm,对光反射灵敏,眼球各向活动尚可;右侧鼻唇沟正常,伸舌居中;左侧肢体肌力4级、右侧5级,肌张力均正常;双侧肢体感觉基本对称。实验室检查各项指标无明显异常。头部MRI未见明显异常;CTA显示右侧大脑中动脉M1段远端局限性重度狭窄(图1a);DSA可见右侧大脑中动脉M1段重度狭窄,狭窄率达80%(图1b)、长度约10mm,狭窄近端及远端管腔直径约2.50mm,改良脑梗死溶栓血流分级(mTICI)2b级。根据患者临床症状与体征、辅助检查结果,临床诊断为右侧大脑中动脉重度狭窄、缺血性卒中、高血压(1级)。人院后即予以阿司匹林100mg/d、氯吡格雷75mg/d和阿托伐他汀20mg/d等药物口服。于2018年9月21日在全身麻醉下行右侧大脑中动脉支架成形术,在DSA监视下将6F Envoy导管(美国Cordis公司)置于右侧颈内动脉C2段,0.014in×200cm的Synchro微导丝(美国Stryker公司)缓慢通过右侧大脑中动脉狭窄段并稳定在M2~M3段;MINI TREK球囊(2mm×12mm,美国Abbott公司)精确定位后以810.60kPa的压力扩张,DSA显示狭窄段血流灌注明显改善、残留狭窄率约30%(图1c)后即行NOVA球囊扩张支架(2.25mm×2.00mm,美国Sanofi公司)定位并810.60kPa的压力持续扩张球囊3秒,以支架完全张开为释放成功。术中DSA发现支架植入部位对比剂外渗(图1d),以低压力充盈球囊阻塞血流并以球囊封闭血管(图le),鱼精蛋白15mg中和肝素等,30分钟后再次行DSA可见无对比剂外渗,支架贴壁良好、残留狭窄率<10%(图1f),并且狭窄远端血流灌注明显改善,mTICl分级为3级。术后即刻腰椎穿刺脑脊液检查可见血性脑脊液流出,压力约为150mmH2O(1mm H2O=9.81×10-3kPa,80-180mm H2O),予尼莫地平5ml/h预防血管痉挛、复方甘露醇250ml/次(3次/d)脱水降低颅内压。手术次日复查头部CT,显示多发脑沟、脑池内高密度影,提示蛛网膜下腔出血;通过腰椎穿刺连续释放血性脑脊液,至术后第5天(2018年9月25日)CT显示颅内出血基本吸收方停止治疗。患者共住院12天,出院时左侧肢体麻木、无力症状改善,且无其他自觉症状与体征。
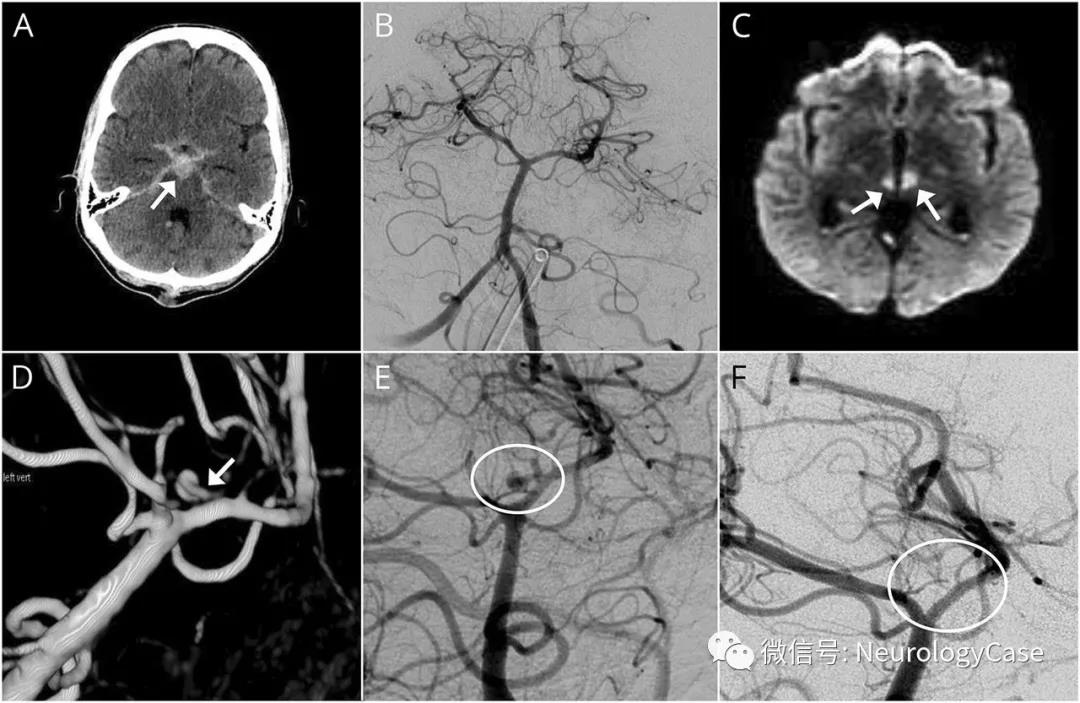
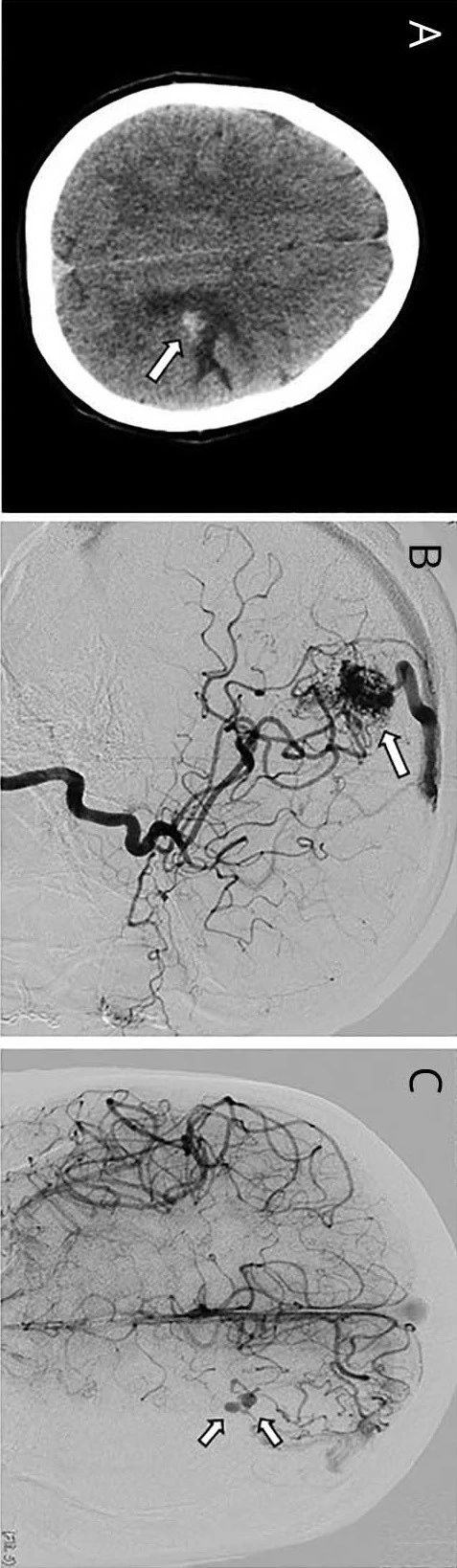
再次入院诊断与治疗经过 患者出院后2个月(2018年11月14日)再次入院复查,头部DSA显示右侧大脑中动脉支架成形术后改变,血管腔外可见一囊袋样膨出,大小约7.40mm×3.60mm,内可见对比剂滞留,排空延迟(图2a),考虑假性动脉瘤形成.大脑中动脉血流及其远端血流灌注尚可。为防止假性动脉瘤破裂,2018年11月19日在全身麻醉下行颅内动脉瘤栓塞术。患者仰卧位,选用6F EnvoyDA导引导管(德国Medos公司)推送至右侧颈内动脉C2段,再次经DSA确认假性动脉瘤形态及位置;然后选取合适工作角度,Echelon-10微导管(美国Stryker公司)塑形后配合Transend微导丝(美国Stryker公司)推送至动脉瘤内,将微导丝通过狭窄段血管至右侧大脑中动脉,交换置入Headway21微导管(美国Ternumo公司)至右侧大脑中动脉远端,经Echelon-10微导管依次采用4mm×80mm、2mm×60mm和2mm×60mm弹簧圈填塞动脉瘤腔,并经Headway21微导管植入3.50mm×15.00mm LVIS自膨式密网支架(美国Terumo公司)至载瘤动脉段释放辅助栓塞;DSA显示动脉瘤填塞满意(图2b),释放支架、撤除微导管。患者住院9天,术后常规服用阿司匹林100mg/d和氯吡格雷75mg/d,治疗21天后改为阿司匹林100mg/d和阿托伐他汀20mg/d长期口服。术后6个月复查,头部CT未见颅内梗死灶,恢复良好(图2c)。

讨论
颅内动脉粥样硬化性狭窄既是缺血性脑血管病的主要原因(30%-40%),又是导致病死的预测因子,我国高达51%的缺血性脑血管病均为颅内动脉狭窄所致。随着血管狭窄程度的增加,脑卒中复发率也随之升高,狭窄率≥70%的患者1年内缺血性脑血管病复发率>20%。近年公布的临床试验结果提示,通过严格筛选手术适应证,采用血管内治疗脑卒中的30天复发率仅为4.3%,明显低于支架成形术和强化药物治疗预防颅内动脉狭窄患者脑卒中复发研究(SAMMPRISE)和Vitesse支架治疗缺血性卒中研究(VISSIT)。对于存在低灌注的颅内动脉重度狭窄患者,于缺血性卒中发病14天后行血管内支架成形术可以显著降低脑卒中复发率。本文病例治疗前存在偏侧肢体无力症状,并经DSA证实患侧血流灌注下降且长期药物治疗无效,故施以右侧大脑中动脉支架成形术,术后临床症状明显改善,提示手术治疗有效。
球囊扩张或支架释放过程导致的血管破裂是支架成形术的严重并发症,如果不能及时止血即可导致严重后果。本文病例术中于支架释放后出现的大脑中动脉破裂,主要与颅内动脉解剖结构、所选择的球囊扩张支架直径过大或狭窄血管的病变性质有关。颅内动脉管壁较其他脏器动脉管壁薄,而且血管中膜平滑肌和外膜弹力纤维相对较少,当血管发生病变时其血管壁失去弹性、脆性增加,本文患者右侧大脑中动脉管腔直径约为2.50mm,选择的球囊扩张支架规格为2.25mm,在支架释放过程中,由于过度牵拉而引起血管壁撕裂出血。另外,本文患者为中年女性,颅内血管狭窄的原因不十分明确,可能为非动脉粥样硬化性改变导致的管壁脆性增加、出血,采用球囊局部压迫止血并获得成功,从而防止了灾难性后果的发生。但患者术后2个月复查时,DSA发现右侧大脑中动脉破裂出血处形成假性动脉瘤,此为颅内动脉瘤的特殊类型,因不具有弹性纤维或平滑肌细胞等完整的血管壁结构,发生破裂出血的风险极高。血管内致密栓塞是治疗颅内假性动脉瘤的主要方法之一,通过隔绝假性动脉瘤与正常血管腔之间的通道而使动脉瘤逐渐萎缩,同时保持载瘤血管通畅。采用弹簧圈致密填塞瘤腔,同时结合支架重建血管壁可最大限度地减少复发、提高治愈率。本文患者假性动脉瘤的形成考虑与手术创伤有关,二次手术中,我们采用LVIS自膨式密网支架辅助进行动脉瘤致密填塞,有效实现了损伤血管的管腔内重建且未影响其他穿支血管的血流,取得了较好的治疗效果。
支架成形术是治疗症状性颅内动脉粥样硬化性重度狭窄的重要方法之一,术中引起的血管破裂可通过球囊封闭进行补救,而手术创伤导致的假性动脉瘤以弹簧圈致密填塞治疗为宜。
原始出处:
李广文,孙玉杰,刘彤晖,张勇.LVIS支架辅助弹簧圈栓塞治疗大脑中动脉支架成形术后假性动脉瘤一例[J].中国现代神经疾病杂志,2019,19(10):771-774.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#LVIS支架#
31
#成形术#
25
#弹簧圈栓塞#
37
#大脑中动脉#
25
#假性动脉瘤#
33