2019肿瘤免疫治疗十大事件盘点
2020-01-05 丁丁伴你行 丁丁伴你行
近几年,肿瘤免疫治疗百花齐放,2018年更是“肿瘤免疫治疗的元年”,从当年的诺贝尔生理学或医学奖授予了肿瘤免疫疗法开拓者,到免疫联合化疗首次在小细胞肺癌中获得成功,再到我国国家药品监督管理局(NMPA)批准了进口免疫治疗药物“K药”和“O药”上市,免疫治疗走进了大众,更有众多的肿瘤患者把免疫治疗药物当成“神药”。但实际上,就目前而言,肿瘤免疫治疗适用的人群及有效率仍然有限,将其当做万能的“神药”还
近几年,肿瘤免疫治疗百花齐放,2018年更是“肿瘤免疫治疗的元年”,从当年的诺贝尔生理学或医学奖授予了肿瘤免疫疗法开拓者,到免疫联合化疗首次在小细胞肺癌中获得成功,再到我国国家药品监督管理局(NMPA)批准了进口免疫治疗药物“K药”和“O药”上市,免疫治疗走进了大众,更有众多的肿瘤患者把免疫治疗药物当成“神药”。
但实际上,就目前而言,肿瘤免疫治疗适用的人群及有效率仍然有限,将其当做万能的“神药”还为时尚早。不过,任何一款药物的研发都是艰难曲折的,需要不断的探索,肿瘤免疫治疗的潜力还没有被我们完全挖掘出来,或许未来免疫疗法能够不断延长肿瘤患者的生命,真正地将肿瘤变成“慢性病”。
2019年即将过去,在这一年,多款免疫治疗药物的最新临床数据先后公布,小编梳理了今年免疫治疗的最新进展,盘点了十个值得关注的事件或进展。
1首个三阴性乳腺癌免疫治疗方案获批!3月8日,美国FDA加速批准了全球首个用于三阴性乳腺癌免疫治疗的药物——Tecentriq(atezolizumab,阿特珠单抗)联合化疗(Abraxane[白蛋白结合型紫杉醇],nab-paclitaxel),用于一线治疗PD-L1表达阳性且无法切除的局部晚期或转移性三阴性乳腺癌。
该治疗方案的获批是基于一项多中心、随机、双盲的III期研究IMpassion130的数据,这也是在三阴性乳腺癌患者中开展的首个阳性III期免疫治疗疗法研究。研究结果显示“与安慰剂组相比,atezolizumab联合化疗方案显著降低疾病进展和死亡风险,联合治疗方案的中位无进展生存期(PFS)为7.2个月,而安慰剂加化疗方案仅5.5个月。此外,在PD-L1表达阳性的三阴性乳腺癌中,患者获益会更大:中位总生存期(OS)从15.5个月延长至25个月”。
值得一提的是,该药目前已经在国内提交了申请,尽管申请的首个适应症为肺癌,但相信不用很久,国内的三阴性乳腺癌患者也可以用上这个治疗方案。
2肝癌双免疫疗法:“O+Y”强强联合,二线有效率31%11月11日,百时美施贵宝(BMS)宣布,美国FDA已经接受免疫治疗药物PD-1单抗 Nivolumab(Opdivo,俗称“O药”)联合CTLA4抑制剂 Ipilimumab(Yervoy,伊匹木单抗)的补充生物制剂许可申请(sBLA),并授予突破性疗法的称号,用于治疗既往接受过索拉菲尼治疗的晚期肝癌(HCC)患者。预计审批结论日期为2020年3月。
该申请主要是基于一项名为CheckMate-040的临床1/2期研究结果,这是一项开放、多中心的临床研究,旨在评估纳武利尤单抗(O药)或以纳武利尤单抗为基础的联合治疗方案治疗晚期肝癌的疗效和安全性。这也是迄今为止中位总生存(mOS)唯一达到终点的临床研究。
根据纳武利尤单抗(O药)和伊匹木单抗剂量的不同,研究中将患者随机分为3组:A组(纳武利尤单抗 1mg/Kg联用伊匹木单抗 3mg/Kg,每3周1次的用药频率,在连续用药4个周期后,序贯纳武利尤单抗 240mg,序贯用药频率为2周1次)、B组(纳武利尤单抗 3mg/Kg联用伊匹木单抗 1mg/Kg,每3周1次的用药频率,在连续用药4个周期后,序贯纳武利尤单抗 240mg,序贯用药频率为2周1次)、C组(纳武利尤单抗 3mg/Kg,每2周1次用药,联用伊匹木单抗 1mg/Kg,每6周1次用药)。
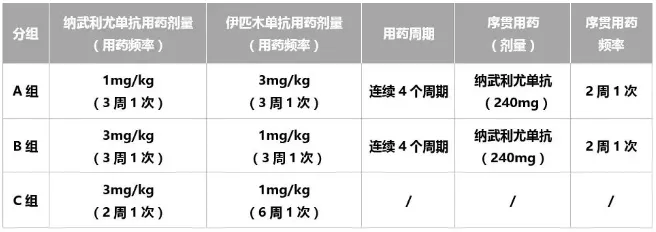
研究结果显示:无论PD-L1表达水平如何,所有治疗组患者均从中获益,观察到客观缓解。生存期方面,其中A组中位总生存期(mOS)最长,达到了22.8个月(95% CI: 9.4, N/A),30个月总生存率高达44%(95% CI: 29.5, 57)。B、C组的mOS分别为12.5和12.7个月。在疾病控制率(DCR)方面,A、B、C组分别为54%、43%和49%。另外,该组合疗法带来了31%的总体客观缓解率(ORR),其中5%获得完全缓解,26%获得部分缓解;中位缓解持续时间(mDoR)为17.5个月(95% CI:11.1,N/A)。而在安全性方面,研究结果显示安全性可控,在所有治疗组中,均未观察到新的安全信号。
3国产PD-1联合FOLFOX4或GEMOX方案一线治疗晚期肝癌,DCR为79.4%今年的ASCO会议上公布了一项由中国专家秦叔逵教授作为主要研究者牵头开展的研究——国产PD-1卡瑞利珠单抗(3 mg/kg,静滴),联合经典的FOLFOX4方案(氟尿嘧啶+亚叶酸钙+奥沙利铂)或GEMOX方案(吉他西滨+奥沙利铂)作为一线方案治疗晚期HCC(肝癌)或BTC(胆管癌)的临床研究。
这是一项正在进行的前瞻性、单臂、多中心的II期临床试验,纳入未接受过系统治疗的晚期HCC(共34例,其中27例HBV阳性)和BTC(共47例,其中17例HBV阳性)患者,给予卡瑞利珠单抗联合FOLFOX4方案或GEMOX方案治疗。结果显示,在34例可评估的HCC患者中,确认的ORR为26.5%,DCR为79.4%,中位PFS为5.5个月,中位缓解持续时间(mDoR)尚未达到。在32例可评估的BTC患者中,确认的ORR为9.4%,DCR为90.6%,中位PFS尚未达到,中位缓解持续时间(mDoR)为5.3个月。在中位总生存期(OS)方面,两者均未达到。
4 K药用于NSCLC治疗,5年生存率可达29.6%该数据是基于今年美国临床肿瘤学会(ASCO 2019)公布的KEYNOTE-001的5年生存随访数据。这是第一项评估抗PD-1药物Pembrolizumab(英文商品名Keytruda,中文名帕博利珠单抗,俗称“K药”)用于初治或经治晚期非小细胞肺癌(NSCLC)疗效和安全性的Ib期试验。
试验结果显示:针对初治患者,使用Keytruda作为一线药物,总的五年生存率平均为23.2%,其中:PD-L1 1%-49%(52名患者)的5年生存率为15.7%;PD-L1 ≥50%(27名)的患者五年总生存率高达29.6%。
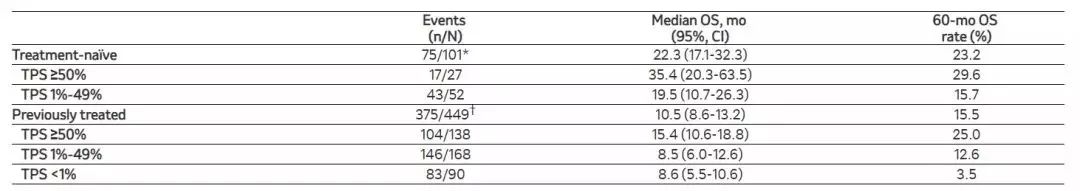
 针对经治患者,使用Keytruda作为二线及后线药物,平均五年总生存率为15.5%。其中:PD-L1 <1%(90名)的5年生存率为3.5%;PD-L1 1%-49%(168名)的患者中,5年OS率为12.6%;PD-L1≥50%(138名)的患者五年生存率高达25.0%。
针对经治患者,使用Keytruda作为二线及后线药物,平均五年总生存率为15.5%。其中:PD-L1 <1%(90名)的5年生存率为3.5%;PD-L1 1%-49%(168名)的患者中,5年OS率为12.6%;PD-L1≥50%(138名)的患者五年生存率高达25.0%。
PACIFIC研究是一项随机、双盲、安慰剂对照的III期临床研究,研究共入组了713例不可手术切除的III期NSCLC同步放化疗后未进展的肺癌患者,随机分组进行PD-L1单抗Imfinzi(durvalumab)或安慰剂治疗。2017年ESMO大会上公布的研究结果显示,Imfinzi 显著延长 PFS 超过 11 个月(16.8 个月 vs 5.6 个月;HR=0.52;95%CI:0.42-0.65),相比放化疗,durvalumab巩固治疗降低了32%的死亡风险。
在2019年的ASCO大会上,PACIFIC研究又公布了最新的研究数据,其3年总生存率达到57%(安慰剂组为43.5%),并且预期5年总生存率可达50%,这意味着该药有望让近50%的III期不可切除的NSCLC患者实现“临床治愈”。
基于PACIFIC的研究数据,2018年2月,该药获美国FDA批准用于治疗III期不可手术切除,接受初始放化疗后无进展的局部晚期非小细胞肺癌(NSCLC)患者。
且值得一提的是,该药在近日(12月9日)获我国药品监督管理局批准上市,用于治疗同步放化疗后未进展的不可切除的III期非小细胞肺癌(NSCLC),这也是国内首个上市的PD-L1单抗。
6 肺癌双免疫,“O+Y”一线治疗获阳性结果!在今年的ESMO大会上,公布了一项名为Checkmate227的临床研究的第一部分最终结果,这项研究评估了 Nivolumab(Opdivo,俗称“O药”)联合Ipilimumab(Yervoy,伊匹木单抗)用于一线治疗晚期非小细胞肺癌(NSCLC)患者的疗效。

研究结果显示:与化疗相比,该联合治疗方案在PD-L1≥1%的患者中总生存获益显著 [HR 0.79; 97.72% (CI): 0.65 至 0.96)]。另外,在探索性分析中发现,对于PD-L1 <1%的患者,“O药”联合低剂量伊匹木单抗能改善患者的总生存 [HR 0.62; 95% CI: 0.48 至 0.78]。双免疫治疗组的2年生存率在PD-L1≥1%与PD-L1<1%的人群中均为40%,而化疗相对应的2年生存率则分别为33%和23%。
“O药”联合低剂量的伊匹木单抗达到了研究的独立共同主要终点,即PD-L1≥1%的患者中的总生存(OS)期。这也是首个显示与化疗相比,双免疫方案用于非小细胞肺癌一线治疗能给患者带来显著生存获益的临床研究。
7 K药获批单药用于晚期食管癌的治疗!7月31日,默沙东(MSD)宣布Keytruda获得FDA批准,作为治疗复发性局部晚期或转移性食管鳞状细胞癌患者的单一疗法,这些患者的肿瘤表达PD-L1(综合阳性评分[cps]≥10),既往在一线或多线系统治疗后疾病仍然进展。该适应症的获批,使keytruda成为目前首个获批用于治疗复发局部晚期或转移性食管鳞状细胞癌患者的抗PD-1疗法,为患者提供了一个重要的新的单药治疗方案。
本次的获批是基于KEYNOTE-181和KEYNOTE-180的研究数据,KEYNOTE-181研究结果表明,在具有PD-L1表达的食管鳞状细胞癌(cps≥10)中,接受keytruda治疗的中位生存期(OS)为9.3个月,而接受化疗方案治疗组为6.7个月,死亡风险降低31%,差异达到统计学意义(HR 0.69;P=0.0074)。18个月的OS率也更优,为26%,化疗组为11%。
KEYNOTE-180是一项多中心、非随机、开放标签的试验,入组了121例局部晚期或转移性食管癌患者,这些患者在既往接受至少两次晚期食管癌全身治疗期间或之后发生疾病进展。除了先前的治疗线数外,合格标准与KEYNOTE-181相似,给药剂量方案相同。根据RECIST v1.1,主要疗效观察指标为ORR和DoR。试验结果显示,35例表达PD-L1(cps≥10)的食管鳞状细胞癌患者的ORR为20%。在7例缓解患者中,DoR范围为4.2至25.1+ 个月,5例患者(71%)的缓解时间为6个月或更长,3例患者(57%)缓解时间为12个月或更长。
8 K药联合Niraparib(尼拉帕利)治疗铂耐药卵巢癌,控制率67%在今年的ASCO大会上报道了一项名为TOPACIO的研究,这是一项PARP抑制剂niraparib(Zejula)联合K药治疗铂耐药复发卵巢癌的I、II期临床试验。该研究I期和II期分别入组14例(9例卵巢癌、5例TNBC)和53例卵巢癌患者。共62例卵巢癌患者(中位年龄60岁)。其中45%的患者既往接受过三线或以上治疗,97%的患者既往接受过紫杉类药物治疗,63%的患者接受过贝伐珠单抗治疗,29%的患者对铂类原发耐药。大多数的患者(73%)未携带BRCA突变。11名患者有BRCA突变, 6名有未知BRCA状态。同源重组缺陷(HRD)检测结果为22例患者为阳性,31例为阴性,9例未知。

结果显示,总人群ORR(客观缓解率)为24%,DCR(疾病控制率)为67%,并且患者的疗效与标志物的状态无关,即无论患者是否存在BRCA基因突变和HR功能缺陷,其有效率和疾病控制率均相似。
9 膀胱癌:靶向+免疫一线治疗,有效率高达71%在今年的ESMO大会上,公布了一项名为EV-103的研究,这是一项针对“enfortumab vedotin + K药一线治疗无法耐受铂类的晚期尿路上皮癌患者”的研究,这也是一个新的联合治疗方案。
enfortumab vedotin是在2018年3月上市的一种用于治疗膀胱癌的ADC型药物,药物共有两种成分,微管破坏剂MMAE和抗Nectin-4单克隆抗体连接。而K药在此前即已获批用于局部晚期或转移性尿路上皮癌的一线治疗。它们两者联用会有什么样的效果呢?EV-103(NCT03288545)研究结果显示:其有效率高达71%、疾病控制率高到93%,其中13%的患者出现完全缓解。
10 O药联合瑞戈非尼治疗MSS型胃癌/结直肠癌有效率40%,疾病控制率高达88%今年的ASCO大会上报道了一项来自日本的Ib期REGONIVO研究,这是一项采用瑞戈非尼联合纳武利尤单抗(俗称“O药”)治疗微卫星稳定(MSS)型晚期胃癌和结直肠癌的研究。研究共纳入了50例晚期胃癌或结肠癌患者(胃癌和结肠癌各25例),均是2线及以上治疗失败,入组后接受O药+瑞戈非尼治疗。
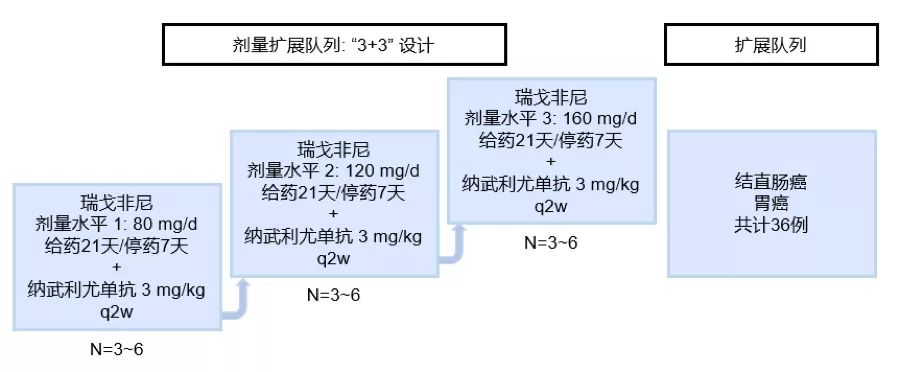
(REGONIVO研究设计,本图来源“肿瘤资讯)
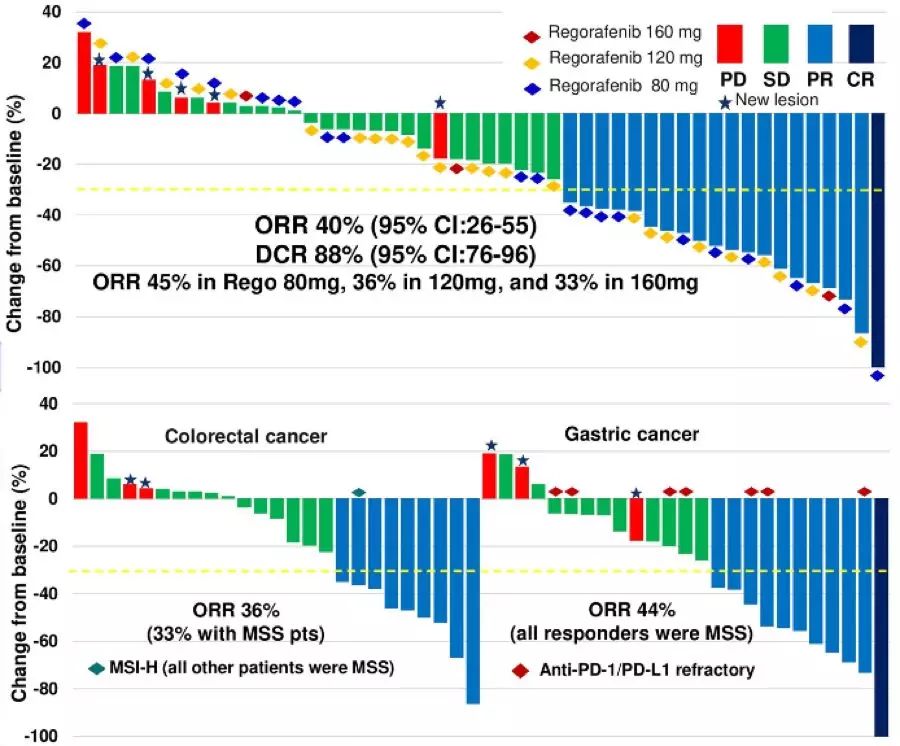
(REGONIVO研究ORR结果,本图来源“肿瘤资讯)
研究发现总体ORR达到40%,DCR高达88%,其中肠癌组的ORR达到36%,MSS(微卫星稳定型)肠癌患者的ORR为33%;胃癌组的ORR为44%。总体中位PFS为6.3月,肠癌的中位PFS为6.3月,胃癌的中位PFS为5.8月。对于多线治疗失败的患者而言,这样的疗效可谓是新希望。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言