AACR 2020:索凡替尼联合特瑞普利单抗治疗晚期实体瘤Ⅰ期研究结果公布
2020-05-01 MedSci MedSci原创
2020年美国癌症研究协会(AACR)年会由线下转为线上,于4月27日-28日和6月22日-24日分两次举办。会议期间,北京大学肿瘤医院陆明教授代表其研究团队公布了和黄医药自主研发的口服酪氨酸激酶抑制
2020年美国癌症研究协会(AACR)年会由线下转为线上,于4月27日-28日和6月22日-24日分两次举办。会议期间,北京大学肿瘤医院陆明教授代表其研究团队公布了和黄医药自主研发的口服酪氨酸激酶抑制剂(TKI)索凡替尼(surufatinib)联合特瑞普利单抗(toripalimab,针对PD-1的人源化lgG4型单克隆抗体)治疗晚期实体瘤的Ⅰ期临床研究结果(Abstract # 9563)。

研究发现,在肿瘤发生发展过程中,异常血管生成与肿瘤的进展、转移、免疫逃逸和耐药密切相关[1,2],抗血管生成治疗能够阻断肿瘤获取养分,“饿死”肿瘤。然而,抗血管治疗也会有“失利”的时候,即有些肿瘤患者会发生抗血管治疗耐药。近年来有研究发现,集落刺激因子-1受体(CSF-1R)能够使肿瘤相关巨噬细胞(TAM)向M2型(参与免疫抑制、促瘤作用)极化,调节肿瘤微环境至免疫抑制状态,导致肿瘤细胞成功实现“逃逸”。可见,在抗肿瘤过程中,扭转肿瘤微环境的免疫抑制状态,对于更有效地抑制肿瘤发展至关重要。
索凡替尼是一种新型口服酪氨酸激酶抑制剂(TKI),具有抗血管生成和免疫调节双重活性,其作用机制是:通过抑制血管内皮生长因子受体(VEGFR 1/2/3)和成纤维细胞生长因子受体(FGFR 1)来抑制肿瘤新生血管生成;还可通过抑制CSF-1R,减少M2型TAM,促进机体对肿瘤细胞的免疫应答(图1)。
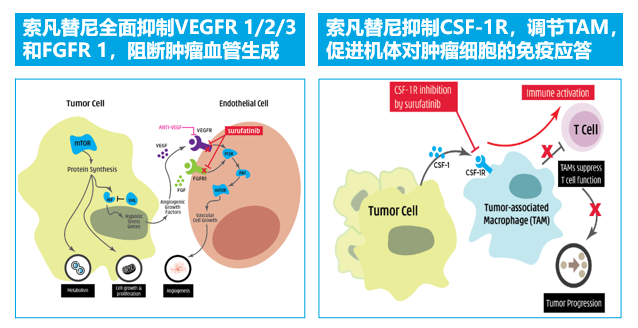
图1 索凡替尼的抗肿瘤双重作用机制
体外实验显示,索凡替尼抑制各靶点的半抑制浓度(IC50)低,意味着索凡替尼与各靶点高特异性结合,抑制作用强,抗肿瘤疗效强(图2)[3]。
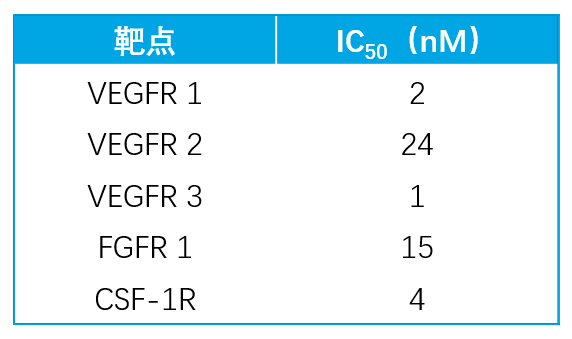
图2 索凡替尼抑制各靶点的IC50
基于独特的抗肿瘤双重机制,索凡替尼具有全面的抗肿瘤活性。多项正在进行的临床试验均证实,索凡替尼在神经内分泌肿瘤、胆道癌以及其他多种实体瘤(包括胃癌、甲状腺癌、非小细胞肺癌等)颇具潜力的疗效及良好的安全性。
除了单药治疗,索凡替尼与免疫治疗的联合应用也在探索中。动物实验显示,在小鼠肠癌CT26模型中,与单独用药相比,索凡替尼联合PD-L1或PD-1单抗均可增强抗肿瘤疗效,延长小鼠生存时间[4]。
基于上述,为此项Ⅰ期临床研究(索凡替尼联合特瑞普利单抗治疗晚期实体瘤)的开展奠定了基础,索凡替尼与特瑞普利单抗联合应用在晚期实体瘤中具有一定的应用潜力。
研究方法
研究的主要终点是评价索凡替尼联合特瑞普利单抗首次给药后28天内的剂量限制毒性(DLTs),以探索最大耐受剂量(MTD),确定Ⅱ期推荐剂量(RP2D)。次要终点为评估治疗的客观缓解率(ORR)、无进展生存期(PFS)、总生存期(OS)和疾病控制率(DCR),并测定索凡替尼和特瑞普利单抗的药代动力学(PK)。
剂量爬坡队列(n=16)采用传统的“3+3”剂量递增设计(索凡替尼150mg/200mg/300mg口服,每日1次),确定MTD;剂量扩展队列(n=14)(索凡替尼200mg/250mg/300mg口服,每日1次),进一步评估联合方案的安全性和疗效(图3)。
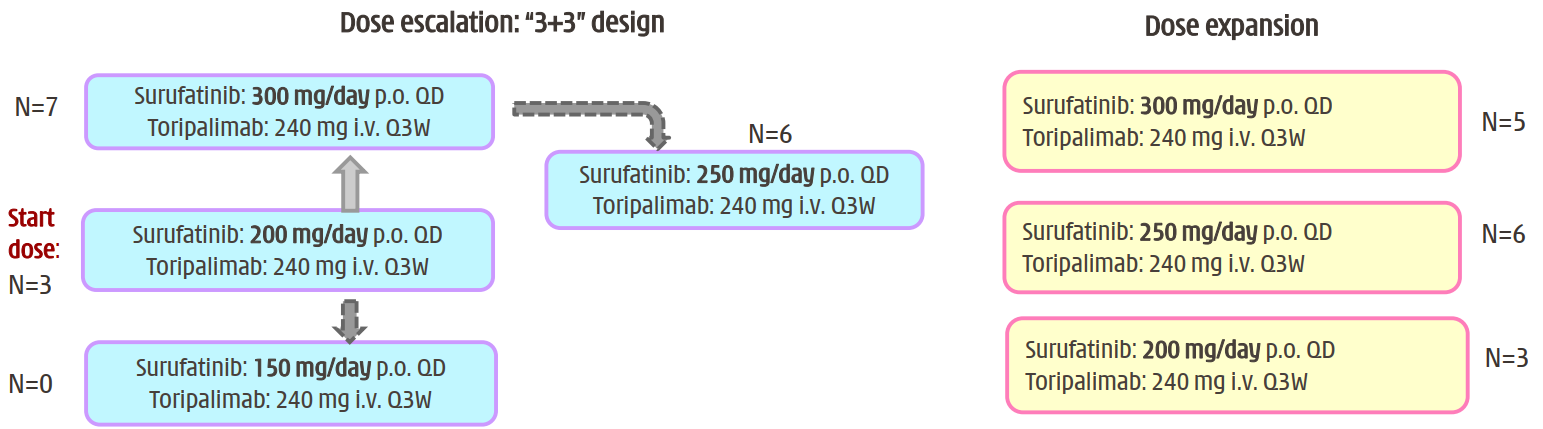
图3 研究设计
研究结果
研究纳入的瘤种类型多,患者人群范围广:截至2020年4月10日,研究共纳入30例晚期实体瘤患者,大多数为神经内分泌肿瘤(neuroendocrine neoplasms,NENs),包括神经内分泌瘤(neuroendocrine tumor,NET)和神经内分泌癌(neuroendocrine carcinoma,NEC)。此外还囊括结直肠癌(colorectal carcinoma,CRC)、胃癌(gastric adenocarcinoma,GC)、食管鳞癌(esophageal squamous cell carcinoma,EC)和转移性鳞状细胞癌(metastatic squamous cell carcinoma,MSCC)多个瘤种(图4)。其中,NET 8例(G1/G2级4例,G3级4例)、NEC 13例、CRC 4例(其中1例为伴高度微卫星不稳定[MSI-H])、GC 2例、EC 2例、MSCC 1例。
患者均为既往标准治疗无效或无有效治疗方案的不可切除的转移性或局部晚期癌症患者,接受过多线治疗,其中7例接受过抗血管生成治疗,但都未接受索凡替尼或免疫检查点抑制剂治疗。
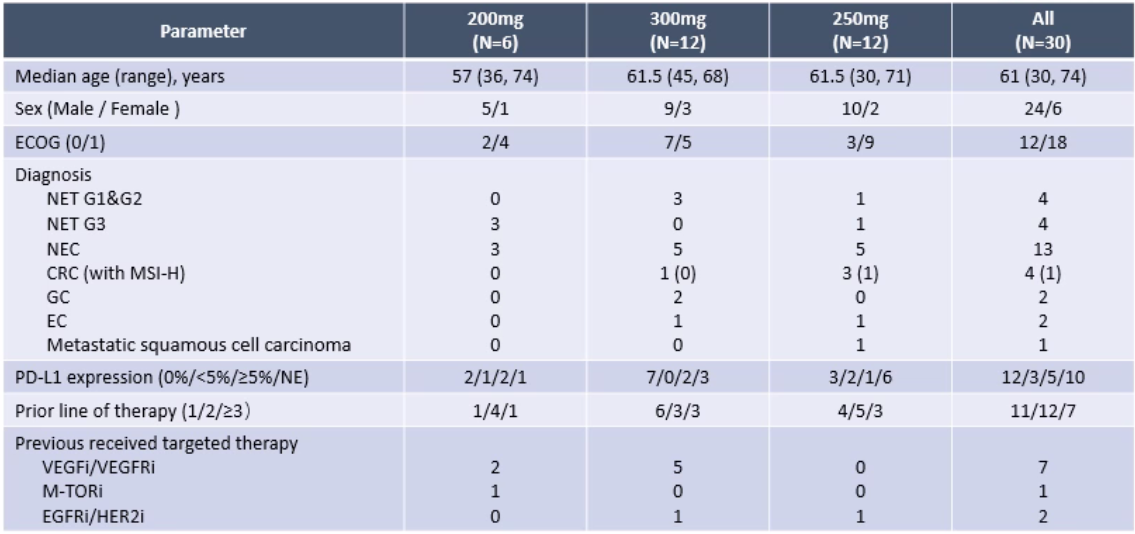
图4 入组患者的基线特征和疾病诊断情况
索凡替尼(250mg)联合特瑞普利单抗具有良好的安全性和耐受性。索凡替尼250mg剂量组的≥3级治疗相关不良事件(TEAEs)发生率低于300mg组(25.0% vs 58.3%)。剂量调整后,索凡替尼250mg组的TEAEs显著低于200mg和300mg组(33.3% vs 83.3% vs 58.3%)。
索凡替尼(250mg)联合特瑞普利单抗在各个实体瘤中都具有显著的抗肿瘤活性。在29例可评估的患者中,总体DCR为79.3%,ORR为34.5%。与200mg、300mg相比,索凡替尼250mg剂量组患者的生存获益更好(DCR:100% vs 50% vs 75%;ORR:63.6% vs 16.7% vs 16.7%),NENs患者的获益尤其显著,此外还有1例EC、1例CRC和1例MSCC患者获得PR(图5)。目前,30%(10/30)的患者仍在治疗中。
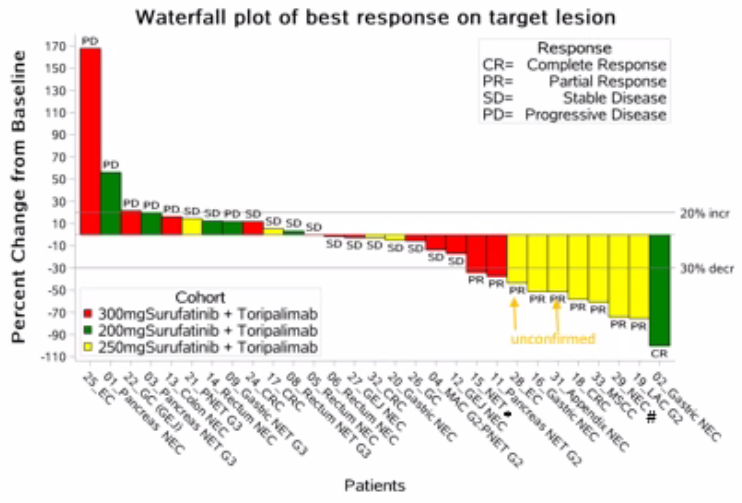
图5 目标病灶最佳反应瀑布图
总结
总体来看,对于晚期实体瘤,尤其是NENs患者,索凡替尼联合特瑞普利单抗具有令人鼓舞的抗肿瘤活性,且耐受性良好,没有观察到预期外的安全信号。Ⅰ期研究得出,索凡替尼RP2D为250mg/天。目前,索凡替尼联合特瑞普利单抗治疗实体瘤的Ⅱ期多中心临床研究(NCT04169672)已启动,研究结果值得期待。
陆明教授研究解读
从实验室到临床:验证索凡替尼与特瑞普利单抗协同抗肿瘤作用
近年来,免疫治疗在肿瘤研究领域取得重大进展。目前,通过PD-L1、肿瘤突变负荷(TMB)和微卫星状态等生物标志物寻找免疫治疗获益的潜在人群是研究热点。然而这部分获益人群仅约占所有肿瘤患者的20%,其余约80%的患者接受免疫治疗能否获益,如何获益,是临床的重要探索方向。
除了肿瘤自身,肿瘤微环境也会影响机体免疫功能。如何通过调节肿瘤微环境的免疫细胞(包括淋巴细胞和巨噬细胞等)功能,改善免疫抑制状况,从而增强免疫检查点抑制剂的疗效,是目前国内外临床共同关注的问题。而PD-1单抗联合其他疗法,包括抗血管治疗、化疗以及其他靶向药物,有望解决这一难题。
目前,PD-1单抗联合小分子抗血管药物是最有前景的治疗方案之一。索凡替尼是一种具有抗血管生成-免疫调节双重抗肿瘤作用机制的新型口服TKI,一方面可以通过抑制VEGFR 1/2/3和FGFR 1阻断肿瘤血管生成;另一方面还能抑制CSF-1R,通过调节TAM,促进机体对肿瘤细胞的免疫应答。日本的REGONIVO研究中,瑞戈非尼也是一种口服多靶点的多激酶抑制剂,与纳武利尤单抗联合表现出协同抗肿瘤效果。
研究者猜测,索凡替尼/瑞戈非尼联合PD-1/PD-L1单抗的协同作用可能与CSF-1R靶点有关。在肿瘤微环境中,CSF-1能够与其招募来的TAM表达的CSF-1R结合,抑制免疫细胞对肿瘤的识别和免疫反应。抑制CSF-1能够解除TAM导致的免疫抑制,改善PD-1单抗治疗效果,增强整体的抗肿瘤疗效。临床前研究显示,索凡替尼联合PD-1单抗的疗效显著优于单药治疗。基于此,研究者将这种联合方案投入临床试验,即本项Ⅰ期临床研究——这是一个从实验室到临床的探索过程。
研究人群范围更广泛,探索抗血管联合免疫治疗在更多类型患者中的疗效
与此项研究类似,REGONIVO研究也是抗血管联合免疫治疗用于实体瘤的研究,但其结果的重复性还有待验证。我们会参考REGONIVO研究,但未来并不考虑与之进行对比。抗血管与免疫治疗联合的协同机制尚未研究透彻,还需进行更多的临床试验加以探索。
在入组人群方面,REGONIVO研究纳入的是既往接受过治疗的晚期GC和CRC患者。与REGONIVO研究相比,本研究患者人群覆盖范围更广泛,包括NET、NEC、CRC、GC、EC和MSCC。
以Ⅰ期研究结果为基,对Ⅱ期研究充满信心
此项Ⅰ期研究的研究目的包括两方面。第一,确定RP2D,选择疗效最佳的索凡替尼剂量强度。第二,初步观察索凡替尼与特瑞普利单抗联合方案在各种晚期实体瘤中的治疗效果。
研究分为索凡替尼200mg、250mg和300mg三个剂量组。在安全性方面,索凡替尼250mg剂量组的TEAEs发生率更低,患者在≥3级TEAEs和剂量调整后的TEAEs发生方面均表现出较好的耐受性在疗效方面,索凡替尼250mg组的疗效良好,7例患者达到PR,包括NEC、EC、MSCC、CRC和肺非典型类癌(LAC)。基于以上数据,索凡替尼250mg可作为Ⅱ期研究的推荐剂量。尽管Ⅰ期研究纳入患者的数量较少,但所获得的结果为后续Ⅱ期研究提供了很多参考,也增强了研究者开展Ⅱ期研究的信心。
期待进一步研究为联合方案临床可行性增添证据
本项Ⅰ期研究结果的公布令人振奋,在治疗安全性和适应证方面为下一步的Ⅱ期扩大样本量研究提供参考。目前,索凡替尼联合特瑞普利单抗治疗晚期实体瘤的全国多中心Ⅱ期临床研究已经启动,并开始陆续入组患者,期待Ⅱ期研究能够就该方案的临床可行性提供更多的证据。
本项Ⅰ期研究结果证明,索凡替尼与特瑞普利单抗联合应用,具有显著的抗肿瘤疗效。既往在肝癌、黑色素瘤等肿瘤中的研究也证实,免疫微环境调节相关的靶向药物与免疫治疗联合应用,能够发挥1+1>2的抗肿瘤活性。这为靶向+免疫治疗应用于肿瘤领域提供了更多的思路。然而目前临床对于二者联合的协同抗肿瘤机制认识尚不全面,还需更多的基础研究进行深入探索。
初步探索取得成果,扩大样本量Ⅱ期研究稳步推进
此项研究最大的局限性在于,Ⅰ期研究只是探索性研究,主要是为后续研究做准备。下一步研究计划是进行扩大样本量的Ⅱ期临床研究,主要观察联合治疗的疾病控制情况和患者生存时间。目前已在国内5家研究中心已经启动,有望很快完成患者入组。
参考文献:
1. Naveen SV et al. Angiogenesis 2014;17:471-4942. Shom Goel et al. Physiol Rev 2011;91(3):1071-11213. Xu JM, et al. Oncotarget. 2017 Jun 27;8(26):42076-42086.4. Jinghong Zhou, et al. Cancer Res 2017; 77(13 Suppl): Abstract nr 4187
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#结果公布#
29
#索凡替尼#会成为新一代#抗血管新生#类抗肿瘤药物吗?
193
#瑞普利单抗#
32
#研究结果#
27
#AACR 2020#
0
#ACR#
35
#晚期实体瘤#
31
#AACR#
36