PARP 抑制剂 Rubraca (rucaparib)一线治疗晚期卵巢癌,显著延长了PFS
2022-04-02 Allan MedSci原创
在 HRD 阴性患者的探索性亚组中,Rubraca 组患者的中位 PFS 为 12.1 个月,而安慰剂组为 9.1 个月。
卵巢癌是发源自女性卵巢的癌症,会产生会入侵以及转移到其他部位的异常细胞。卵巢癌初期症状不明显,随病情进展,才会出现许多癌症的典型症状,包括胀气、腹胀、骨盆痛等。癌症较容易扩散到腹膜、淋巴结、肺脏、肝脏等部位。
制药公司 Clovis Oncology 近日宣布,其 PARP 抑制剂 Rubraca (rucaparib) 在一线维持治疗晚期卵巢癌、输卵管癌或原发性腹膜癌时,与安慰剂相比,Rubraca (rucaparib) 显著延长了无进展生存期 (PFS)。
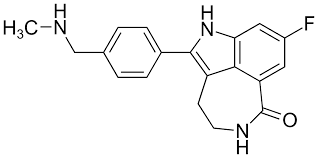
图1.PARP 抑制剂 Rubraca (rucaparib) 的分子式
这些积极数据来自于 III 期 ATHENA 研究的 ATHENA-MONO 部分,该试验正在研究 Rubraca 在一线卵巢癌维持治疗中的作用。具体来说,ATHENA-MONO 招募了 538 例患者,随机分配至 Rubraca 单药治疗组或安慰剂组。结果显示,Rubraca 治疗组的 HRD 阳性人群的中位 PFS 为 28.7 个月,而安慰剂为 11.3 个月,风险比 (HR) 为 0.47。同时,在研究中观察所有接受治疗的受试者时,Rubraca 组的中位 PFS 为 20.2 个月,而安慰剂组为 9.2 个月。
在 HRD 阴性患者的探索性亚组中,Rubraca 组患者的中位 PFS 为 12.1 个月,而安慰剂组为 9.1 个月。在 BRCA 突变肿瘤患者的探索性亚组中,Rubraca 组的中位 PFS 为未达到,而安慰剂组为 14.7 个月。关于安全性,Rubraca 组的停药率为 11.8%,而安慰剂组为 5.5%。
同时,阿斯利康和默克公司的 PARP 抑制剂 Lynparza(奥拉帕尼)于 2018 年获得美国批准,作为某些 BRCA 突变卵巢癌患者的一线维持治疗。葛兰素史克的 PARP 抑制剂 Zejula (niraparib) 于 2020 年在美国获得批准,用于晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌患者的一线维持治疗。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#抑制剂#
36
#ACA#
30
#rubraca#
0
#PARP抑制剂#
76
#CAP#
39
#APA#
32
#晚期卵巢癌#
42
#PFS#
35
#PARP#
32
学习了
0