PNAS:偶然突变的积累能减缓癌症发展
2013-02-07 生物无忧 PNAS
一个典型的癌细胞基因组中分散着成千上万的突变,有着数以百计的突变基因.然而,这些突变基因中只有一小部分被认为是癌症的驱动子,负责癌症特征的表现,例如不受控制的细胞生长.癌症生物学家们很大程度上忽略了其他突变,因为他们相信那些突变对癌症的进展发挥着微小的作用,甚至乎没有作用. 但是由麻省理工学院(MIT)、哈佛大学、Broad研究所和布莱根妇女医院的一项联合研究首次表明,这些偶然突变(passen
一个典型的癌细胞基因组中分散着成千上万的突变,有着数以百计的突变基因.然而,这些突变基因中只有一小部分被认为是癌症的驱动子,负责癌症特征的表现,例如不受控制的细胞生长.癌症生物学家们很大程度上忽略了其他突变,因为他们相信那些突变对癌症的进展发挥着微小的作用,甚至乎没有作用.
但是由麻省理工学院(MIT)、哈佛大学、Broad研究所和布莱根妇女医院的一项联合研究首次表明,这些偶然突变(passenger mutations)不只是凑热闹而已.当它们积累到一定程度,就能减缓甚至停止癌症的发展.
这一发现发表在本周的PNAS上,MIT物理和健康科学技术学院的Leonid Mirny副教授是这篇文章的资深作者.他说:我们的结果暗示,癌症应该被视为一个渐进的过程,它的进程由驱动子推动细胞生长与偶然突变逐渐累积破坏癌症之间的微妙平衡决定.
另外,研究者们认为,能够使局面有利于偶然突变的药物或许能为癌症治疗提供一种新的方法,即用癌症本身的武器“突变”来击败它自己.尽管单个偶然突变的影响是微不足道的,“但是从总体上看,它们可以产生深远的影响,”Mirny说,“如果一种药物可以让它们更有害点,每一个偶然突变的影响虽然很微小,但是集体的效应却可以建立.”
权力斗争
癌症的发展可以持续数年甚至数十年,在这一过程中,细胞会逐渐积累必要的驱动突变.这些突变通常激活促进细胞生长的致癌基因,如Ras,或关闭通常抑制细胞增长的肿瘤抑制基因,如p53.
偶然突变是伴随驱动子的突变而随机产生的,它们通常被认为是良性的:在自然群体中,自然选择清除了有害的突变.然而,Mirny和他的同事们怀疑,癌症的进化过程可能是不同的,它们允许带有极小有害效应的突变不断积累.
为了验证这一理论,研究人员创建了一个模拟癌症增长的计算机模型,随着癌症的发展过程,细胞获得了随机突变.这些模拟跟踪了数以百万计的细胞,调查了每个细胞的分裂、突变和细胞死亡.
他们发现,在获得驱动突变的较长周期内会出现许多偶然突变.当一个癌细胞获得一个新的驱动突变时,这个细胞及其后代在接收整个基因组时,也会带上那些初始细胞中的偶然突变.“否则这些突变不会蔓延到整个细胞群,”Mirny说,“他们基本上搭了驱动突变的便车.”
模拟研究发现:在癌症发展中,这个过程会重复五到十次;每一次都有新一波的破坏性偶然突变积累.如果有足够多的有害偶然突变,他们的累积效应就能减缓肿瘤的生长.肿瘤可能变成休眠状态,甚至退化,但是如果获得了新的驱动突变,细胞的增长又会再次启动.这种增长模式与人类癌症患者中常见的情况相吻合.
“癌症可能并不是由一系列不可避免的事件的积累造成,而很可能是由驱动突变与偶然突变之间的微妙平衡形成的.”Mirny说:“药物带来的自然康复或病征缓解实际上可能由有害偶然突变的负载介导.”
当他们分析癌症患者基因组中的偶然突变时,发现了与模型预测相同的结果——微小有害突变的大量积累.
扭转局势
利用计算机模拟,研究人员测试了增加有害突变来治疗肿瘤的可能性.在他们最初的模拟中,每一个有害的偶然突变会使细胞的健康下降约0.1%,当这一比例增加到0.3%时,肿瘤就会因负载了这些自身突变而缩小.
Mirny说,当用药物干扰已知的分子伴侣蛋白时,同样的效果也可以在真实的肿瘤中被发现.蛋白质合成后需要被折叠成正确的形状,而分子伴侣能够帮助蛋白实现这一过程.在癌细胞中,分子伴侣帮助蛋白质折叠成正确的形状,甚至当它们突变时也是如此,这有助于抑制有害突变的影响.
一些能够抑制分子伴侣蛋白的潜在药物现在已经被用于临床上对癌症的治疗,尽管研究人员只是相信,它们的主要功能是抑制驱动突变,而不是增强偶然突变的影响.
在这一研究中,研究人员比较了负载相同驱动突变和不同偶然突变的相同癌细胞系,看谁长得更快.他们还将癌细胞系注射到了小鼠的体内,看看哪个是最有可能转移.

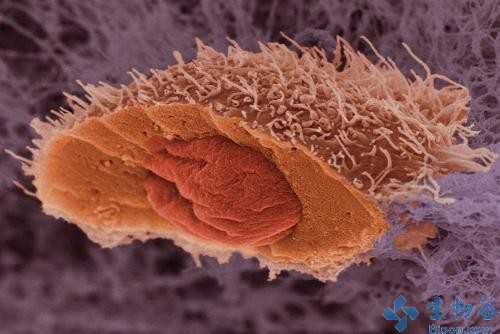
A scanning electron micrograph of a squamous cell carcinoma, a type of skin cancer. The cell has been frozen and split open to reveal its nucleus.
A typical cancer cell has thousands of mutations scattered throughout its genome and hundreds of mutated genes. However, only a handful of those genes, known as drivers, are responsible for cancerous traits such as uncontrolled growth. Cancer biologists have largely ignored the other mutations, believing they had little or no impact on cancer progression. But a new study from MIT, Harvard University, the Broad Institute and Brigham and Women's Hospital reveals, for the first time, that these so-called passenger mutations are not just along for the ride. When enough of them accumulate, they can slow or even halt tumor growth. The findings, reported in this week's Proceedings of the National Academy of Sciences, suggest that cancer should be viewed as an evolutionary process whose course is determined by a delicate balance between driver-propelled growth and the gradual buildup of passenger mutations that are damaging to cancer, says Leonid Mirny, an associate professor of physics and health sciences and technology at MIT and senior author of the paper. Furthermore, drugs that tip the balance in favor of the passenger mutations could offer a new way to treat cancer, the researchers say, beating it with its own weapon—mutations. Although the influence of a single passenger mutation is minuscule, "collectively they can have a profound effect," Mirny says. "If a drug can make them a little bit more deleterious, it's still a tiny effect for each passenger, but collectively this can build up." Lead author of the paper is Christopher McFarland, a graduate student at Harvard. Other authors are Kirill Korolev, a Pappalardo postdoctoral fellow at MIT, Gregory Kryukov, a senior computational biologist at the Broad Institute, and Shamil Sunyaev, an associate professor at Brigham and Women's.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#PNAS#
32