Neurology:协和医院:海马萎缩和血液中的A-beta如何受基因影响?
2022-07-30 Freeman MedSci原创
海马结构异常和β-淀粉样蛋白(Aβ)负担被认为是痴呆症进展的客观指标和阿尔茨海默病(AD)的有效内表型。一项欧洲人的全基因组关联研究(GWAS)发现,常见的遗传变异可以解释76%的
海马结构异常和β-淀粉样蛋白(Aβ)负担被认为是痴呆症进展的客观指标和阿尔茨海默病(AD)的有效内表型。一项欧洲人的全基因组关联研究(GWAS)发现,常见的遗传变异可以解释76%的海马体积(HV)变异。 海马体积的高遗传性和海马的关键功能使其成为遗传研究的重要对象,从而为相关疾病提供了机理上的见解。

图1: 论文封面图
最近,一些研究发现12q14和12q24内的单核苷酸多态性(SNPs)与不同欧洲社区队列中的海马体积变异显著相关。富集和基因水平分析发现参与神经发生的途径和基因(DPP4,MSRB3)与HV有关。
在最近的研究中,血浆Aβ也被发现与CSF Aβ相关,6-9并且可以预测痴呆症的风险。对血浆Aβ的遗传特征研究较少。一项研究表明,在晚期发病的AD血统中,血浆Aβ1-42和Aβ1-40的遗传率分别为0.74和0.54。早期的GWAS显示没有明显的结果,但最强相关基因CTNX3的蛋白产物可以在体外调节Aβ1-42的调节。最近的GWAS发现,主要AD基因(APOE、BACE1、PSEN2和APP)和ZNF397(以前曾报道参与CSF Aβ代谢)附近的变体与血浆Aβ明显相关。
尽管取得了上述成就,但对没有痴呆症的个体中血浆Aβ的遗传性以及血浆Aβ和HV等内涵型之间的遗传相关性的研究还很少。需要更多的分析来证实目前的发现并推测分子机制。大多数GWAS是在白人群体中完成的。这些发现在其他人群中是否有效还有待证明。尽管复杂性状的遗传特征受到了位于非编码区的常见SNPs的影响,但对这种遗传变异的解释是困难和有争议的。全外显子组测序(WES)在将结果与一个基因的分子和生理功能联系起来方面具有优势。
藉此,协和医院的朱以诚团队,利用WES和SNP阵列数据在一个中国社区队列的无痴呆老人中探索血浆Aβ和HV的遗传特征,为这些特征背后的分子机制提供可能的指示。
他们利用全外显子组测序和SNP阵列基因分型数据对海马体积和浆液Aβ进行了关联分析,混合效应线性回归模型对性别、年龄、颅内总体积或APOE ε4进行了调整,同时考虑了家族关系。
他们还对常见的变体进行了基因水平分析,对罕见变体进行了基因负担分析。进一步研究了遗传性和遗传相关性。
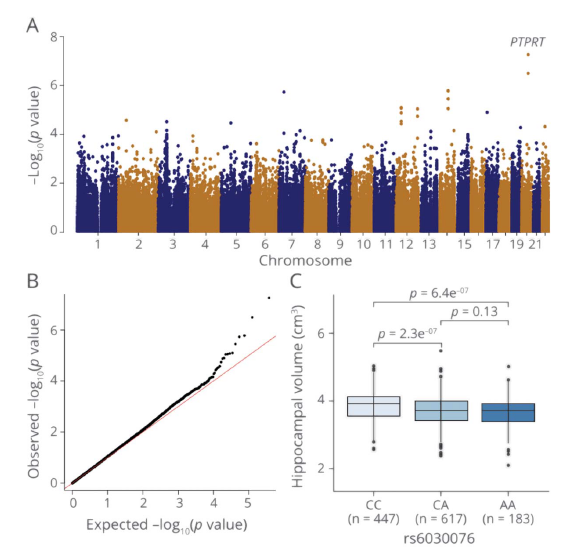
图2:论文结果图
通过全基因组关联研究,他们确定了海马体积的一个基因--PTPRT,其中最重要的SNPs是来自全外显子组测序的rs6030076(P=5.48×10-8,β=-0.092,SE=0.017)和SNP阵列数据的rs6030088(P=8.24×10-9,β=-105.22,SE=18.09),都位于该基因。
基于罕见突变的基因负担分析检测到6个基因与Aβ明显相关。基于SNP的海马体积遗传性为0.43±0.13,血浆Aβ的遗传性为0.2-0.3。
基于SNP的海马体积和血浆Aβ的遗传相关性为负。
该研究的重要意义在于:发现了几个SNPs和一个基因PTPRT,这在以前的GWASs中没有报道,与海马体积相关。此外,遗传性和遗传相关性给出了海马体积和血浆Aβ的概况。该研究结果提供了对这些内涵型的个体差异背后的机制的见解。
原文出处:
Yang XZ, Wan MY, Zhang DD, et al. Investigating the Genetic Characteristics of Hippocampal Volume and Plasma β-Amyloid in a Chinese Community-Dwelling Population. _Neurology_. 2022;99(3):e234-e244. doi:[10.1212/WNL.0000000000200554](https://doi.org/10.1212/WNL.0000000000200554)
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言




















#BET#
38
#Neurol#
32
#萎缩#
42
#协和#
37
#协和医院#
39