深度:新药受试者招募的喜与忧
2020-04-13 巴根 E药经理人
“2020年4月3日,迈入第二年。肺癌、双肺转移、骨转、脑转,确诊后一年了。最重要的不是时间,而是体感与生活质量!”从2019年4月4日父亲初诊肺癌以来,晓宁就一直在记录父亲的
“2020年4月3日,迈入第二年。肺癌、双肺转移、骨转、脑转,确诊后一年了。最重要的不是时间,而是体感与生活质量!”从2019年4月4日父亲初诊肺癌以来,晓宁就一直在记录父亲的抗癌生活。
今年27岁的晓宁和父母居住在浙江的一个县城。去年4月4日,一个普通的工作日,晓宁接到了母亲的电话:父亲上周肩膀疼,拍的CT结果出来了,可能是癌症!
2019年4月9日,PET-CT结果显示肺癌,而非之前猜测的骨癌,这让一家人多少松了口气,14年前,晓宁的爷爷患了肺鳞癌,经过手术和化疗之后痊愈,至今健在。但麻烦来了,父亲的情况不适合做手术,同时,做活检也存在难度,这意味着,分型分类和疗法都难以确定。
经过多次辗转检查,晓宁的父亲最终确诊为肺腺癌。一家人经过商量,决定使用一代靶向药。
“肺腺癌基因突变几率很大,可以吃靶向药,中西医结合效果不错的。免疫疗法复发概率比较高!”当被推荐参加临床试验时,晓宁表示,对于父亲所患的病症,晓宁查了不少资料。加上目前已有明确可用的疗法,靶向药纳入医保后价格也只有数百元,即使耐药也可以更换二代、三代产品,因而晓宁更愿意使用被验证的疗法。
但对于大量的中晚期癌症患者而言,传统疗法几无实效,加入创新药物的临床试验,成为生命中最后的稻草。
而在另一面,中国近二十年来临床试验的数量几乎每几年就翻一番,肿瘤患者日趋“稀缺”。以肺癌为例,每年新增患者的增速约为2%~3%,而大量正在研发中的新药,每一款都需要数百至数千的患者完成三期的临床试验,才有可能进入上市申报阶段。
“每找到100个肿瘤患者,可能同意参加并最终通过临床试验入排标准的只有一两个。”一位临床试验受试者招募从业人员告诉本刊记者。面对各种疑难杂症及绝症,创新药正在全球范围内被源源不断开发出来。但这些新药效果和安全性如何?需要严格的临床验证,方可按照相关法规上市。
01 十年翻五倍的临床试验
本刊记者在药物临床试验登记与信息公示平台搜索肺癌相关临床试验发现,目前中国进行中的相关临床试验数量达到322个,而2016年这一数字仅为135,年均增速在25%左右。
中国的临床研究起步晚于欧美国家。改革开放以来,通过国际间的学术交流与交往,国际上公认的药品临床试验管理规范(GCP)迅速引入我国,并经过约十年的推动与实施,于1999年9月1日我国自己的《药品临床试验管理规范(GCP)》才正式颁布执行。通过GCP的培训及其舆论宣传,越来越多的新药研究开发单位和临床研究机构开始认识和重视GCP。
2005年之前,制药外企率先在中国尝试开展国际多中心临床试验,2005年之后中国开展的临床研究数量较之前呈显著上升趋势,例如礼来的培美曲塞、辉瑞的舒尼替尼、勃林格殷格翰的噻托溴铵等都是在2005年左右在中国启动临床。
中国过去一直是仿制药大国,创新药完整链条的经验仍然较少,且因为政策的原因,此前跨国药企的临床试验到了二期才能进入中国。而今,创新药企如雨后春笋般创办成立,临床试验数量大大增加。2017年,中国加入了ICH,药品监管体系融入国际社会认可的监管体系中,并有更多的临床数据将得到认可。中国相较欧美更加低廉的试验成本、丰富的临床资源和逐渐成长的市场,也在吸引跨国药企将更多的临床试验放在中国。
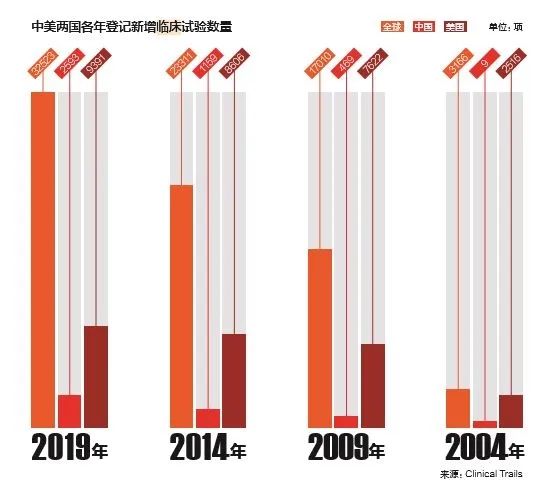
相对于2009年,2019年中国新增的临床试验翻了五倍。根据ClinicalTrial的数据,2004年全球新增临床试验登记3166例,其中中国仅为9例,美国为2516例,而到了2009年,全球新增临床试验登记17010例,其中中国469例,美国7622例,中国的新增临床研究占比从0.28%提高到2.76%,比例提升近10倍,而到了2014年和2019年这一比例分别提升至4.97%和7.97%。在这一平台搜索全球正在进行中的临床研究(招募和尚未开始招募),条目数共达到67727例,其中中国为6093例,美国为23994例。十余年间,中国的临床试验数量增长迅猛。
这同时也为中国患者带来了前所未有的新药。“我国自1985年开始实施药品登记注册办法,那时平均5年出一个新药,但2008~2018年就有44个1类新药上市,与此同时,新药出现的越来越快,2018年批准的1类新药就有10个。”国家新药研究和开发专家委员会委员、新药创制专项技术副总师陈凯先院士于2019年11月在一次公开场合中说道。
尽管中国是临床资源最为丰富的国家之一,但暴增的临床使得招募受试者的难度越来越大。“受试者招募过程中面临的挑战部分是由于大量类似试验同期招募所致。”武田亚洲开发中心负责人王璘指出,对于扎堆热门靶点的产品来说招募的挑战会更大,而武田等公司研发专注于区分度高的差异化产品,因而对招募公司的依赖较低。“国内的新药研发属于趋之若鹜型,每个PD-1都会选择肺癌适应证,造成患者分流,一遍一遍又一遍做一模一样的临床试验,导致竞争激烈。”厚普医药总经理王亚楠补充道。
相对于2%~3%增速的患者数量,以及不断被验证获批上市的新药,新药临床试验的增速是其数十倍,并且相同靶点的药品竞相开发,对于一些“热门癌种”的临床试验,找到合适的患者是一件极为头痛的事情。
02 为新药试验匹配患者
“我们不介入受试者招募工作。”王璘表示,作为制药企业不会直接参与受试者招募,“招募主要由参加临床试验的医院负责,我们的责任是帮助临床研究者深入了解试验方案以及入组标准,由研究者评估做出最终入组患者的决定。”自2015年来,武田已经在亚太地区(除日本之外)进行了约50项临床试验,其中有30多项是在中国进行的,而这都是由武田亚洲开发中心通过与CRO的合作共同完成的。
制药企业常常将临床试验外包于CRO进行。CRO帮助药企选择经过认证的“临床试验机构”(医院)以及“研究者”(医生),并共同设计制定临床试验方案,而做这项业务的一个关键是要拥有快速召集受试者来完成试验的能力。
“临床试验费用不由公司直接支付给受试者或医院,而是由CRO企业通过研究者基金的形式支付给医院的,我们在临床试验中的责任是全面执行和质量监管。”王璘表示。CRO向医院付“管理服务费”,并委托医院推荐“研究者”。研究者通常是医生,他们负责招募患者并进行临床试验。之后由CRO向受试者支付“营养费”并分发试验药物,同时监督试验的全过程。所有的试验数据,由医生交付CRO,以进行统计分析,CRO协助制药企业申报上市。
“我每周都会在医院的病历系统里筛查病人,一个月能够入组一个患者就是不错的情况了。”一位在某省肿瘤医院负责临床研究的医生告诉本刊记者,受试者的招募往往持续数月至数年。“一般会通过医院内张贴的大字报、招募公司、病历系统中寻找病人等方式寻找合适的受试者。”上述医生表示。
但仅仅依靠医生和线上线下的招募广告,已经不能满足日益增长的临床试验对数量和时间的要求,受试者招募公司应运而生。
相对于医生、大字报等传统招募方式,招募公司的优势就在于覆盖范围更广更易匹配患者。“小红书、抖音、微博、微信群都有他们招募的渠道。”一位新药研发人士表示,招募公司的一个价值在于能够“异地招募”受试者。由于中国的临床试验中心集中在北上广等少数大城市,而招募公司的半径能够通过线上、线下的方式触达周边城市,为更多合适的患者提供到使用新药的机会,也为新药临床试验加速度,补足申办方在受试者招募方面的短板。
“研究中心医生的触达半径基本只在本院,而招募公司能从河北招募到病人来北京。”上述新药研发人员表示。
晓宁接触到的临床试验信息基本来自于招募公司的招募专员。“一般招募专员的工作方式是通过医生来寻找,维护好医生关系,就能找到患者。”上述新药研发人士说道,招募专员通过其他非临床试验医院的医生获得患者资源,或者直接通过医院的系统来寻找患者,这是最为普遍的做法。
“2004年前后就有了招募公司,当时是以健康受试者为主。对于患者的招募,可以以资历最老的捷信诞生时间为标杆。”该新药研发人士告诉本刊记者,该公司算是行业的开拓者,也是老牌的招募公司,成立于2008年,据其官方简介,目前已经服务超过40个药品。该公司于2015年在新三板挂牌上市。到了2011年左右,大量的招募公司出现,他预估目前类似的公司至少有上百家。此外,有些大型制药企业也会选择自建招募队伍,例如恒瑞、正大天晴等,也有CRO集团业务扩大到招募公司,其中较为知名的有泰格旗下的思默。
但值得注意的是,对于新药研发企业来说,通过招募公司这种途径是最为昂贵的。“一个招募专员一个月可能就入一两个患者,一万块钱肯定不够。”上述业内人士表示,这其中的费用包括招募专员的提成、维护专家的费用以及受试者的补贴等等,成功招募一个患者的成本并不低。
但为何新药研发企业愿意使用这种昂贵的方式?“这是行业普遍的做法,也是招募患者的一个渠道。我们一个试验上可能会用不止一个招募公司。”百济神州副总裁汪来表示,“中国的临床临床资源其实很丰富,病人很多,但中国的问题是水平好的研究中心不多,所以往往这些中心临床试验扎堆,大家都在抢病人,尤其是肿瘤领域更激烈,这也是药企做临床试验的一个难点。”
而百济神州正是捷信医药最大的客户。2018年,捷信医药超过四分之一的收入来自于百济神州,捷信年报显示,2018年营业收入大增80.8%,达到5006万元,净利增长98.21%,达到337.54万元。默沙东、礼来、复星医药都是捷信的前几大客户。
但一个临床试验的受试者不可能完全依靠招募公司,制药企业往往在试验进度不达预期时启用这种招募方式,招募的主要责任仍然落在研究者身上。上述业内人士表示,速度是招募公司的优势之一,而一款新药的上市时间越来越成为决定其市场表现的重要因素。
在海外,美国临床研究信息机构Centerwatch统计了过去5年美国和欧洲的临床试验情况后,发现只有10%的临床试验能够按时完成入组,有1/3的临床试验机构能够最终招满受试对象,大约一半的机构被迫延长其招募周期。据不完全统计,在中国进行的抗癌药品及疗法,只有45%临床试验能按时找到受试者,完成入组。无论海内外,受试者招募都是令医药企业头痛的问题。
03 门槛被拉低
一位招募专员需要维护地区内或者专门领域内的诸多医生资源。“这些人大多来自于医药代表和CRC,因为他们通常都拥有医生资源。”一位曾在招募行业工作的业内人士表示。某招聘网站上,对于招募专员的工作职责也描述为“根据项目要求制定并落实区域工作计划,拜访医院及社区医生,传递临床研究项目信息,寻找合适的患者参加临床研究”,并表示“医药销售、临床、CRC经验优先”。
但不少招募公司认为只要维护好医生资源,就能进入这一行业。一时间,招募公司遍地开花。
随着涌入的公司越来越多,整个行业出现了分化。“大部分是关系型,其生存之道就是和某个领域的专家关系好,少部分企业是技术型,除了维护好专家关系,同时关注受试者招募的商业模式、战略规划以及病人的告知、受试者的引流、员工的培训、专家的鼓励等等,并帮助减少受试者脱落率。”上述新药研发人士表示,大量进入这个领域的企业拉低了行业门槛,他们缺乏对临床试验的敬畏和认知。
“由于没有相应的法律法规,很多人都认为这只是一个市场和生意。表面上这个事情没有门槛,注册个公司、考个GCP就可以做,但实际需要专业的临床经验知识。”王亚楠略显遗憾地说道。有些医生甚至被“宠坏了”,例如白介素-6相关的临床试验,由于哄抢患者,给医生的费用越来越高,造成了不良竞争,关系型企业挤兑专业的技术型公司。
据上述新药研发人士,招募行业甚至出现了垄断现象,申办方如果要在某医院进行临床,需要购买所在医院推荐的招募公司的服务,而院方则在申办方和招募公司两方“吃利”;此外还有招募公司怂恿患者隐瞒病史、伪造病例,教予话术以通过入组标准,而这终将为临床试验的质量患者的健康及其后的药监核查埋下隐患。
此外,受试者招募这一行业还有诸多关系需要厘清。由于医生仍然是主要的招募渠道,当招募方在研究中心以外的医院组织线下活动进行招募时,需要付给院方和医生相应的报酬,厚普医药目前通过多点执业的形式,利用周末的时间来进行相关活动,但大部分招募公司或多或少都存在合规的风险。
“招募公司就像珍爱网、百合网,在缺乏治疗手段的患者和缺乏病人的研究中心之间搭建桥梁,搭的好,对哪方都是好事,但搭不好就是黑洞。”该新药研发人员表示,王亚楠也认为,一些进入这个领域的企业缺乏对临床试验的敬意,损害患者和试验质量,也影响了行业声誉。
由于受试者招募是新药研发环节中较小的一个环节,目前还没有相关法规约束。2019年新版《药品管理法》和2020年发布的《药品注册管理办法》都对临床试验环节新增了相应规定,但对招募这一细节问题上仍缺乏相应可依靠的条文。行业急需规范。
04 劳力型行业希冀转型
对于厚普等较为大型的招募公司,仍然希望在这一行业内有所突破。
严苛的入组标准和越来越难寻的患者,使得患者转化率偏低,王亚楠告诉本刊记者,目前厚普通过线上、线下两种方式招募受试者,其中线下招募的受试者占比在80%左右,包括患者活动、医生、院内广告等渠道,“主要靠员工铺下去沟通”;线上的招募占比在20%左右,包括线上的患者组织、第三方的数据、基因检测公司等渠道。
但转化率、转化量低仍然是一个问题,患者难以精准定位。同时激增的临床试验使得行业竞争激烈,“有的公司通过各种方式搜集、哄抢病人,例如‘免费用药’、‘最先进’、‘世界第一个’等不合规词语诱导患者,过分夸大疗效。”上述新药研发人员对部分受试者招募公司的行为表达了担忧。
美国等国家有专门的受试者保护法,我国在相关法律中也有涉及到受试者权益保护的部分,但描述仍然模糊。厚普医药在线上招募时也遇到过问题,其在做小程序时曾经跟腾讯做过多次沟通,对方才同意利用小程序进行临床试验服务,而在其他的网络渠道上发布信息时,也有遭删除甚至封号的风险。而问题的根源在于缺乏相关法律依据,招募工作发生纠纷时“无法可依”。
王亚楠表示,目前受试者招募可以参考的相关条款只有ICH指导原则、GCP规范、伦理审核和广告法等,其他没有可参考的信息,“怎么做合理合法,能不能在医生、患者群体直接发布信息,都没有相关的法律法规。目前在三期试验的招募广告里不能发二期的数据,也不能带厂家信息,招募工作有着种种限制和风险。”
“中国的招募公司是劳力型,国外的招募公司是服务型。”王亚楠表示,在国外,受试者招募形态跟国内不同,可以在媒体上发布;国外的患者组织、医生组织比较熟悉招募知识,也有这种成熟的职能。而在中国,对患者信息的归属权没有明确,因而患者信息的分享在法律方面就模糊。
他以来自美国的DEEP6公司为例,这家公司可以连接医院的系统,当遇到合适的病人时系统会告知医生,至少避免院内流失,不需要医生或者CRC一个个去查。
目前,厚普医药计划在不同疾病领域“建池”,从患者首次就诊就开始建立随访关系,提供一些专业资讯,当疾病发展到一定程度时,部分病人就可以选择临床试验的方式,一方面患者节省费用,一方面部分情况下确实对于患者的病情更有价值,而这样一些计划需要得到患者组织、线上患者社区以及患者本人等各方面的支持。王亚楠也希望,相关部门能够厘清受试者招募各个环节的关系、责任与义务,患者组织也能承担起相应的职责,共同为缺乏治疗手段的患者与新药研究者搭起良好的桥梁。
平均每个临床试验由于所处阶段不同,因而需要的受试者数量从20到数千不等。目前在肿瘤领域较为火热的PD-1单抗,由于其对多种癌症都有效,因而国内几乎每家获批PD-1的企业都开了20个以上的临床试验。目前国内仅PD-1这一品种就已有至少30余家企业申报,开设临床数百个。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#受试者#
39
#受试者招募#
38
#招募#
28