FXR激动剂ASC42治疗NASH:美国FDA已批准IND
2020-10-12 Allan MedSci原创
制药公司Gannex Pharma今天宣布,其候选药物ASC42治疗非酒精性脂肪肝(NASH)的研究性新药申请(IND)已获得FDA批准。
制药公司Gannex Pharma今天宣布,其候选药物ASC42治疗非酒精性脂肪肝(NASH)的研究性新药申请(IND)已获得FDA批准。
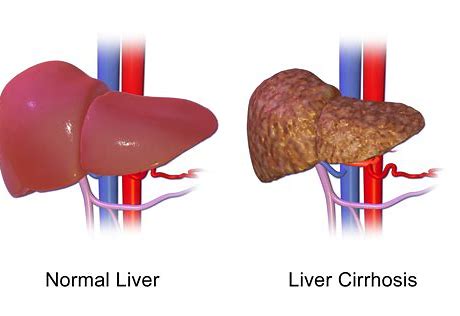
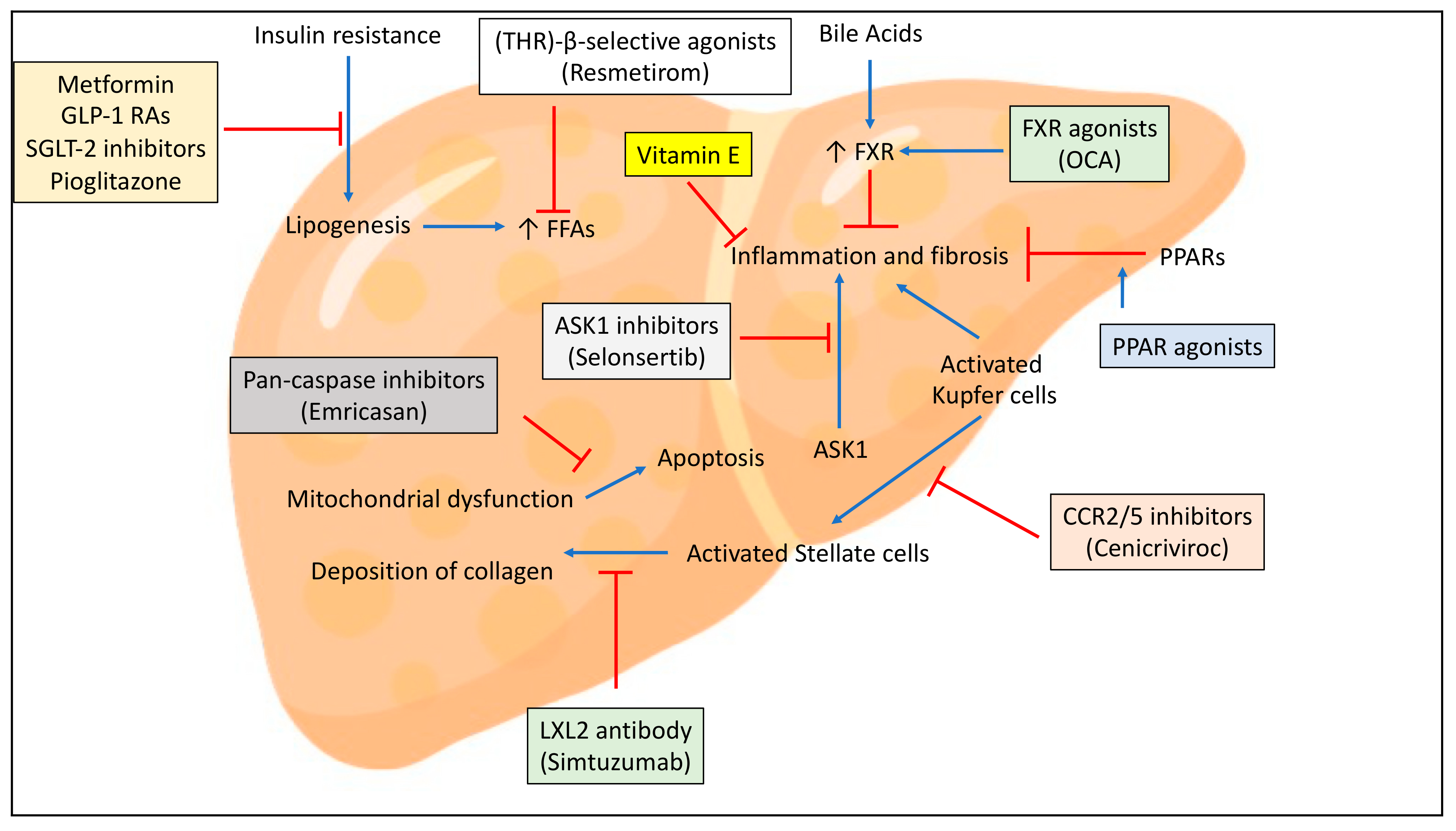
ASC42是一款新型非甾体选择性强效法尼醇X受体(FXR)激动剂。在两种NASH动物模型中,ASC42能够明显改善肝脂肪变性、炎症和纤维化。
Gannex Pharma在其NASH管线的临床阶段还有另外两种候选药物ASC40和ASC41。在II期临床试验(FASCINATE-1研究)中,在50 mg组中,口服脂肪酸合酶(FASN)抑制剂ASC40(TVB-2640)已被证明能以61%的应答率显著降低肝脏脂肪水平。ASC41是一款肝脏靶向的前药,其活性部分(ASC41-A)对THR-β具有选择性。预期ASC42可以单独使用,也可以与ASC40或ASC41联合使用。
Gannex Pharma首席科学官Handan He博士说:“我们很高兴FDA为NASH批准了ASC42的IND。NASH是一种越来越流行的疾病,目前尚无批准的疗法。这是一个重要的里程碑,使我们能够在今年开始临床试验,以满足治疗NASH的医疗需求”。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#FXR激动剂#
35
#ASC#
34
#ASH#
28
#IND#
27
#美国FDA#
33
#FXR#
31
#激动剂#
20