Clin Cancer Res:Niraparib联合镭-223治疗转移去势抵抗性前列腺癌的I期研究
2022-11-09 AlexYang MedSci原创
调查了niraparib(一种PARP抑制剂)与Radium-223联合治疗转移趋势抵抗性前列腺癌(mCRPC)的安全性情况。
据估计,2021年美国有25万名男性诊断为前列腺癌,是美国男性癌症死亡的第二大原因。前列腺癌细胞的生长依赖于雄性激素,因此,雄性激素阻断疗法是治疗前列腺癌的基础疗法。但随着时间的推移,该疗法仍会出现疾病进展,部分是通过不依赖于雄性激素刺激的雄性激素受体(AR)重新激活的机制,引起去势抵抗性前列腺癌。

近期,来自美国的研究人员在《Clin Cancer Res》上发表文章,调查了niraparib(一种PARP抑制剂)与Radium-223联合治疗转移趋势抵抗性前列腺癌(mCRPC)的安全性情况。

研究纳入了接受≥1线雄激素受体(AR)靶向治疗后,出现进展性mCPRC和骨转移,但没有已知的BRCA-1或BRCA-2变异或较大内脏疾病的男性。Niraparib剂量逐渐升级并与Radium-223标准剂量联合使用,并采用时间-事件连续重新评估的方法进行评估。剂量限值毒性(DLT)概率<20%的最高剂量水平定义为最大耐受剂量(MTD)。次要终点包括PSA变化和无进展生存。探索性分析包括评估ctDNA中发现的DNA突变以及全血样本中评估的基因表达变化。
共有30名患者接受了niraparib和镭-223治疗。其中,13名患者接受了100毫克niraparib治疗,12名患者接受了200毫克niraparib治疗,5名患者接受了300毫克的niraparib治疗。共有6起DLT事件:2例(13%)为中性粒细胞减少症,2例(13%)为血小板减少症,疲劳和恶心各有1例(3%)。贫血(2/13%)和中性粒细胞减少(2/13%)是最常见的3级不良事件。对于既往接受过化疗的患者,MTD为100毫克,而未接受过化疗的患者MTD为200毫克。响应者的全血PAX5和CD19基因表达较高,而非响应者的ARG-1、IL-2R和FLT3基因表达较高。
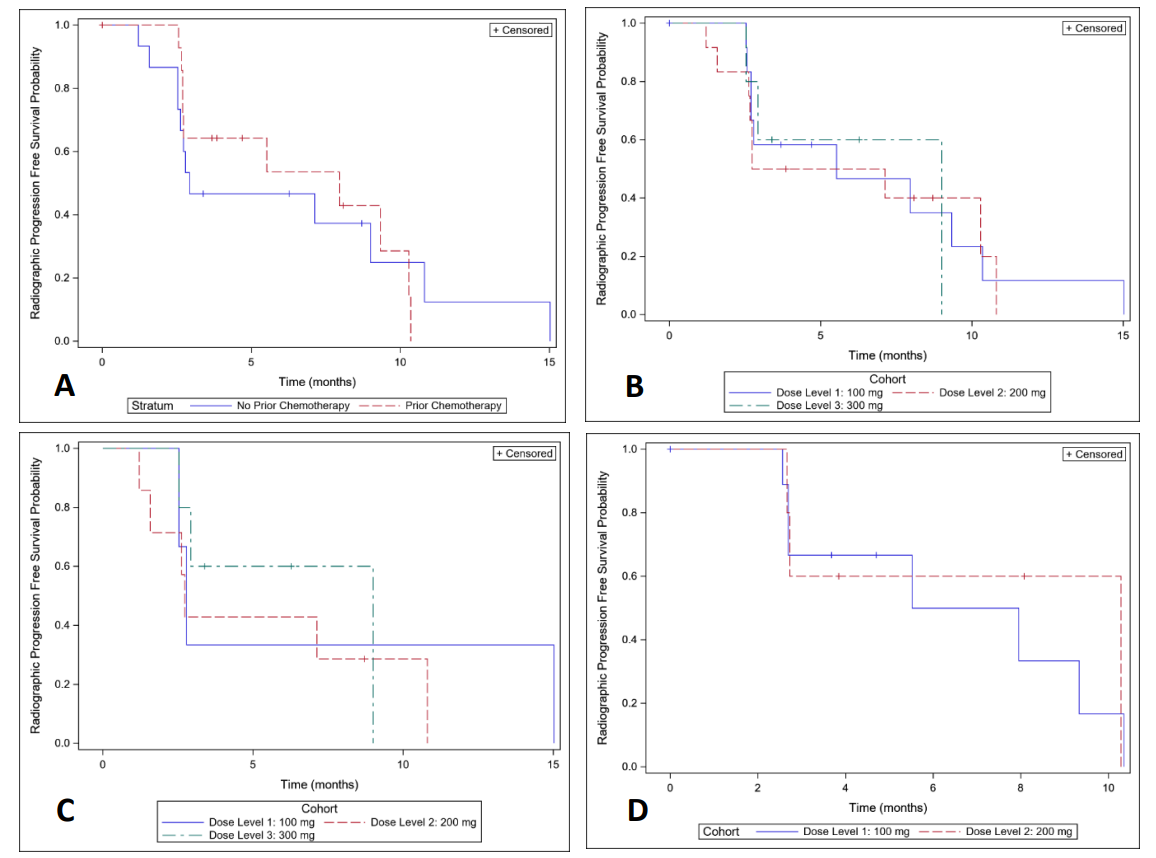
放射无进展生存(rPFS)情况
综上所述,niraparib与Radium-223联合治疗mCRPC患者是安全的。另外,结合生物标志物的进一步研究,将更好地阐明PARP抑制剂与DNA破坏性药物和其他药物联合治疗的作用。
原始出处:
Zachary Quinn, Benjamin Leiby, Guru Sonpavde et al. Phase I Study of Niraparib in Combination with Radium-223 for the Treatment of Metastatic Castrate Resistant Prostate Cancer. Clin Cancer Res. Nov 2022
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言