中国衰老标志物研究联合体发布“衰老标志物”重磅综述
2023-04-19 老顽童说 老顽童说 发表于上海
该综述是迄今为止最为前沿且详尽的衰老标志物综述,有助于引领衰老评估和预警领域的发展,并推动“健康老龄化”方案的制定。

随着人口老龄化程度不断加深,实现“健康老龄化(healthy aging)”已成为我国乃至世界迫切需要解决的重大社会和科学问题。据测算,我国60岁及以上老年人口将在2035年前后突破4亿,总人口占比将超过30%,进入重度老龄化阶段。衰老是人类慢性疾病的最大危险因素,老年慢病发生的本质是器官的衰老和退变。衰老研究领域的关键科学问题主要包括:(1)我们究竟有多老?(2)我们为什么会老?(3)我们能否健康地老?衰老生物标志物是指示机体、器官、组织、细胞及亚细胞层面衰老相关结构或功能退变的生理及分子指标,可用于监测和评估衰老伴随的生物学变化,并预测器官衰老向病变的演化程度,有助于回答“我们究竟有多老”这一科学问题,是深入开展衰老评估和预警、衰老及相关疾病干预的基础和前提。针对衰老标志物开展系统性研究,对于推动衰老的基础和转化医学发展,改善老年群体健康,制定“健康老龄化”的中国路线图具有重要的理论意义。

近日,《中国科学:生命科学》英文版(SCIENCE CHINA Life Sciences)以“封面文章”发表了由中国衰老标志物研究联合体(Aging Biomarker Consortium,ABC)六十余个研究组联合撰写的巨幅综述——“Biomarkers of aging”。该综述参考了逾2千篇衰老领域研究文献,以超9万字、31张插图和23张表格的篇幅,系统总结了衰老标志物研究在细胞衰老、器官衰老、衰老时钟及其应用、相应伦理及社会意义四个方面的重要进展(图1)。该综述在国际上率先提出了衰老标志物的基本属性、维度以及三种“原色”(Primary colors,系统性、特异性和可用性),定义了衰老标志物的六个“支柱”(Pillars,生理学特征、影像学特征、组织学特征、细胞改变、分子改变和体液分泌因子),并指出“生理行为特征“、“影像学特征“、和”体液分泌因子”可作为衰老标志物临床转化的三个可应用指标。该综述是迄今为止最为前沿且详尽的衰老标志物综述,有助于引领衰老评估和预警领域的发展,并推动“健康老龄化”方案的制定。
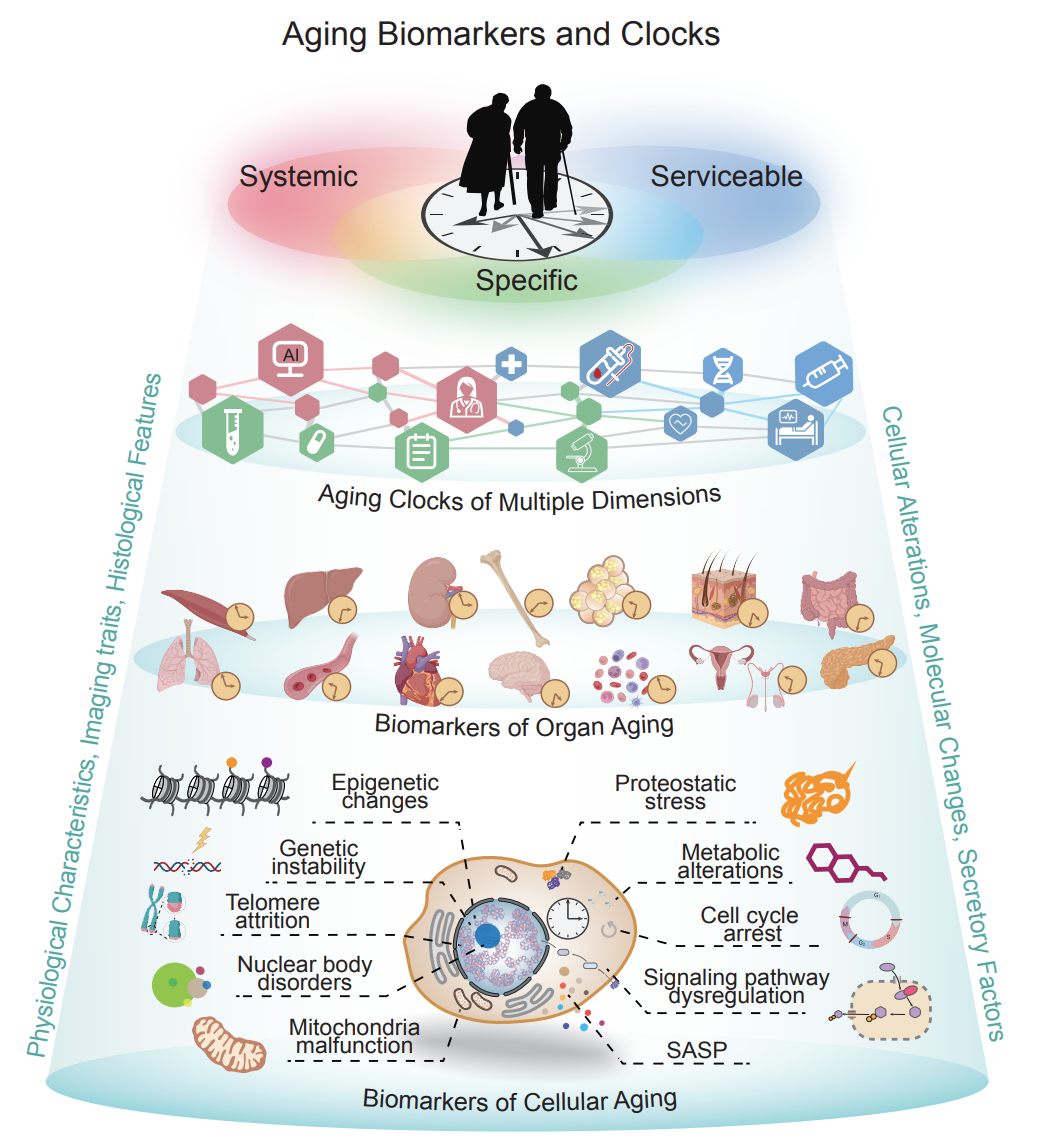
图1 衰老生物标志物概况
-
细胞衰老的生物标志物
细胞是组成器官和机体的基本单元,细胞衰老是器官和机体衰老的驱动力。细胞衰老的生物标志物不仅可以用于监测衰老过程中的细胞水平变化,而且可以用于指示整个器官或生物体的生物学年龄。该部分介绍了表观遗传变化、基因组不稳定性、端粒磨损、核内小体紊乱、细胞周期阻滞、线粒体功能障碍、蛋白质稳态失衡、代谢失调、信号通路异常和衰老相关分泌表型等十个方面的细胞衰老标志物(图2),阐明了上述标志物如何反映甚至驱动衰老相关改变,并提出新型细胞衰老标志物的发现能够拓宽人们对衰老机制的理解,从而为衰老的干预提供潜在靶标。

图2 细胞衰老的生物标志物
-
器官衰老的生物标志物
器官衰老带来的功能衰退(临床上通常表现为多种衰老相关疾病),严重影响老年群体的健康和生活质量。该部分从生理特征、影像特征、组织学特征、细胞变化、分子变化和体液分泌因子等六个方面,深入探讨了跨15种器官/系统(脑、心脏、血管、肺、骨骼肌、肝、肾、骨骼、脂肪、皮肤、肠、胰腺、生殖系统、造血系统和免疫系统)的衰老标志物(图3-4),为科学评估器官衰老程度并预警衰老相关退行性疾病提供了重要参考依据。
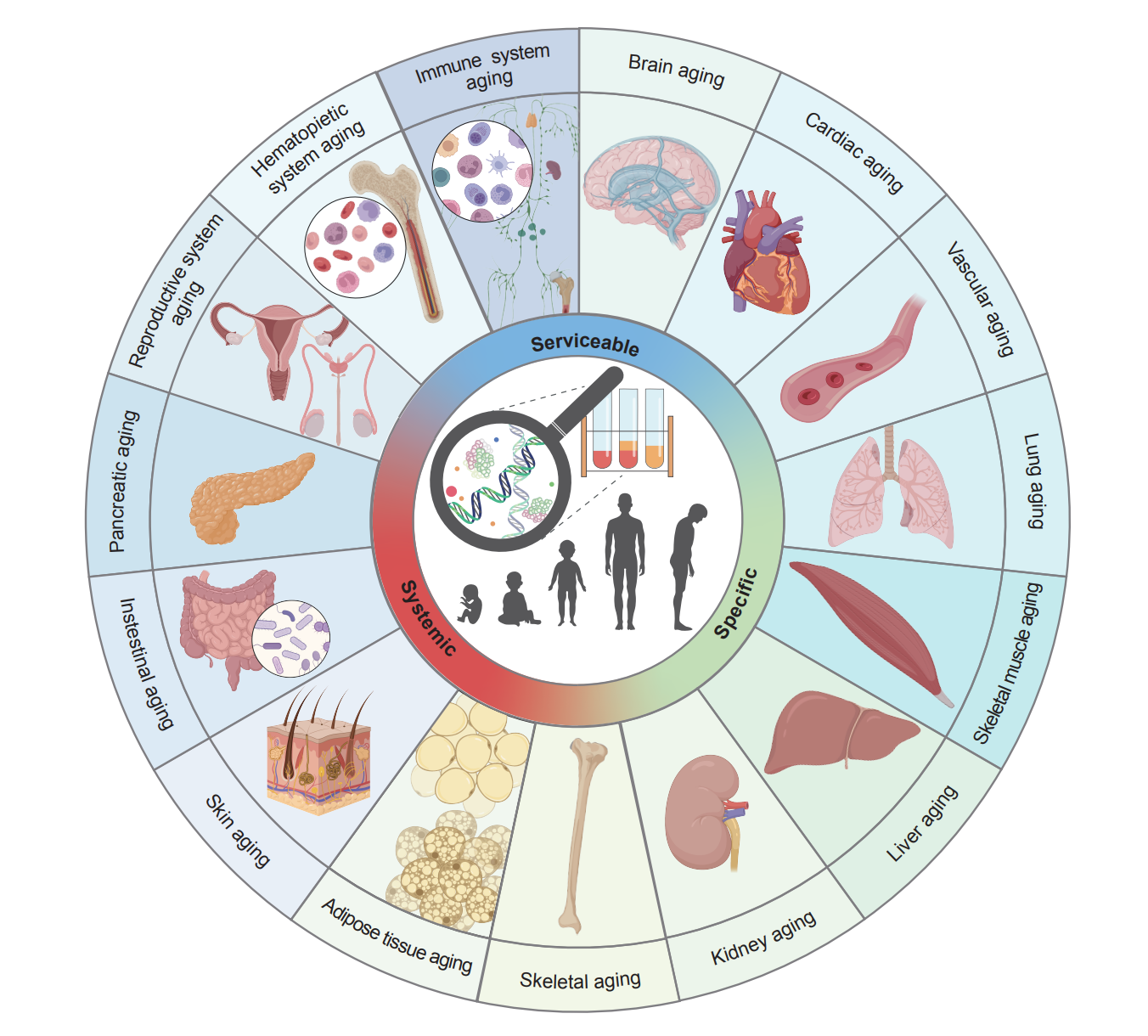
图3 器官/系统衰老标志物概况
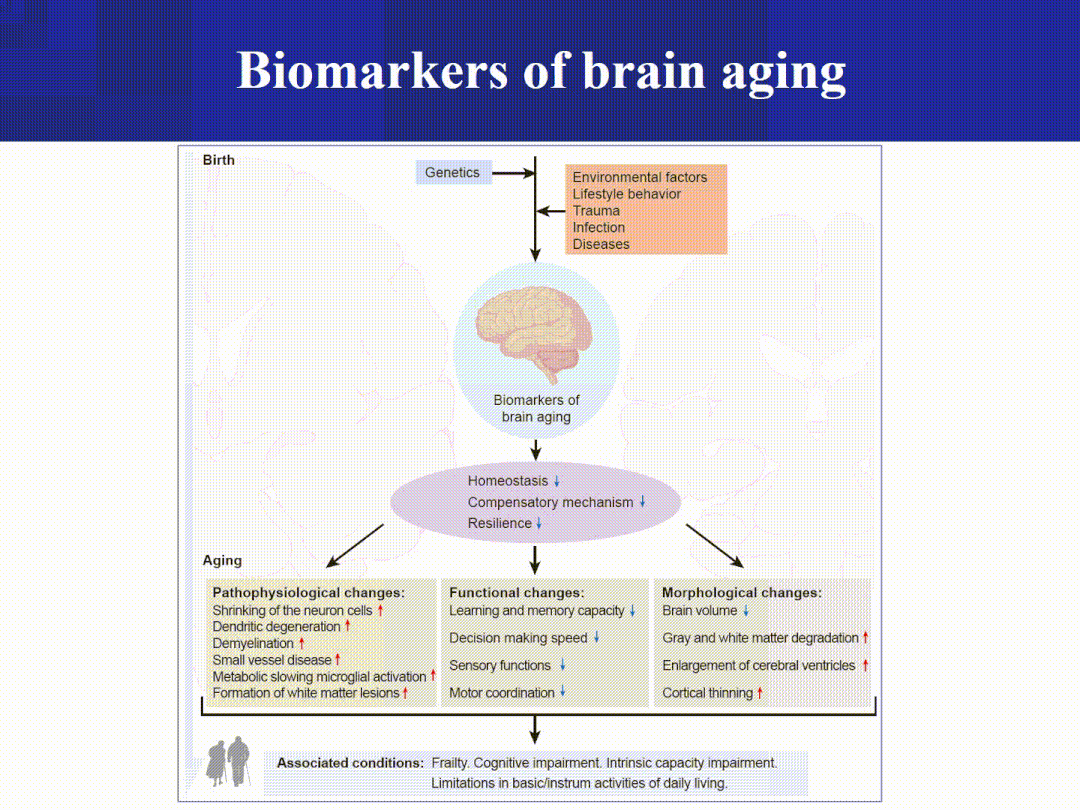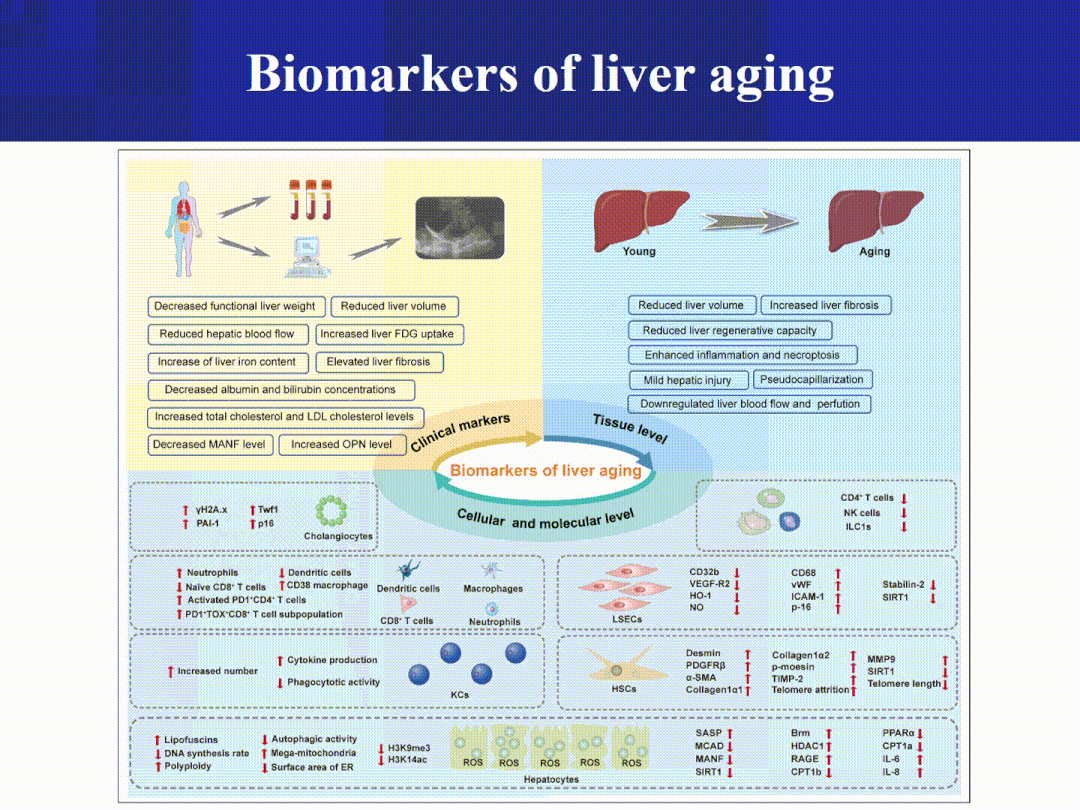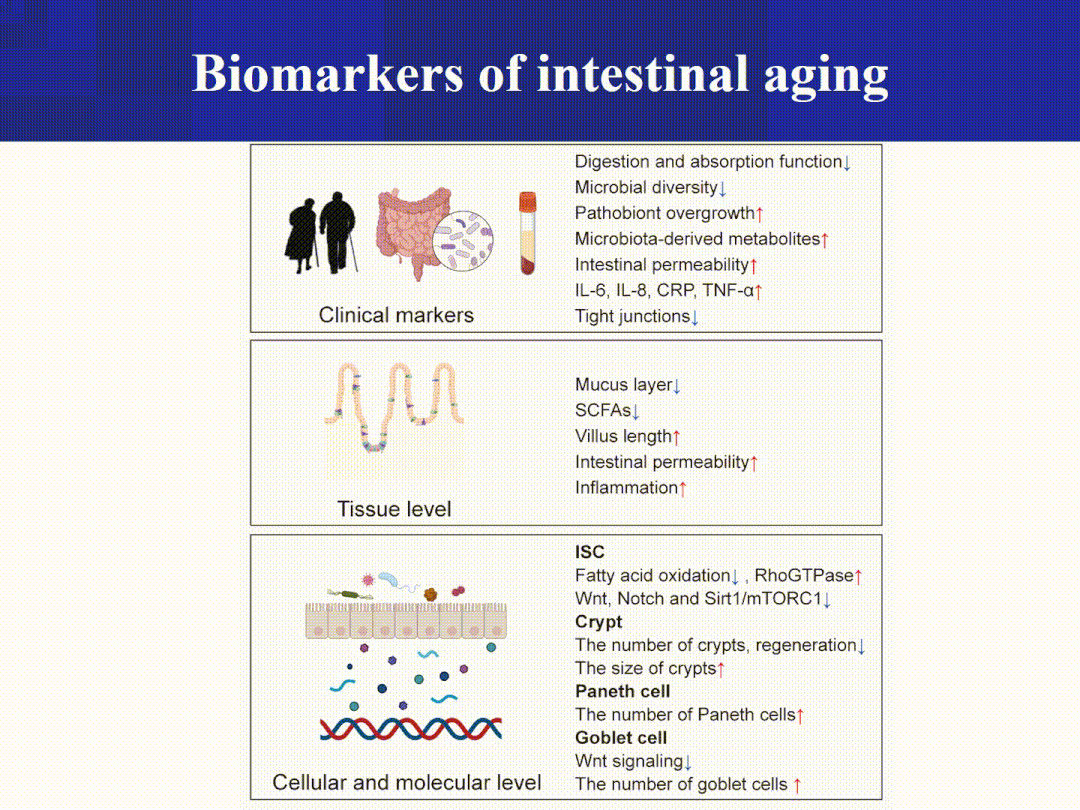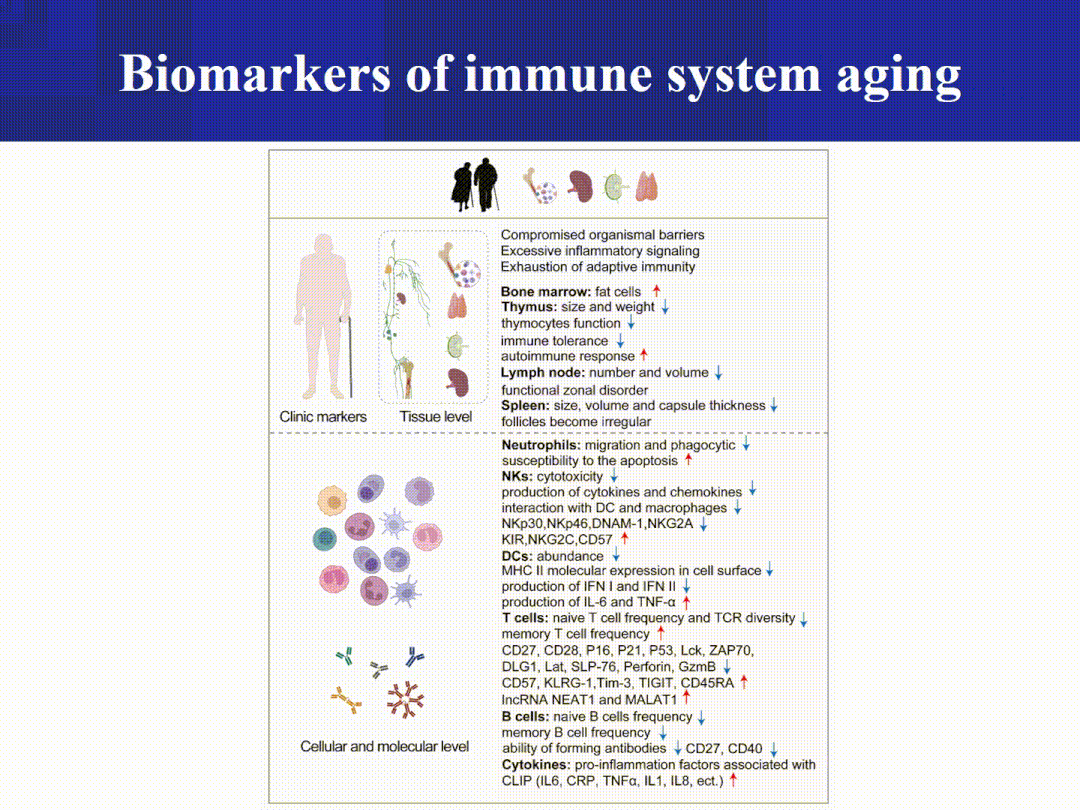
图4 指示不同器官衰老程度的生物标志物
-
衰老时钟及其应用
除了细胞和器官水平,生物个体和种群水平同样展现出衰老的异质性。使用综合指标有助于评估复杂的系统衰老,但选取最佳组合并非易事。以往研究基于大型人群队列,鉴定了衰老测量的生物标志物,结合人工智能等各种建模技术,建立了多个生物年龄或衰老时钟的预测模型。该部分系统介绍了衰老时钟及其应用,包括表型时钟、表观基因组时钟、转录组时钟、蛋白组时钟、代谢组时钟、节律时钟、长寿时钟、单细胞时钟、医学影像时钟、复合时钟,以及人工智能技术在衰老时钟中的应用,并深入探讨了这些模型在临床应用中面临的问题与挑战(图5)。

图5 衰老时钟及其应用
-
衰老标志物研究的伦理和社会因素
衰老生物标志物研究领域正在迅速发展,在预防、诊断或治疗衰老相关疾病方面展现出巨大潜力。然而,衰老标志物的基础研究及其临床转化通常以动物和人作为受试对象,存在潜在的伦理、法律和社会风险。该部分系统探讨了与衰老标志物研究及其临床转化相关的伦理、法律和社会风险,并将其归为四类:(1)科学价值;(2)知情同意;(3)评估诊断结果披露;(4)其他问题。建立规范的衰老标志物研究伦理框架,有助于为研究人员、临床医生、政策制定者和消费者提供指导,保障衰老研究领域的长期健康发展。
附(通讯作者):
刘光慧(中国科学院动物研究所),裴钢(同济大学),邹卫国(中国科学院上海生物化学与细胞生物研究所),朱大海(中国医学科学院基础医学研究所),赵玉政(华东理工大学),赵同标(中国科学院动物研究所),张灼华(中南大学湘雅医院),张云武(厦门大学医学院),张勇(中国医学科学院基础医学研究所),张维绮(中国科学院北京基因组研究所),张亮(中国科学院上海营养与健康研究所),张宏波(中山大学),张存泰(华中科技大学同济医学院附属同济医院),岳锐(同济大学),叶静(上海交通大学瑞金医院),许代超(中国科学院上海有机化学研究所),谢正伟(北京大学),肖意传(中国科学院上海营养与健康研究所),项鹏(中山大学),黄超兰(中国医学科学院北京协和医学院),王韫芳(清华大学长庚医院),王延江(第三军医大学大坪医院),王小宁(中国人民解放军总医院),王霞(清华大学),王思(首都医科大学宣武医院),王树森(南开大学),田梅(复旦大学),孙宇(中国科学院上海营养与健康研究所),孙毅(同济大学),松阳洲(中山大学),宋默识(中国科学院动物研究所),任瑞宝(上海交通大学瑞金医院),任捷(中国科学院北京基因组研究所),曲静(中国科学院动物研究所),彭耀进(中国科学院动物研究所),聂静(南方医科大学南方医院),毛志勇(同济大学),马欣然(华东师范大学),马帅(北京干细胞与再生医学研究院),罗湘杭(中南大学湘雅医院),刘勇(武汉大学),刘兴国(中国科学院广州生物医药与健康研究院),刘强(天津医科大学),刘强(中国科学技术大学),刘林(南开大学),刘峰(中南大学),刘宝华(深圳大学),李鑫(中国科学院动物研究所),黎健(卫生部北京老年医学研究所),李吉(中南大学湘雅医院),孔庆鹏(中国科学院昆明动物研究所),鞠振宇(暨南大学),黄恺(华中科技大学同济医学院附属协和医院),韩敬东(北京大学),高峰(第四军医大学),丁秋蓉(中国科学院上海营养与健康研究所),丁楅森(四川大学),慈维敏(中国科学院北京基因组研究所),陈军(北京大学),陈厚早(中国医学科学院基础医学研究所),陈国兵(暨南大学),陈畅(中国科学院生物物理研究所),陈彪(首都医科大学宣武医院),曹中炜(四川大学),曹丰(中国人民解放军总医院)
原文链接:https://www.sciengine.com/SCLS/doi/10.1007/s11427-023-2305-0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言