FDA授予伊立替康脂质体(ONIVYDE)快速通道指定,用于转移性胰腺癌的一线联合治疗
2020-06-17 MedSci原创 MedSci原创
转移性胰腺癌患者的5年总生存率为3%
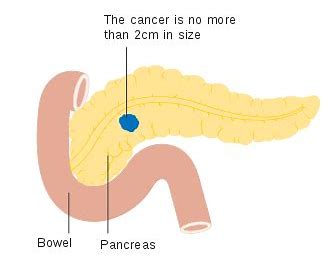
益普生公司宣布,美国食品和药物管理局(FDA)已为其伊立替康脂质体(ONIVYDE)授予快速通道指定,用于与5-氟尿嘧啶/亚叶酸(5 -FU/LV)和奥沙利铂(OX)联合,用于以前未经治疗、无法切除的局部晚期和转移性胰腺导管腺癌(PDAC)患者。
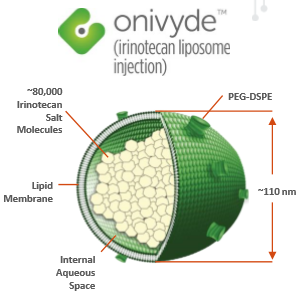
图片来源:https://seekingalpha.com/article/3816696-merrimack-pharmaceuticals-should-drive-higher-in-2016-on-onivyde-and-pipeline
FDA的快速通道计划旨在促进开发,加快对可治疗严重疾病并且有可能满足未满足医疗需求药物的审查。
ONIVYDE与5-氟尿嘧啶/亚叶酸(5 -FU/LV)的组合已经在美国和欧洲被批准,用于治疗基于吉西他滨疗法治疗后病情恶化的转移性胰腺癌患者。
益普生研究与开发部执行副总裁Howard Mayer表示:“ONIVYDE获得批准治疗转移性胰腺癌后,我们将继续致力于了解胰腺癌患者的需求,并努力改善生存率。”
“随着我们为3期NAPOLI-3临床研究不断招收更多的病人,我们期待着与FDA密切合作,将ONIVYDE在更早的疾病阶段用于更多的胰腺癌患者。”
胰腺癌是一种罕见且致命的疾病,约占所有癌症的3%和所有癌症死亡的7%。在美国57600名胰腺癌患者中,超过一半的患者为转移性胰腺癌,5年总生存率为3%。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Onivyde#
33
#脂质体#
44
#NIV#
25
#联合治疗#
40
#转移性#
33
#转移性胰腺癌#
37
#快速通道指定#
39