全球第三款RNAi药物出炉,百亿美金市场谁主沉浮?
2020-12-05 林怡龄 亿欧
2020年,全球第三款RNAi药物获批上市,跟前两款一样,又是出自基因药物先锋公司Alnylam。
2020年,全球第三款RNAi药物获批上市,跟前两款一样,又是出自基因药物先锋公司Alnylam。
11月23日,美国FDA批准了Alnylam的罕见病药物Oxlumo上市。就在四天前,欧盟委员会(EC)也刚批准了该药上市。
从1998年人类发现RNAi现象起,RNAi药物行业便经历坎坷——曾遭遇过市场的火热,也曾被资本“抛弃”,遭遇寒冬。好在20年过去,Alnylam孕育了全球首款RNAi药物,才让这个行业再次回温。
而在这个2025年市场空间将超百亿美金的行业里,坐拥全球仅有的三款RNAi药物的Alnylam,已经提前占据了龙头地位。
预计销售高峰将达5亿美元
随着FDA和EC批准落地,Oxlumo亦成为了全球首款治疗原发性高草酸尿症1型(PH1)的药物。
PH1是一种超极罕见的严重常染色体隐性遗传病,病因为肝脏过氧化丙氨酸-乙醛酸盐氨基转移酶缺乏,导致草酸产生过多,临床表现为高草酸尿症和反复尿路结石。
在Oxlumo获批之前,针对PH1唯一的治疗选择只有一种“过度水合”的方法,即使用过量的液体稀释草酸盐。而唯一解决疾病根源的治疗方法则是肝移植。如今,Oxlumo的获批为该疾病提供了一种新的治疗方式。
Oxlumo的III期临床数据显示,Oxlumo显示出了令人鼓舞的安全性和耐受性。与安慰剂组相比,Oxlumo治疗组患者达到尿草酸水平接近正常化或达到正常化的患者比例,且没有发生严重的不良事件。据悉,该项III期临床试验是一项随机、双盲、安慰剂对照试验,在全球八个国家16个临床中心入组了30例年龄≥6岁的PH1患者,这是在PH1群体中开展的最大规模的介入研究。
目前,Alnylam表示,患者只需要每三个月皮下注射一次Oxlumo。与此同时,Alnylam也准备将该药的平均价格定为每名患者每年49.3万美元,并预计每名患者的净价格将在每年38万美元左右。同时,Alnylam会与患者方签订以疗效价值为基础的三方面协议,以便只在药物有效的情况下才会收取费用。
根据协议,如果患者对治疗产生反应,该公司将在一年后收取付款。此外,公司还会根据市场情况,如患者对疾病意识的提高,诊断随着时间的推移而增加等准备降低价格。Alnylam预计,未来Oxlumo将有可能成为超稀有孤儿产品,且在使用的高峰期产生高达5亿美元的年销售额。
拓展技术和管线布局,Alnylam获黑石投资
事实上,在Oxlumo之前,全球已有两款RNAi药物获批上市,分别为用于成年急性肝卟啉症(AHP)治疗的 GIVLAARI(givosiran) 和用于成人遗传性转甲状腺素蛋白(hATTR)淀粉样变性引起的周围神经病变(多发性神经病,polyneuropathy)的治疗药物 ONPATTRO(patisiran)。而无一例外,它们都出自基因药物领域的先锋Alnylam。
2018年,Alnylam基于LNP(脂质纳米颗粒)技术和自主研发的ESC-GalNAc平台,在两个药物研发中惨败后,交出了全球首个siRNA药物Patisiran。此时,距离人类首次发现RNAi现象,已经过去了20年。小核酸药物研发终见曙光,资本掀起了RNAi药物的第二波投资浪潮。
而接下来的两年里,Alnylam基于ESC-GalNAc平台开发的药物givosiran(商品名:Givlaari)和Oxlumo(lumasiran)也都通过了FDA的上市审批,稳坐RNAi药物研发的龙头宝座。Alnylam今年三季报的数据显示,ONPATTRO第三季度的全球净收入为8250万美元,同比增长24%,而刚刚销售的givosiran则实现收入1670万美元,同比增长52%。
好消息接二连三,不少小核酸药物公司如Ionis、瑞博、Arrowhead等也迅速跟进,开发各自的GalNac共轭连接技术。在该技术支持下,干扰RNA片段经过GalNAc靶向修饰,便可以与干细胞表面的ASGPR(去唾液酸糖蛋白受体)结合,以此进入细胞内部完成递送。
如今,Alnylam正在不断拓展平台的技术,以提供更多的可能性。与此同时,其布局了丰富的研发管线作为后备力量,覆盖基因药物、心血管代谢疾病、肝传染病、中枢神经系统/眼部疾病四个领域。
Alnylam曾在去年表示,2020年将有6项晚期临床项目,并且在4大战略治疗领域拥有14项临床开发项目。而且,其预计每年将产生2-4个支持IND申请的临床前疗法。到2025年,Alnylam希望成为拥有超过8款获批疗法,十多个后期研发项目的全球五大独立生物技术公司之一。
就在今年8月,“心怀壮志”的Alnylam获得了黑石20亿美金的支持,用于RNA 干扰 (RNAi) 创新疗法的开发。Alnylam距离梦想实现,又进了一步。
曾跌落神坛,RNAi五年后市场将超百亿美金
但这个Alnylam想站稳脚跟并成为前五大之一的行业,一开始的发展并不顺利。
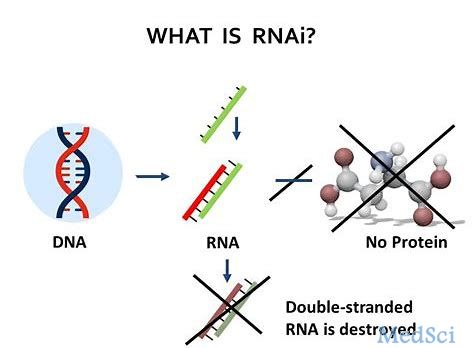
1998年,美国遗传学家Andrew Fire和Craig Mello发现了RNA干扰(RNAi)现象,一时之间让科学家们为之兴奋,认为其在生物学和医学上应用前景广阔。因为利用RNAi技术,便可以直接破坏信使RNA,从而抑制基因表达,将致病蛋白杀死在摇篮中。
2002年,专注于RNAi药物研发的Alnylam便在这样的背景下诞生了。成立之初,出于对技术的狂热,Alnylam将诸多专利律师收入麾下,以尽可能多地申请专利。彼时,这一赛道也涌入了不少企业埋头苦干。
2004年,在Andrew Fire和Craig Mello获得诺贝尔奖前夕,Alnylam用两年时间完成了在美国纳斯达克上市和与诺华达成技术平台使用权合作这两件大事。随后,伴随2016年Andrew Fire和Craig Mello摘得诺奖,RNAi被捧上神坛,资本热度持续高涨。
2005年至2009年,RNAi领域吸引了数十亿美元的资金投入,不仅催生了众多小型生物技术公司,也吸引了诸多制药巨头的进入。2006年至2008年间,罗氏和武田制药分别出资与Alnylam合作,而默沙东和阿斯利康则选择了Alnylam的竞对Sirna。
但这一赛道的狂热并没有持续多久。RNAi药物治疗效果远不及预期、系统给药效果差和脱靶造成的严重副作用都成为了该领域发展道路上的最大障碍。药物严重的副反应始终无法克服,研发也陷入了困境。
2009年,首个开展siRNA临床试验的药物bevasirnaibi(迈阿密制药公司OPKO)因效果欠佳终止临床,给狂热的RNAi药物行业当头浇了一盆冷水。紧随而来的是制药巨头纷纷中断合作离场。
但这个陷入寒冬的市场,并没有就此一潭死水,而是在前期资本狂热的涌进后,开始酝酿新的机会。随着基因测序技术发展和RNAi药物传输技术的突破,时隔几年,寒冬逐渐回暖。
如今,放眼整个行业,已有多个用于肝脏和非肝脏适应症的候选药物正处于I期、II期和III期临床试验中,针对中枢神经系统和其他非肝脏组织的研究性新药(IND)也将进入临床。
显而易见,小核酸药物已经迎来了新一波爆发。广证恒生曾预计,2025年,小核酸药物在罕见病的全球市场规模将达到 90至120亿美元;而因为在小分子化合物、蛋白质类药物不可靶向或不可成药的疾病领域,核酸药物潜力巨大,并且随着给药体系的不断完善,保守估计小核酸药物2025年全球的市场空间将远超100亿美元。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#RNAi药物#
51
#RNAi#
40