BMJ:新药快速审批通道与临床治疗价值
2020-10-09 MedSci原创 MedSci原创
在过去十年中,FDA和EMA批准的新药中,不到三分之一被认为具有较高的治疗价值,但两大医药监管部门对新药授予快速审批资格标准具有一定差异,多数经FDA批准但非EMA批准的加急药物被认为治疗价值较低
近日研究人员开展回顾性队列研究,考察了美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)批准新药的治疗价值,以及获得快速审批与新药价值的关系。

研究人员收集了2007年至2017年期间,FDA和EMA批准的新药数据,并随访至2020年4月1日。通过来自加拿大、法国、德国和意大利的卫生机构对新药价值进行分级评估。研究的主要终点为具有高治疗价值的新药比例,以及快速审批与高治疗价值评级的关系。
从2007年到2017年,FDA和EMA分别批准了320和268种新药,其中181种(57%)和39种(15%)获得了快速审批资格。 在267种参与治疗价值评级的新药中,84种(31%)被至少一家机构评为具有高治疗价值。与未获得快速审批的新药相比,获得FDA[45%(69/153)vs 13%(15/114)]和EMA[67%(18/27)v27%(65/240)] 快速审批药物具有较高治疗价值的比例更高。
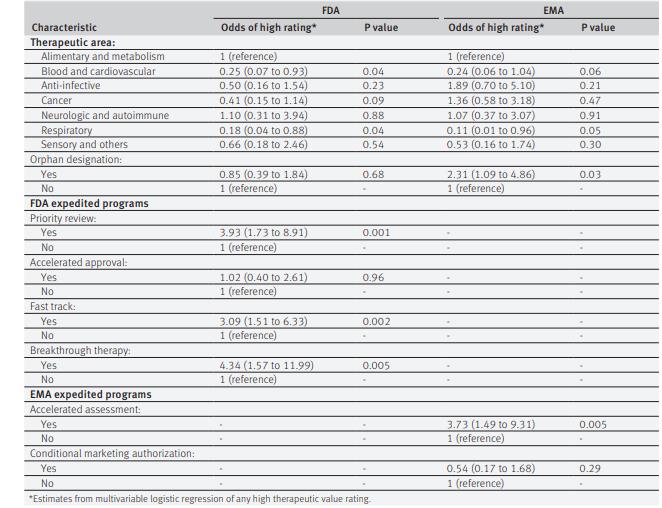
是否获得快速审批对药物的治疗价值有一定预测作用:获得FDA快速审批药物预测具有较高治疗价值的敏感性和特异性分别为82%和54%,而获得EMA快速审批药物预测具有较高治疗价值的敏感性和特异性分别为25.3%和90.2%。
在过去十年中,FDA和EMA批准的新药中,不到三分之一被认为具有较高的治疗价值,但两大医药监管部门对新药授予快速审批资格标准具有一定差异,多数经FDA批准但非EMA批准的加急药物被认为治疗价值较低。
原始出处:
Thomas J Hwang et al. Association between FDA and EMA expedited approval programs and therapeutic value of new medicines: retrospective cohort study.BMJ. 07 October ,2020.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#BMJ#
32
#快速审批#
33
#临床治疗#
41