综述:新冠肺炎的炎症风暴到底有何特殊之处?
2020-04-07 Liu Shuang 李颜课题组
新型冠状病毒(SARS-CoV-2)自入侵我国以来,给我国乃至世界各国造成了巨大的经济损失,也严重威胁着世界各国人民的生命安全。之前的推送已经对免疫系统中各个组分在病毒感染中的作用进行了概述,本次我们
新型冠状病毒(SARS-CoV-2)自入侵我国以来,给我国乃至世界各国造成了巨大的经济损失,也严重威胁着世界各国人民的生命安全。之前的推送已经对免疫系统中各个组分在病毒感染中的作用进行了概述,本次我们将会着重探究一个问题:新冠肺炎的炎症风暴到底有什么特殊之处?我们将比较冠状病毒感染中的炎症风暴与脓毒血症(sepsis)中、免疫治疗和其他病毒感染中炎症风暴的异同,并结合已有报道讨论COVID-19中炎症风暴的诱因和治疗方法。
一、炎症风暴——免疫系统过度活化导致的反噬
炎症风暴又称为细胞因子风暴(cytokine storm),是人体产生的一种过度免疫反应。笼统来说,我们的免疫系统具有抗感染能力,当其检测到感染后能迁移到损伤组织,吞噬病原或分泌细胞因子促进机体对损伤组织的修复和对病原的清除,这便是免疫系统对自身的保护作用。但如果这种作用过强,就会产生炎症风暴导致的组织损伤——机体大量产生细胞因子作用于损伤组织或其他组织的免疫细胞,导致免疫系统处于过度活化状态攻击自身。
在之前我们曾对模式识别受体(pattern recognize receptor, PRR)进行过介绍,PRR能识别外来异物,如病原相关分子模式(pathogen associated molecular pattern, PAMP)和组织损伤产生的损伤相关分子模式(damage associated molecular pattern, DAMP),激活下游信号通路以启动对病原或组织损伤的响应。正常生理状态下,组织细胞衰老后会通过凋亡(apoptosis)的方式被机体清除[1]。在这种状态下,细胞死亡释放出的物质是通过凋亡小泡的形式被巨噬细胞吞噬,并不会引起免疫系统的识别。但在病原或其他原因导致的组织损伤状态下,组织细胞会通过焦亡(pyroptosis)或坏死(necrosis)等方式死亡[2]。这种非正常状态下的死亡会导致组织细胞内容物暴露在体内,被自身免疫系统识别为外来物质,激活免疫应答。当病原数量过多、组织损伤较为严重时会导致免疫细胞持续活化并向炎症区域募集,细胞因子过量生成并进入体循环;而大量的细胞因子又会导致免疫细胞的大量激活,在短时间内引起广泛且剧烈的炎症反应,产生恶性循环(图1),这也是临床上导致感染病人死亡的罪魁祸首[3]。
在接下来的内容中,我们将比较在细胞因子释放综合征、脓毒血症和不同病毒感染中,人体细胞因子种类和浓度变化。
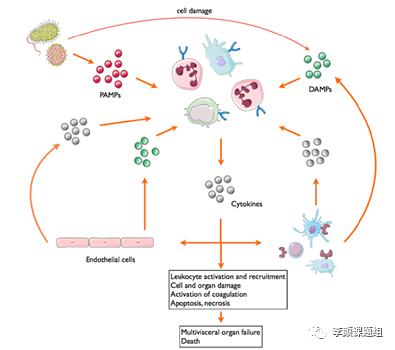
图1 炎症风暴中的级联反应
(Benjamin G, semin immunopathol, 2017)
1.脓毒血症中细胞因子的变化
脓毒血症是宿主对感染反应失调所导致的全身性多器官功能障碍,主要是细菌感染所致。细菌表面的多种PAMP能够被白细胞或内皮细胞表面的PRR识别,激活炎性细胞因子的释放。每年全世界报道的脓毒血症患者有1300-3000万人,且致死率在20%左右[4],死亡主要是由后期感染导致的炎症和多组织损伤。关于脓毒血症中炎症风暴的诱因,有报道证明革兰氏阴性菌细胞壁外的脂多糖(lipopolysaccharide, LPS)发挥着重要作用。LPS能够被细胞表面的TLR4识别,激活下游NF-κB信号通路,促进IL-1β和IL-18前体的切割和释放,这些炎性因子分泌到胞外后能够激活机体炎症反应[5]。
脓毒血症涉及到的细胞因子种类也很多,已有报道的有与抑炎相关的IL-4、IL-10、IL-1RA;促炎相关的IL-1β、IL-6、CCL3、CCL5、MCP-1、IP-10和TNF-α[6]。尽管脓毒血症的生物信息学研究取得了重大的进展,临床上也尝试减弱炎症反应或靶向细胞因子来治疗,但最终都以失败告终。最近已有研究证明镁离子在脓毒血症中具有重要作用。将镁离子与LPS混合后注射小鼠,与单独LPS注射相比,能够显著降低炎性因子如IL-6、IL-1β的分泌和肺部的损伤,并且显著提高存活率。体外实验证明,这种效果是通过抑制GSDMD-N端介导的细胞焦亡实现的[7]。
2.免疫治疗中细胞因子的变化(以CAR-T为例)
嵌合抗原受体T(chimeric antigen receptor T cell, CAR-T)细胞疗法是一种治疗癌症的经典方式,该方法向患者体内回输经过改造过的细胞毒T细胞,这些T细胞能够靶向肿瘤特异抗原对肿瘤进行特异性杀伤。因其精确、快速、高效的优点,现已批准应用于多发性骨髓瘤、急性淋巴细胞白血病(ALL)和非霍奇金淋巴瘤(NHL)的治疗[9]。细胞因子释放综合征(cytokine release syndrome, CRS)是CD19 CAR-T细胞治疗后最常见的不良事件,也是引起炎症的源头之一。在临床报告中,所有严重性等级CRS发生率为35%-100%,一般在回输细胞后的2-3周内出现[10]。其源于CAR-T回输后的过度激活所导致的一系列免疫细胞如T、B淋巴细胞,NK/T细胞和巨噬细胞等释放大量的细胞因子,这些炎症介质会引起组织损伤。
CAR-T中炎症风暴涉及到的细胞因子与脓毒血症中略有不同,主要包括IL-6、IFN-γ、IL-10、MCP-1和GM-CSF,其他细胞因子如IL-1、IL-2、sIL2Rα、IL-8和TNF-α等也有过报道[10-12]。其中,IL-6主要由内皮细胞分泌,能够导致补体级联反应的激活、毛细血管渗漏、凝血级联反应和心肌功能障碍[13];IFN-γ能够导致患者产生流感样的症状,导致巨噬细胞的激活,TNF-α、IL-6和IL-10的释放而进一步加剧炎症[14]。
3. 病毒感染导致的细胞因子变化
(1)人呼吸道合胞病毒(human Respiratory Syncytial Virus,hRSV)
hRSV是在婴儿时期和儿童早期导致支气管炎和肺炎的主要原因,轻者会出现持续4-7天的轻微鼻炎及发烧,严重者会出现剧烈的咳嗽、气喘等症状,甚至危害生命。研究表明,该病毒入侵后会导致IFN-γ和IL-10的降低,TNF-α和IL-4的升高[15],这与SARS-CoV和MERS-CoV感染后产生的表型不同。但hRSV与SARS也有许多共性,如IL-6、IL-12、MCP-1、IP-10的升高[16]。
(2)SARS-CoV
之前的报道表明,SARS病人血浆中拥有更高的Th1型细胞因子IFN-γ,炎性因子IL-1β、IL-6、IL-12和IL-13;但是在所有正常病人中并没有明显的TNF-α的升高。Th1型细胞因子IL-2和Th2型细胞因子IL-4的浓度都处于正常值以下[18,31],而抑炎因子IL-10浓度在只在某些重症患者血浆中升高(无显著差异)。此外,促进多形核中性粒细胞(PMN)迁移的趋化因子IL-8、促进单核细胞迁移的趋化因子MCP-1和促进Th1细胞趋化作用的因子IP-10都有所提高[17-18]。但也有报道称尽管IL-4浓度处于正常值以下,在正常值以下的升高或许是导致SARS重症病人死亡的因素[19]。以上细胞因子的综合作用可能会导致Th1细胞核NK细胞的激活、PMN和单核细胞向肺部的迁移而加剧肺炎。
(3)MERS-CoV
MERS-CoV的细胞因子变化与SARS-CoV有所类似,两者均表现出IFN-γ的升高;但与之不同的是TNF-α、IL-10、IL-15和IL-17A的升高,IL-4、IL-12和IL-13的浓度却没有较大差异[20]。由此可见,感染MERS-CoV的病人表现出更强的Th1和Th17型免疫反应。IL-17A能够将单核细胞核嗜中性粒细胞募集到炎症部位并增强其他细胞因子和趋化因子如IL-6、IL-1β、TGF-β、MCP-1和TNF-α的作用,来介导呼吸道感染和过敏反应中的气道重塑。
(4)SARS-CoV-2
临床上的COVID-19重症病例,一部分来自于免疫系统太弱,无法控制病毒复制而导致病情加重;另一部分是由于免疫系统过度应答而加重肺部损伤,引起炎症风暴而出现重症。
与SARS和MERS患者相同的是,SARS-CoV-2感染者的IL-1β、IFN-γ、MCP-1和IP-10在血浆中的浓度上调,可能会导致产生Th1型反应。但不同的是COVID-19患者血浆中Th2型细胞因子IL-4、IL-10和IL-13的浓度有明显上调[8]。因此COVID-19患者的免疫反应更加类似于Th1和Th2型。图2总结了在不同病毒感染后人细胞因子的种类和浓度变化的现有报道。

表1 不同病毒感染后细胞因子种类变化
(+:明显上调 -:明显下调 0:无显著性差异)(引用见文末)
通过表1我们可以看出,COVID-19与SARS和MERS患者细胞因子种类变化有一定的类似。但横向对比会发现,COVID-19患者与炎症密切相关的细胞因子的量级其实远小于SARS和MERS病人,也小于急性脓毒血症和重症CRS病人(表2)。由此可见,COVID-19患者体内的炎症水平似乎并没其他疾病那么强烈(如COVID-19患者IL-1β浓度为0.5-8pg/ml,而SARS患者IL-1β浓度为30-400pg/ml;COVID-19患者IFN-γ浓度为5-25pg/ml,而MERS患者IFN-γ浓度为120-250pg/ml)。
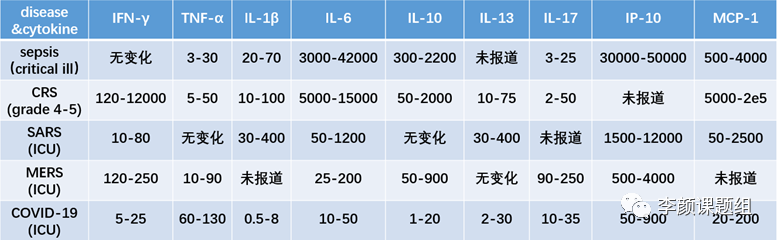
表2 不同疾病患者血浆中细胞因子浓度差异(单位:pg/ml)
(引用见文末)
值得注意的是一些与Th2相关的细胞因子,如IL-4、IL-10和IL-13在COVID-19患者血浆中的浓度上升。IL-4主要由T细胞分泌,可以促进T和B细胞的增殖并促进T细胞向Th2型转化,抑制炎症[24];IL-10则是主要的抗炎因子,能够抑制许多细胞如髓系细胞、NK细胞和T细胞的细胞因子分泌[25]。上升的IL-4和IL-10或许是COVID-19患者整体炎症水平不如SARS和MERS患者强烈的原因。
IL-13在过敏性气道疾病中研究较多,主要参与粘液的生成。其能够作用于IL-4Rα受体,激活下游信号通路进而促进某些与粘液产生有关的基因转录,促进气道上皮细胞转化为杯状细胞,而这些杯状细胞能够产生粘蛋白堵塞气道[26]。钟院士在向欧洲呼吸学会分享诊疗经验时,也曾提到过COVID-19患者肺部粘液增多,粘蛋白MUC5AC和MUC1-CT段增加,这或许是由患者体内升高的IL-13导致的。提示我们干预IL-13信号通路或许能够减少肺部粘液的聚集,改善临床病症。
二、COVID-19炎症风暴的诱因及治疗
关于COVID-19炎症风暴的诱因可能有以下几个途径:1.病毒在体内快速复制,免疫细胞大量活化释放炎症因子。2.病毒感染后在体内诱导细菌的二次感染,导致免疫细胞在应对细菌感染中过度活化。3.病毒导致的组织损伤产生大量的DAMP,可以被免疫细胞识别,引发强烈的免疫反应。
关于SARS-CoV-2诱导炎症风暴的分子机制也有了新突破。最近,中科大研究团队对33例COVID-19患者进行了分析,发现与健康人相比,患者外周血中的炎性单核/巨噬细胞(CD14+CD16+)的比例和数目明显升高。这些巨噬细胞能够分泌更多的促炎因子IL-6和GM-CSF[21](图2)。其中IL-6能够作用于血管内皮细胞和肺泡细胞,导致血管渗漏和肺损伤;而GM-CSF能够促进髓系细胞的增殖分裂,增加巨噬细胞和粒细胞的数量,从而进一步提高患者炎症水平。此外,分泌GM-CSF和IL-6的CD4+ T细胞的比例以及分泌IFN-γ的T细胞比例在患者中也明显升高。
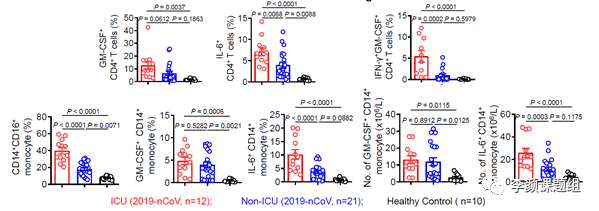 图2炎性巨噬细胞和Th1细胞在COVID-19患者中的变化
图2炎性巨噬细胞和Th1细胞在COVID-19患者中的变化
(Zhou Y.G., BioRxiv, 2020)
作者推论,SARS-CoV-2感染后,迅速激活体内炎性T细胞和炎性单核/巨噬细胞,导致GM-CSF和IL-6的产生,这些免疫细胞也许会进入肺部并发挥免疫损伤作用,导致严重肺部损伤乃至休克,这可能是诱导炎症风暴的原因之一。因此采用IL-6单抗Siltuximab和IL-6R单抗Tocilizumab或许能够有效阻断IL-6激活的信号通路进而减弱炎症风暴,治疗重症患者。
如今,IL-6R单抗Tocilizumab在临床上的应用主要是治疗重症CRS。在治疗4-5级CRS时,短时间使用一次Tocilizumab就能在一周内降低炎性因子IL-6和IFN-γ在患者血浆内的浓度,一般可降低1-4个数量级[27],减弱机体对炎症因子的过度响应,在临床重症CRS患者救治中具有较好的疗效。最近,中科大研究团队招募了21名COVID-19患者,在开展常规治疗的同时注射了Tocilizumab(400mg静脉滴注),结果显示,所有患者在注射Tocilizumab后均出现体温的恢复,有19名患者出现肺部症状的减弱[28]。因此未来,探索IL-6信号通路在COVID-19患者中的作用的研究也至关重要。
在COVID-19治疗方法中,酌情使用糖皮质激素对于重型、危重型SARS-CoV-2 感染的肺炎,早期、适量、短程糖皮质激素治疗既有利于控制细胞因子风暴,阻止病情进展,缩短病程,又可避免长期大量使用糖皮质激素导致的不良反应和并发症[22]。糖皮质激素的主要作用是抑制免疫系统的活化和炎症反应,在之前推送中已有介绍,此处不再赘述。
值得一提的是,COVID-19重症患者除许多促炎因子的浓度升高外,常伴随有外周血G-CSF和嗜中性粒细胞的大量增加[8]。一项对82例死亡病例的统计表明,有55例患者均表现出嗜中性粒细胞的大量扩增[23],表明极大可能出现了细菌的二次感染,这种症状与临床上脓毒血症的症状十分类似。结合前文提到的镁离子对脓毒性休克具有保护作用[7],提示我们为COVID-19病人补充安全剂量的镁离子或许有助于改善临床重症。
三、讨论
尽管现有临床证据表明,靶向IL-6信号通路能够很好地减弱COVID-19病人的炎症反应,减缓疾病进程。但一个比较有趣的现象是,通过表2的横向对比,我们可以看出,相对于其他疾病中的IL-6大幅度上升,COVID-19病人血浆中的IL-6浓度其实并不高(10-50 pg/ml),而明显升高的一个细胞因子是TNF-α(60-130 pg/ml)。
TNF-α作为一种参与全身性炎症反应的细胞因子,是构成急性期反应的主要细胞因子之一。其主要由巨噬细胞产生,此外,其他细胞如嗜中性粒细胞、T细胞、NK细胞和肥大细胞等也参与了TNF-α的合成与分泌。结合中科大团队的发现,炎性巨噬细胞在COVID-19重症患者中明显升高,这提醒我们,TNF-α在COVID-19的疾病进程中一定发挥着举足轻重的作用。因此,靶向TNF-α的单抗Infliximab对于疾病的治疗或许也有较大的潜力。
在未来,除IL-6信号通路,研究TNF-α在SARS-CoV2感染中的作用或许能够更好地帮助我们了解该疾病的发生发展过程。建立靶向TNF-α或巨噬细胞的治疗手段也有着广阔的发展前景。
表1引用:[8] [15] [16] [17] [18] [19] [20] [30] [31]
表2引用:[8] [10] [16] [17] [18] [19] [20] [27] [29] [30] [31]
参考文献
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#炎症风暴#
50
学习了,非常感兴趣。
103
新冠肺炎,疫情何时才能消失
63