武汉物数所在蛋白质动态学研究的新技术新方法方面获进展
2016-12-30 武汉物理与数学研究所 武汉物理与数学研究所
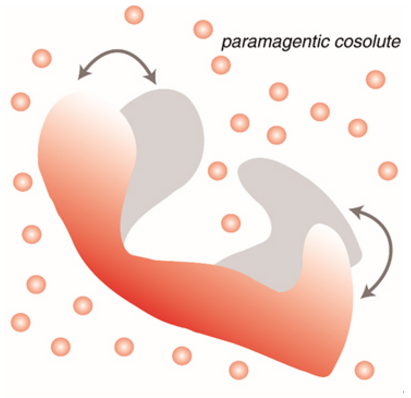
溶液顺磁弛豫增强研究蛋白质动态结构示意图近日,中国科学院武汉物理与数学研究所生物大分子动态学研究组在蛋白质动态学研究的新技术新方法发展方面取得新进展,相关研究成果发表在《德国应用化学》(Angew. Chem. Int. Ed,DOI: 10.1002/anie.201609830View)上。“生命在于运动”是法国著名思想家伏尔泰提出的运动哲学格言。蛋白质作为生命组成的基本单元,其本身也是处于不
近日,中国科学院武汉物理与数学研究所生物大分子动态学研究组在蛋白质动态学研究的新技术新方法发展方面取得新进展,相关研究成果发表在《德国应用化学》(Angew. Chem. Int. Ed,DOI: 10.1002/anie.201609830View)上。
“生命在于运动”是法国著名思想家伏尔泰提出的运动哲学格言。蛋白质作为生命组成的基本单元,其本身也是处于不断运动的动态过程中。作为生命活动的执行者,蛋白质只有通过运动才能执行特定的生物学功能,因此对蛋白质结构的动态变化的了解是洞悉其功能的关键。然而受到研究手段的制约,蛋白质动态学的研究远远落后于其结构研究。
溶液核磁共振能够在接近生理环境的溶液状态下对蛋白质进行解析,是研究蛋白质动态结构的理想方法。其中具有代表性的顺磁弛豫增强方法(Paramagnetic Relaxation Enhancement,以下简称PRE)不仅检测范围广,还能在微秒-毫秒的时间尺度上准确捕获蛋白质的动态结构,尤其是出现概率低的瞬态结构。传统的PRE方法在研究过程中,需要对蛋白质进行定点突变来引入顺磁探针,这种做法可能会破坏蛋白质本身的结构特性,额外引入的顺磁探针本身的运动也会影响到结果的准确性。
生物大分子动态学研究团队的此项研究发展了免标记的顺磁核磁技术,即不需要连接顺磁探针,将自主开发的顺磁探针直接加入到蛋白质溶液样品中来进行检测。在核磁共振实验的基础上,联合全原子分子动力学模拟采样和蒙特卡洛模拟退火的结构挑选方法来获得具体的结构信息。该方法在不同大小、不同运动特性的蛋白质体系上进行了应用,准确地捕获了这些蛋白质在溶液当中的动态系综结构。该方法的建立和发展为蛋白质动态学的研究提供了一种全新的准确便捷的研究手段。
该文的第一作者是武汉物数所副研究员龚洲。这项工作得到了科技部、国家自然科学基金委以及美国霍华德休斯医学研究所(HHMI)基金的支持。
原始出处:
Dr. Zhou Gong,et al. Protein Structural Ensembles Visualized by Solvent Paramagnetic Relaxation Enhancement. Angewandte Chemie.19 December 2016.
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#新方法#
14
#白质#
13
学习了,谢谢作者分享!
0
#新技术#
16
#蛋白质#
14