Nat Immunol:肿瘤免疫治疗抵抗的机制综述
2019-11-23 bioart bioart
肿瘤是目前威胁人类健康的首要杀手。近年来肿瘤免疫疗法对于改善某些类型的肿瘤治疗做出了突出的成绩。靶向免疫检查点PD-1和CTLA-4的抗体已经作为治疗黑色素瘤和非小细胞肺癌以及其他类型的实体瘤的标准策略。临床数据显示胶质母细胞瘤(Glioblastoma GBM)只有不多于10%的病人对免疫疗法有效。 近期,来自美国约翰霍普金斯大学的Christopher M. Jackson
肿瘤是目前威胁人类健康的首要杀手。近年来肿瘤免疫疗法对于改善某些类型的肿瘤治疗做出了突出的成绩。靶向免疫检查点PD-1和CTLA-4的抗体已经作为治疗黑色素瘤和非小细胞肺癌以及其他类型的实体瘤的标准策略。临床数据显示胶质母细胞瘤(Glioblastoma GBM)只有不多于10%的病人对免疫疗法有效。

综合“Three Es”模型和“冷热”肿瘤分类,临床中肿瘤可分为四大类:
1. 内外源因素抵抗性都低;
2. 内源抵抗低外源抵抗高;
3. 内源抵抗高外源抵抗低;
4. 内外源抵抗都高。
临床中黑色素瘤属于第一种,约50%的病人对PD-1和CTLA-4抑制剂联合治疗有效。GBM具有高度的内源性抵抗机制和外源获得性抵抗机制,属于第四种,所以只有低于10%的病人对免疫检查点抑制剂治疗有效。临床中第二和第三种肿瘤类型则有些模糊不清。第二种肿瘤治疗最初有效,但会迅速获得逃避机制,例如非小细胞肺癌,这个时间通常不到一年。第三种肿瘤本身炎症水平较低,不能产生较强的炎症反应。前列腺癌属于这种类型,肿瘤组织中免疫细胞浸润少,对免疫检查点抑制剂反应性较差。然而如果将疫苗和抑制剂联合治疗则能够提高治疗效果,这也表明一旦提高了免疫反应,前列腺癌对于免疫检查点抑制剂的反应性会得到提高。如果联合了肿瘤“冷热”的分类,则更能系统的理解“Three Es”分类。本综述以GBM为例,阐述了目前发现的肿瘤免疫治疗抵抗机制。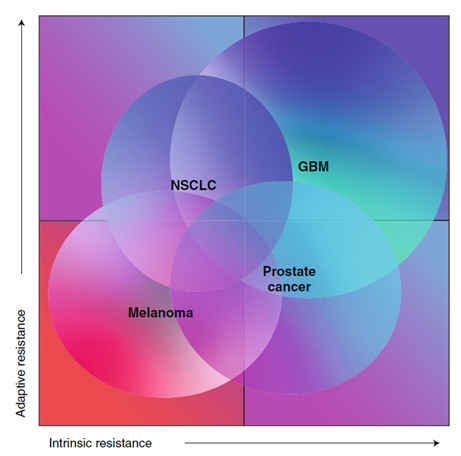
胶质瘤(Glioma)起源于中枢神经系统中的支持细胞——胶质细胞,其中胶质母细胞瘤(GBM)属于胶质瘤中最严重的一种,为IV级。GBM在美国的发病率为十万分之三。常规的治疗方法包括切除和放化疗。病人的平均生存率仅为15个月,五年生存率少于5%。GBM具有其他恶性肿瘤的分子特点,也包含有独特的特点。GBM很少向远处转移,被完全切除的GBM会在临近的脑组织中复发。放化疗能够延长病人寿命,但是会出现放化疗抵抗的肿瘤细胞。胶质瘤肿瘤干细胞被认为是治疗抵抗的来源。胶质瘤干细胞具有强大的DNA修复和分化为基质和血管的能力,获得了放化疗抵抗。由于GBM肿瘤内的异质性和分子可塑性,造成GBM没有合适的治疗靶点。对比原位和复发的肿瘤组织发现约90%的分子的表达都会在复发部位变化。基于GBM的这些特点,肿瘤免疫治疗有望克服以上这些特点。T细胞通过识别抗原不断的肿瘤组织中累积,精准进行细胞毒性功能,并形成记忆T细胞,抑制肿瘤的生长。一些实验性数据显示免疫治疗能够促进GBM的治疗,但是还尚未应用于临床。配对研究原位GBM和复发的GBM组织也能够进一步揭示获得性的抵抗机制。
无论是肿瘤之间还是肿瘤组织内部,GBM都具有高度的异质性,这些不同的突变都会实实在在促进肿瘤细胞的增殖和存活。为了进一步探究和对GBM的分子和临床特点进行分类,CGAT(The Cancer Genome Atlas)将GBM分为四种类型:前神经(proneural)、神经型(neural)、经典型(classical)和间充质型(mesenchymal)。其中经典亚型是通过含有EGFR突变来定义的。神经亚型GBM会表达神经元相关的基因。前神经类型GBM则会高表达转录因子SOX2和OLIG2以及PDGFRA。而间充质亚型GBM会发生NF1突变。 这样的分类方法只是一个探究GBM生物学的开始。进一步的研究还在改写着这个分类,特别是GBM肿瘤内高度的异质性。有一个研究发现在11个GBM的不同区域中,不同的分子类型存在于同一个肿瘤中。这样的肿瘤内异质性是对多种治疗抵抗的分子基础。肿瘤内异质性也是针对GBM的免疫治疗能够有效发挥作用的顽固障碍。免疫治疗摧毁了治疗敏感的细胞,治疗抵抗的细胞会迅速生长起来。分子的异质性也是GBM重要的内源性抵抗的机制。如果其他肿瘤免疫治疗可以比喻“战场”的话,那么对于GBM的肿瘤免疫治疗则更像是“游击战”。 适应性免疫应答如果需要达到选择性消灭肿瘤细胞而不累及正常脑组织则需要特殊性的靶点。这样的靶点需要表达在大多数的肿瘤细胞上,而不是正常组织细胞上,并且靶点对于肿瘤的生长和存活比较关键,这样能避免基因编辑造成的免疫攻击逃避。有一些研究已经表明在黑色素瘤和非小细胞肺癌中一些抗原已经能够作为肿瘤对于免疫检查点抑制剂敏感的标志,但是如果是由化疗诱导的抗原则不会有类似的效应。在另外的研究中则绘制了肿瘤中的抗原图谱,这个肿瘤抗原图谱基于MHC分子结合的亲和性和T细胞的识别性,该图谱能够预测接受PD-1靶向抗体治疗的小细胞肺癌和接受CTLA-4靶向抗体治疗的黑色素瘤的病人的生存情况。另外有研究发现高质量的肿瘤抗原特别是能够模拟微生物的抗原表位能够提高治疗效果,而单单提高肿瘤抗原的数量则不能达到促进效果。这些数据都表明肿瘤抗原的类型而不是数量是促进肿瘤免疫治疗效果的关键。 由于GBM肿瘤内高度的分子异质性,这也给分辨有效的肿瘤抗原提高了难度。目前研究的较多的肿瘤抗原是EGFR截短的三型异构体,这个肿瘤抗原在11%的确诊的GBM中高表达,在19%的GBM中表达。以往一项研究发现基于14个氨基酸肽段的疫苗(rindopepimut)对于82%的不表达EGFR三型异构体的复发GBM安全有效。但是接下来的临床试验却发现早期的免疫治疗的胜利却预示着肿瘤后面会逃避治疗,这也导致临床实验被停止。针对GBM的多价疫苗也正处于临床试验阶段,这些疫苗通过靶向多种抗原而致力于减少肿瘤的免疫逃逸。然而这些抗原还没有经过仔细的研究其有效性。利用高通量测序的方法计算T细胞抗原受体和抗原表位能够预测一些高效抗原和病人特异性的肿瘤抗原。这项技术结合精准疫苗或许能够克服GBM肿瘤内异质性带来的内源性因素治疗抵抗。这些正在进行的技术摸索也需要更多的数据支持才能确定是否能够全球推广。 另一种潜在的替代方法使将高效的肿瘤抗原原位引入GBM中。改造后的溶瘤病毒能够特异性攻击肿瘤细胞,这一过程造成肿瘤细胞死亡以及肿瘤抗原漏出,促进二次免疫反应。一期和二期溶瘤病毒针对GBM的临床实验研究发现能够促进抗肿瘤免疫反应。溶瘤病毒的应用会提高CD8+效应T细胞的浸润,降低免疫检查点TIM-3的表达。机制上的研究表明,溶瘤病毒(poliovirus PVSRIPO)攻击肿瘤细胞导致细胞中病原和损伤相关模式识别分子和肿瘤抗原释放,激活树突状细胞和一型干扰素反应。尽管溶瘤病毒治疗GBM的临床有效性还需要更多的临床实验来证明,但是目前的数据表明对付“冷”肿瘤,可以引入有效的肿瘤抗原来激发免疫反应。
免疫系统失能是在大脑肿瘤中应用免疫治疗的最主要的障碍。2011年的一项报道表明约73%的接受放疗和替莫挫胺的GBM病人每立方厘米的肿瘤内的CD4+T细胞少于300个。基础研究显示不依赖于GBM的病理类型,颅内的肿瘤都会诱导针对大脑肿瘤抗原的系统性的免疫抑制。用黑色素瘤细胞上的肿瘤抗原表达在脑癌、侧腹部肿瘤或者肺癌,随后将表达特异性针对肿瘤抗原的TCR的CD8+T细胞过继回输。检测免疫反应发现,只有脑癌的肿瘤模型出现了系统性免疫抑制反应,删除或者损伤对于肿瘤抗原的细胞毒性反应。这个现象在人样本中的其他病理类型的GBM也得到了印证。实验显示阻止了S1P1的内化和联合CD137激动剂能够恢复循环中淋巴细胞数量。 治疗性的免疫抑制作用是另一个需要考虑的因素。替莫挫胺会消除PD-1抑制剂的作用,阻碍了效应性的记忆T细胞产生。用来治疗GBM患者脑水肿的皮质类固醇,但是皮质类固醇所导致的免疫效应还存在争议。因为皮质类固醇会导致免疫抑制。
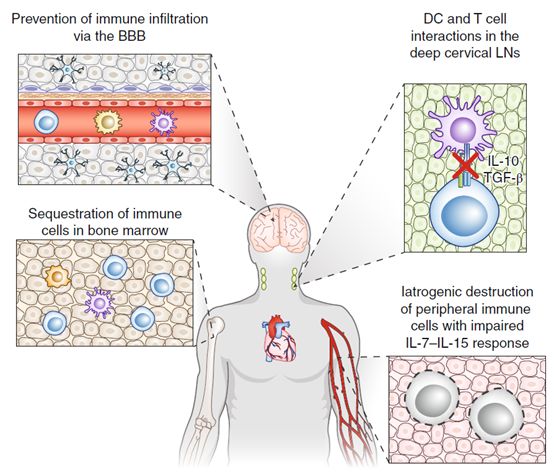
以上提到的数据讲述了克服内源性抵抗的两个问题。首先需要一个合适的肿瘤抗原靶点,其次GBM肿瘤内免疫抑制需要克服。如果攻克了GBM免疫基础水平低的问题,中枢神经细胞也可以诱导系统免疫反应。如果内源性都抵抗问题得到解决,那么外源性抵抗机制是免疫治疗GBM的另一个绊脚石。
免疫系统能够攻击肿瘤细胞,并且不会引起自身免疫反应是肿瘤治疗史上最有影响力的发现。尽管免疫检查点分子能在多种实体瘤中检测得到,在免疫应激中这些免疫抑制信号通路能够高表达。黑色素瘤中PD-1的配体PD-L1和PD-L2能够通过γ干扰素诱导的JAK-STAT信号激活表达。在肿瘤中如果存在能够被测出的基础水平的炎症反应,那么给予免疫检查点靶向抗体则能够促进抗肿瘤免疫反应的发挥。靶向PD-1和CTLA-4的抗体能够激发级别程度高的黑色素瘤和非小细胞肺癌以及肾细胞癌和其他肿瘤的抗肿瘤免疫。然而有一大部分这些类型的肿瘤病人并不能从免疫检查点抑制剂中获益。其他类型的免疫检查点像TIM-3在肿瘤获得PD-1抑制剂治疗耐药后会发生高表达。在动物模型中联合应用PD-1和TIM-3的抗体则会提高治疗效率。 基于以上的数据支持,目前临床致力于通过联合其他靶点抗体以克服PD-1或者CTLA-4靶向抗体治疗耐药问题。目前这种策略是否能够适用于GBM的治疗尚不清楚。免疫检查点抑制剂治疗的疗效能够通过检测肿瘤抗原而预测。一旦肿瘤抗原被识别,什么类型的细胞被耗竭或者被激活尚不清楚。所以一个最基础的问题还亟需解决就是GBM到底有多“冷”。 一些研究表明GBM浸润的T细胞表达多种免疫检查点,并且处于一种类似于慢性病毒感染的耗竭状态。尽管GBM中的免疫细胞耗竭非常严重,但这个也不是独一无二的,对于免疫检查点抑制剂治疗不敏感的肿瘤也存在类似的现象。有报道发现存在高突变的GBM能够提供有效的肿瘤抗原,能够受益于PD-1抑制剂的治疗。这个报道也表明如果内源性抵抗能够克服,外源性抵抗机制也能够跟其他“冷”肿瘤一样得到解决。在GBM模型中,联合应用PD-1和TIM-3靶向抗体能够提高治疗效果。研究其他类型的免疫检查点的数量正在逐年增加。其他的免疫检查点会是什么功能,它们是多余的,还是和其他免疫检查点功能一样或者是具有独一无二的免疫抑制功能?结合其他的标志物,例如表达在肿瘤细胞或者肿瘤相关巨噬细胞的免疫检查点配体也能够揭示GBM特异性的免疫抑制特性。
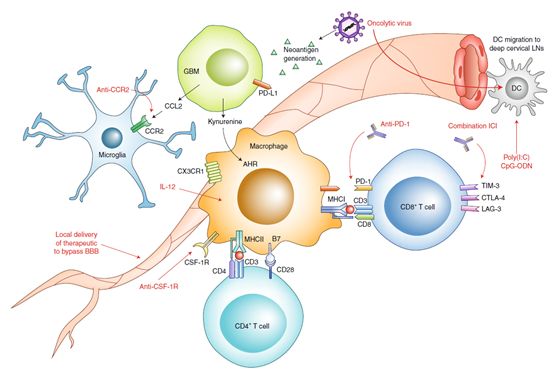
在切除GBM的组织中存在大量的髓系来源的细胞,已经成为了研究的焦点。肿瘤相关的巨噬细胞TAM通过多种途径促进肿瘤的发生发展,包括促进基因组不稳定性,支持肿瘤干细胞以及促进上皮间充质转换和通过免疫检查点配体表达来抑制抗肿瘤适应性免疫应答。 GBM募集TAM,并且促进其向抗炎症的M2方向极化。胶质瘤细胞的代谢产物kynurenine通过激活转录因子AHR来促进TAM的募集和极化。AHR也是一个评判预后的独立的标志物,用来代表髓系基因表达的丰度。GBM中的淋巴细胞较少,但是肿瘤间质中的TAM能够判断临床治疗的反应性。 针对TAM采取的是治疗策略是阻止外周单核细胞进入中枢神经系统,阻碍小胶质细胞的免疫抑制功能以及促进TAM重编程向抑制肿瘤的M1表型。抑制CCR2和CCL2能够降低TAM的密度以及能够有效地促进治疗效率。细胞因子CSF-1能够促进小胶质细胞和TAM的功能和存活,抑制它的受体CSF-1R能够抑制GBM的进展。在实验中利用CSF-1R的靶向抗体能够极大的抑制肿瘤,然而后期会因为PI3K的信号激活而导致50%的肿瘤复发。细胞因子IL-12能够将巨噬细胞从促肿瘤的表型转变为抑制肿瘤的表型。纳米颗粒能够有效地将IL-12输送到肿瘤微环境中。在GBM中,利用CD47的靶向抗体能够将小胶质细胞和TAM重编程为M1方向的巨噬细胞,吞噬肿瘤细胞。尽管这些策略是否能够促进GBM肿瘤治疗还尚不清楚,但是清楚的是单核细胞代表了一种以前未被重视的一群免疫细胞。 抗原递呈是沟通固有免疫和适应性免疫的桥梁。树突状细胞能够将CNS的抗原运输到深层的颈淋巴结。前面已经介绍过,CNS中的抗原改造过的CD8+T细胞是免疫耐受性的表型。DC是否能够参与这个过程还未可知。但是靶向DC细胞确实能够提高GBM的临床治疗效率。
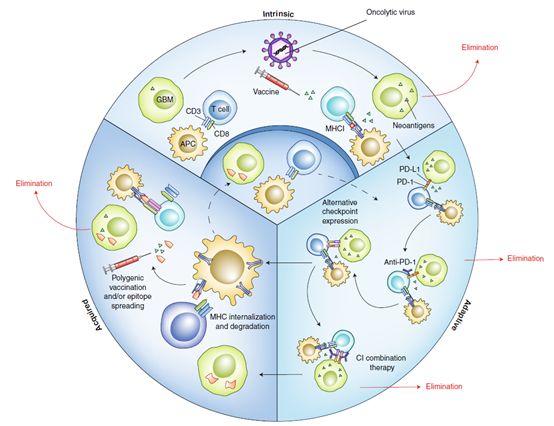
GBM能够用多种方法获得治疗抵抗。GBM免疫治疗的焦点是淋巴细胞,但是GBM中浸润的淋巴细胞非常少,并且表达多种免疫检查点。这也是免疫治疗GBM收不到良好效果的原因。联合多种免疫检查点抑制剂治疗方法是否能够进入临床还未可知。髓系来源的细胞是获得治疗抵抗的重要媒介,这个靶点还承载着治疗的希望。 随着免疫检查点抑制剂应用于更多的肿瘤病人,第三种抵抗机制也就出现了。这种抵抗机制是在免疫压力下发生的基因突变。这些适应性应答会产生内源性抵抗,导致后期治疗失败。对接受过免疫治疗并获得治疗抵抗的四名非小细胞肺癌的病人的抗原谱分析发现有些抗原发生丢失。类似的免疫细胞和肿瘤细胞的相互作用在黑色素瘤细胞中也有观察到。针对治疗产生了免疫治疗抵抗的“热”肿瘤,焦点集中在筛选高质量的肿瘤抗原。如果这个方法有效,也能够将这些肿瘤抗原应用于克隆出携带与这些抗原结合的TCR的效应T细胞来克服获得性治疗抵抗。然而那些免疫反应较低的肿瘤获得性抵抗的机制还不清楚。 目前GBM的免疫治疗还存在强度较大的内源性和获得性治疗抵抗。有研究对66名PD-1靶向抗体治疗后复发的GBM病人进行研究。他们发现17名病人的GBM组织切除的界面上的免疫反应作为治疗的基础。能够对免疫治疗做出应答的病人存在MAPK信号的激活,而不应答的病人则存在PTEN的突变。能够对免疫治疗做出应答和不应答的病人的生存率虽然有差别,但差别较小,从14.3月到10.1月的区别。GBM的程度较高的肿瘤内的异质性造成的GBM的获得性治疗抵抗一点也不惊讶。总结这些数据也表明攻克获得性抵抗是促进GBM的免疫治疗效果的可靠的出路。
总结
将免疫治疗应用于临床肿瘤极大地提高了恶性程度高的肿瘤的治疗效率。这些进步的取得是靠免疫检查点抑制剂的应用。但是仍然有超过50%的病人不能从这种方法中获益。现在肿瘤免疫治疗关注的焦点是克服多种类型的抵抗机制。针对GBM的研究已经发现在抗肿瘤治疗的各个阶段都会产生抵抗。增加肿瘤免疫治疗的效果不仅需要打破免疫耐受,产生免疫反应的抗原,也需要围绕肿瘤细胞不断适应治疗获得的逃避机制展开研究。更多的研究需要投入到认识肿瘤和免疫系统的相互作用中,GBM或许能够为此引路。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Nat#
44
机制研究离临床仍然有距离,不过与临床结合思考,仍然有帮助的,不能仅仅是纯临床思维,转化思维同样重要
44