10月25日,Cell子刊《Cell Reports》新发表一篇文章揭示,科学家们开发出一种基于CRISPR技术的高通量编辑平台,借此筛查增强免疫系统对抗艾滋病病毒能力的候选基因。
近期,加州大学旧金山分校、Gladstone研究所的研究团队利用CRISPR/Cas9基因编辑技术,找到了能够增强T淋巴细胞防御HIV病毒入侵的基因突变。他们以CRISPR变体为基础,构建了一个高通量基因编辑平台。
借助这一平台,他们可以检测不同的基因突变对免疫系统防御HIV病毒能力的影响值。他们以捐赠的人类免疫细胞为模型,利用这一新体系在体外快速编辑T细胞候选基因,旨在加快治愈艾滋病的进程。
相关研究成果于10月25日发表在Cell子刊《Cell Reports》,由加州大学旧金山分校细胞和分子药理学教授、药学院定量生物科学研究所(QBI)主任、Gladstone研究所高级研究员Nevan J. Krogan和加州大学旧金山分校医学院微生物和免疫学助理教授Alexander Marson带领团队完成。
基因编辑为治愈艾滋病提供可能
自上世纪90年代开始,伴随着生命医学的进步,人类对于艾滋病的了解和认知,抗逆转录病毒药物的研发和上市让艾滋病正朝着慢性病的方向发展。但是,每年依然有数百万新增感染者出现,我们依然没有办法彻底根治艾滋病。一旦病毒入侵患者的免疫系统,它可以永久性地掩藏在宿主细胞中。因此,患者不得不终生服用抗逆转录病毒药物。
然而,并不是每个人都容易受到病毒攻击,科学家们发现有些人的免疫系统抵抗HIV病毒感染的能力天生强于其他人。因此,他们希望未来有一天能够编辑艾滋病患者的免疫系统,增强免疫细胞防御HIV病毒的能力。
以抵抗力强的人为模型,科学家们能够通过基因组测序技术获得强化免疫系统的关键突变基因。但是,这些基因的功能却不同:一些控制病毒入侵免疫细胞,一些控制病毒基因在宿主细胞内的扩增。科学家没有办法从这些候选基因中,鉴定出真正赋予T细胞抗性的基因。
基于CRISPR,构建高通量编辑平台
去年,Marson团队首次在体外制备了CRISPR体系,并将其添加至捐赠的人类T细胞中,最终成功编辑了T细胞的特定基因。
今年,他们在去年的基础之上,开发了一个自动化系统,可以高通量、并行编辑T细胞。这一新方法能够让研究人员在成千上万个捐赠T细胞中编辑不同的候选基因,随后利用HIV感染这些突变的免疫细胞,以此筛选出防御病毒感染的关键基因。
尽管T细胞是免疫系统的主要“兵力”,但是它们只能够在体外生存数周时间。而这一系统的亮点则在于速度,克服了T细胞体外生存期短的缺陷。研究人员表示:“如果我们试图编辑T细胞,并将他们回输至患者体内。那么,这一系统将为其快速、安全和有效性提供黄金标准。”
研究人员利用新技术编辑了CXCR4、CCR5基因(编码不同HIV病毒株感染免疫细胞的受体分子)。结果发现,CXCR4基因或者CCR5基因失活,都能够封锁HIV病毒对人类T细胞的攻击。
此外,他们发现,同时抑制两个基因(一个基因负责病毒入侵免疫细胞,另一个基因确保病毒在宿主细胞中生存和扩增),能够让T细胞获得“双重保障”。
为了展示这一高通量编辑技术的有效性,研究人员挑选了45个与HIV病毒入侵宿主细胞能力相关的基因,对它们进行了146种不同的基因编辑处理。他们发现,当其中一些基因缺失时,会赋予HIV病毒耐药性。
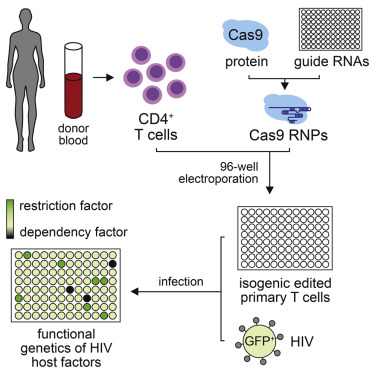
研究团队计划利用这一新平台筛查HIV病毒其他的弱点,从而找到细胞治疗或者药物的新靶点。他们也希望能够利用基因编辑技术插入更多巧妙的突变,例如在不完全沉默基因的前提下改变细胞功能使其增强对病毒的防御能力。
同时,他们更希望,除了艾滋病,这一系统将更广泛地应用于其他传染病的研究和治疗中。现在,我们能够修改人类免疫细胞,并快速看到编辑效果。未来,这一技术平台的应用前景将是巨大的。
原始出处:
[2] Researchers use CRISPR to accelerate search for HIV cure. Science Daily.October 25, 2016.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Cell#
29
#CEL#
25
#CRISPR#
23