Radiology:深度学习,让胸片焕发“第二春”!
2021-06-07 shaosai MedSci原创
尽管胸片是最常见和最完善的成像方式之一,但对于重要的临床表现,胸片存在显著的解读差异性和较低的敏感性。

尽管胸片是最常见和最完善的成像方式之一,但对于重要的临床表现,胸片存在显著的解读差异性和较低的敏感性。深度学习的最新进展为改善胸片判读提供了新的临床前景,最近有几篇报道称,机器学习模型在不同胸片表现方面可达到放射科医师水平。深度学习有潜力增强胸片在临床放射学中的应用,但面临包括广泛性差、频谱偏倚和跨研究比较困难等多方面的挑战。
近日,发表在Radiology杂志的一项研究利用放射学专家判定的参考标准开发和评估了基于深度学习的胸片解读模型,为胸片的这一传统技术的新应用提供了新的思路。
本研究开发了深度学习模型来检测胸片上的四种表现(气胸,磨玻璃表现,结节或肿块,骨折)。本项回顾性研究使用了两组数据。数据集1 (DS1)由来自多城市医院网络的759611张图像组成,而ChestX-ray14是由11220张图像组成的公开数据集。通过对图像子集的自然语言处理和专家评审,为657954张训练图像提供了标签。测试集分别由DS1和ChestX-ray14的1818张和1962张图像组成。参考标准由放射学家判定的图像审查确定。通过受试者工作特征曲线下面积分析、敏感性、特异性和阳性预测值评价其性能。四名放射学家对测试集的图像进行了回顾以行性能比较。对DS1应用逆概率加权来解释正放射图像富集和估计种群水平的表现。
气胸、结节或肿块、磨玻璃表现和骨折的受试者工作特征曲线下人群调整区域DS1分别为0.95(95%执行区间[CI]: 0.91, 0.99)、0.72 (95% CI: 0.66, 0.77)、0.91 (95% CI: 0.88, 0.93)和0.86 (95% CI: 0.79, 0.92)。ChestX-ray14的受试者工作特征曲线下面积分别为0.94 (95% CI: 0.93, 0.96)、0.91 (95% CI: 0.89, 0.93)、0.94 (95% CI: 0.93, 0.95)和0.81 (95% CI: 0.75, 0.86)。
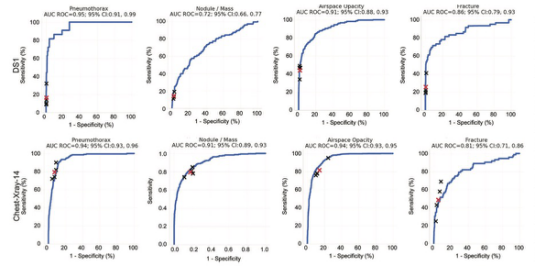
图1 受试者工作特征(ROC)曲线的性能评价。模型(蓝色曲线)和放射医师个体(黑色叉)在数据集1 (DS1)和ChestX-ray14测试集的四种表现的性能。阅读者的平均性能用红叉表示。对于DS1, ROC曲线和阅读者操作点代表了人口调整分析。
综上所述,本研究开发并评估了临床相关的人工智能胸片判读模型,该模型通过使用不同的图像集实现与放射科医生相似的诊断性能。本文报告的人群调整性能分析以及公开可获得的ChestX-ray14图像的判定标签可以为促进临床有用的胸片人工智能模型的持续发展提供有用的资源。
原文出处:
Anna Majkowska,Sid Mittal,David F Steiner,et al.Chest Radiograph Interpretation with Deep Learning Models: Assessment with Radiologist-adjudicated Reference Standards and Population-adjusted Evaluation.DOI:10.1148/radiol.2019191293
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#胸片#
34