Cancer Cell:北京大学解析肿瘤微环境形成的潜在影响因素
2022-03-18 北京大学生物医学前沿创新中心 网络
该研究勾勒出了结直肠癌肝转移患者多种组织的免疫图谱,揭示了肿瘤细胞特性和驻留器官对不同免疫细胞表型的影响。
2022年3月17日,北京大学生物医学前沿创新中心(BIOPIC)张泽民教授、任仙文副研究员、首都医科大学附属北京世纪坛医院外科彭吉润教授合作在国际期刊Cancer Cell上以Article形式在线发表了题为Immune phenotypic linkage between colorectal cancer and liver metastasis的研究论文。

肿瘤微环境(TME)特征与癌症免疫治疗的效果有着内在的联系,且TME的特征会显著影响癌症的进展和转移情况。系统解析肿瘤微环境中不同细胞的表型是理解肿瘤发生发展、以及提高免疫治疗效果的关键。然而随着近些年单细胞技术的发展,研究人员发现不同癌症类型之间的TME有着巨大的差异,如耗竭T细胞在肝癌和肠癌患者中的比例要显著高于其在肺癌中的比例。此外,部分器官也拥有较为特异的免疫细胞类型,如大脑中的小神经胶质细胞,肝中的黏膜相关恒定T细胞(MAIT)和胃肠道中的上皮内淋巴细胞(IEL)等。那么造成不同癌症类型之间TME差异的原因是什么?是由器官微环境(niche)造成?还是由肿瘤细胞特征(malignancy)造成?亦或是两者协同作用?
对来自不同癌种、不同病人的TME进行比较分析无法回答以上问题,因其无法排除肿瘤细胞差异和不同病人遗传背景不同而产生的影响。与跨癌种分析不同,肿瘤转移的过程为研究人员提供了一个独特的系统来揭开niche和malignancy对TME的影响,因转移位肿瘤来自同一个体的原发肿瘤,收集转移患者的不同肿瘤位点可以帮助研究人员解析相同来源的肿瘤细胞在不同器官中形成的TME。
研究人员收集了17个未经治疗的结直肠癌肝转移(CRLM)患者的包括原发肠癌及癌旁,肝转移及癌旁,肠系膜淋巴结和外周血在内的101例配对样本,通过多平台的scRNA-seq和T细胞受体(TCR)序列测序,构建了CRLM患者免疫细胞的高分辨率转录组图谱。进一步整合了18位原发结直肠癌(CRC)和16位原发肝癌(HCC)患者的100例配对样本,设计了PhenoAligner方法来量化niche和malignancy对免疫细胞表型的影响,定义了表型显著受到肿瘤细胞特征影响的免疫类群(M型)、表型显著受到器官微环境影响的免疫类群(N型),系统揭示了TME、癌症类型和器官微环境之间复杂的相互作用(图1)。
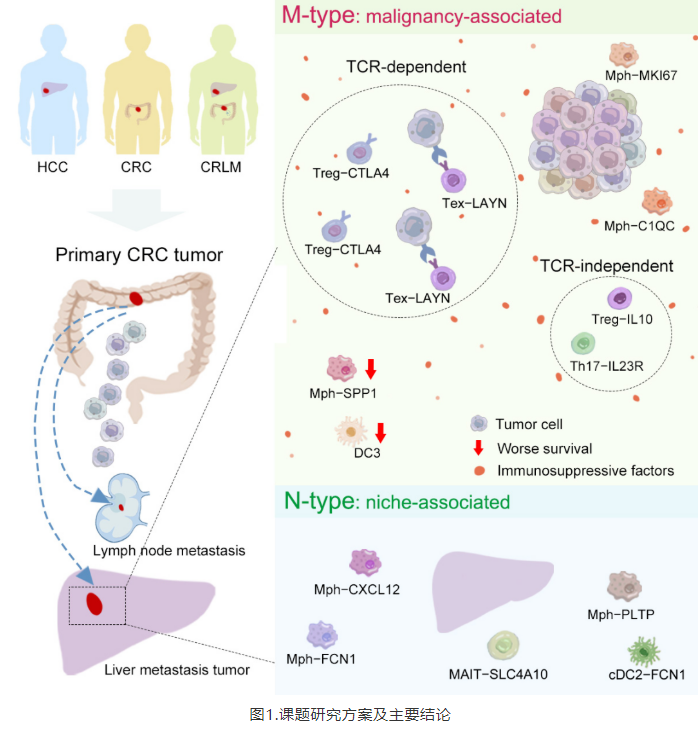
通过比较CRC和HCC患者的免疫细胞浸润情况,研究人员发现免疫细胞的浸润可能与病理状态相关(肿瘤/癌旁组织),也可能与其驻留的器官相关(肠/肝):Treg-CTLA4,Tex-LAYN和Mph-C1QC与癌旁相比更加富集在肿瘤组织中;MAIT细胞倾向于在肝中富集而IEL细胞倾向于在肠中富集。为了去除跨癌种比较潜在的偏差,研究人员利用肿瘤转移数据自体对照的优势,设计了PhenoAligner算法以CRLM为模型系统评估了niche和malignancy对免疫细胞表型的影响(图2)。
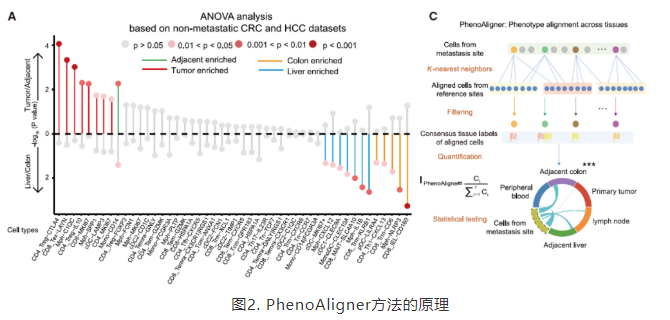
在CD8+T细胞中,耗竭T细胞(Tex)被识别为M类,即其表型主要受肿瘤细胞决定:在原发肿瘤位和肝转移位存在大量相近表型的Tex细胞,而在其他组织中不存在或极少。这一基于PhenoAligner分析得到的结果进一步得到了TCR序列分析结果的证实,在两个肿瘤位点间存在大量具有相同TCR序列的Tex细胞。但是Tex细胞跨组织迁移的能力极低,进一步的TCR信息和velocity分析揭示外周血中的Temra, Tem和原发灶、转移灶中的Tex细胞之间存在紧密关系,可能由共同的前体细胞经过相同的肿瘤相关抗原刺激形成。这一发现进一步丰富和深化了目前对肿瘤免疫循环(cancer-immunity cycle)过程的认识(图3)。

在CD4+ T细胞中,四个亚类被PhenoAligner识别为M类,结合TCR信息发现其中Treg-CTLA4和Th1-like细胞与Tex细胞一样呈现TCR依赖的模式,而Treg-IL10和Th17细胞则呈现TCR不依赖的模式,即在原发和转移肿瘤位之间没有共享的TCR序列,揭示不同肿瘤位点的Treg-CTLA4和Th1-like细胞来源于同样的前体细胞,而Treg-IL10和Th17细胞则是被肿瘤细胞从不同的起源招募而来。研究人员还发现CRLM患者的原位肿瘤中两类Treg细胞(Treg-IL10和Treg-CTLA4)的浸润要显著多于没有发生转移的CRC患者,表明与未转移的肠癌相比,发生肝转移的原位肠癌的肿瘤微环境呈现更强的免疫抑制状态。
树突状细胞(DC)是抗原特异性免疫反应的关键细胞亚群之一,在该项研究中研究人员首次在CRLM病人的肿瘤中鉴定出了DC3这一新的DC2亚型,且被PhenoAligner方法识别为M类。DC3高表达C1QA,CD68,CD163和CD14,且其特征基因和较差的预后相关。
此外,研究人员发现了三群分别高表达SPP1,C1QC和MKI67的肿瘤相关巨噬细胞(TAM),且这三群都被识别为M类。其中,C1QC+ TAM高表达CXCL9和CXCL10等与免疫检查点治疗好的响应相关的基因,且主要发挥细胞吞噬和抗原呈递的功能,提示C1QC+ TAM可能在CRLM患者的治疗中发挥有益作用。与之相反,SPP1+ TAM主要发挥促血管生成和促进肿瘤转移的功能,且其特征基因和更差的预后相关。值得注意的是,研究人员发现SPP1+ TAM不存在于原发肝癌中,却在结直肠癌的肝转移位点显著富集。对淋巴结位点的分析也发现,SPP1+ TAM只在淋巴结转移的患者中被识别到,提示SPP1+ TAM会促进CRC癌细胞的转移,对其进行功能抑制可能会在CRLM患者的治疗中发挥积极的作用。
综上,该研究勾勒出了结直肠癌肝转移患者多种组织的免疫图谱,揭示了肿瘤细胞特性和驻留器官对不同免疫细胞表型的影响,为深入理解不同癌症类型之间的免疫特征搭建了桥梁。通过PhenoAligner方法识别到了多种与肿瘤进展或转移相关的关键性免疫细胞,为开发转移癌新的临床检测与治疗手段提供了新的思路,也为后续相关研究工作提供了极有价值的数据资源。
北京大学BIOPIC/生命科学学院博士生刘烨丹,张启明为该论文的并列第一作者。北京大学BIOPIC张泽民教授,任仙文副研究员和北京世纪坛医院彭吉润教授为该论文的共同通讯作者。该研究得到北京市科委、国家自然科学基金、国家重点研发计划、北京未来基因诊断高精尖创新中心(ICG)的支持和资助。
论文链接:
https://www.cell.com/cancer-cell/fulltext/S1535-6108(22)00065-4
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#解析#
61
#CEL#
40
#北京大学#
53
#cancer cell#
41
#Cell#
39
#肿瘤微环境#
60
#影响因素#
37