GUT:HBV整合促进肝细胞癌局部及远距离致癌驱动因子的改变
2021-02-10 MedSci原创 MedSci原创
这项研究强调乙型肝炎病毒(HBC)相关的肝细胞癌(HCC)可通过不同的机制促进。肝组织中HBV整合的深入表征揭示了与肝癌发生有关的新HBV相关驱动程序机制。
这项研究强调乙型肝炎病毒(HBC)相关的肝细胞癌(HCC)可通过不同的机制促进。肝组织中HBV整合的深入表征揭示了与肝癌发生有关的新HBV相关驱动程序机制。HBV整合有多种直接致癌作用,这对于HBV感染患者的随访仍然是一个重要的挑战。
2月9日,GUT报道了HBC整合促进HCC的局部和远距离致癌驱动因子改变的结果。这项研究对主要来自欧洲和非洲的大量患者的非肿瘤和肿瘤肝组织中的HBV基因组进行了综合分析,旨在于准确地描述HBV整合与病毒和宿主基因组学及临床特征相关的关系。

该团队建立了一条新通路,在177名法国籍HBV阳性患者取样,共对177份HCC和170份非肿瘤肝组织样本中进行肝炎病毒捕获测序。在选定的3个肿瘤样本中,使用长读测序或生物纳米全基因组图谱重建了复杂的整合。
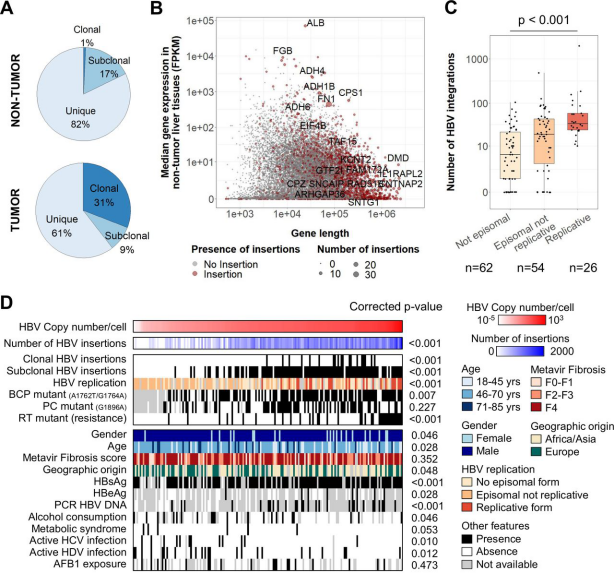
结果显示,HBV整合发生在开放的染色质区域,并与肝脏中的病毒复制有关。在170例非肿瘤性肝组织中,高HBV拷贝数与女性、年轻人、非洲或亚洲地域、血清乙型肝炎表面抗原(HBsAg)、乙型肝炎e抗原(HBeAg)和HBV DNA阳性有关。相反,HBV拷贝数和HBV整合较少与慢性肝病的辅助因素相关,如活动性HCV或HDV感染、饮酒或代谢综合征。只有18%的样本含有复制型HBV,它们富含A型,并显示出更多的整合,这表明HBV复制和整合是相互关联的过程。此外,HBV拷贝数高的样本显示基底核心启动子(BCP;A1762T/G1764A)或RT区域有频繁突变,这些突变有利于病毒复制。
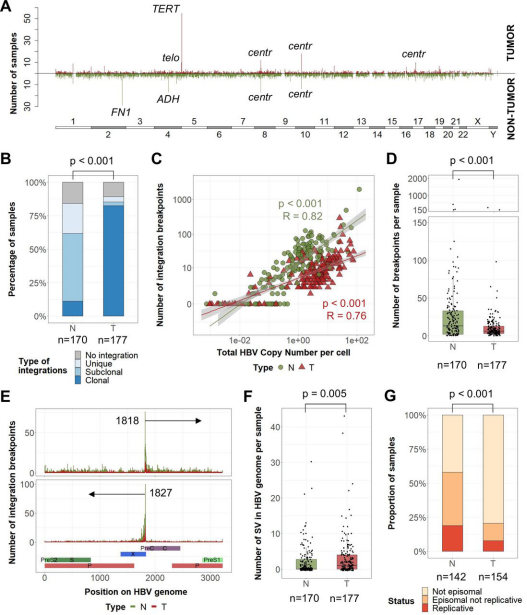
总体而言,肿瘤和非肿瘤组织具有不同的HBV整合谱和HBV序列结构。HBV整合数与每个细胞的HBV拷贝数高度相关。然而,尽管肿瘤每个细胞的HBV拷贝数更高,但每个样品的HBV断裂点数却比其相应的非肿瘤组织要低(平均值分别为12 vs 39,p <0.001)。这可能反映了感染期间大量肝细胞中独特的HBV整合的高度多样性,以及转化细胞的克隆扩增引起的多样性降低。在这两种类型的组织中,最常见的HBV整合热点出现在DR1序列(1817-1836)周围的HBx基因的C端区域,对应于HBV的双链线性DNA形式的末端。
在肿瘤中,仅检测到一部分HBV基因组对应于整合的HBV DNA,且常截断HBx基因。此外,肿瘤中的HBV基因组在病毒序列中包含更多数量的结构变异(缺失、重复、倒置),并且在肿瘤相邻肝组织中仅观察到有3%(17/514)的结构变异 。最后,人类基因组中HBV /人类交界的定位和方向表明了肿瘤中有染色体频繁重排,这表明整合过程或整合后的结构修饰比非肿瘤肝脏组织更为复杂。HBV在非肿瘤组织中的整合与病毒复制有关,在大型高表达基因中更为常见。HBV复制在非肿瘤组织中的检出率较高(7%:18%,p <0.001)。这些结果表明,非肿瘤和肿瘤肝组织中的HBV整合可能反映了不同的病毒动力学和选择过程,这些过程并不直接相关。
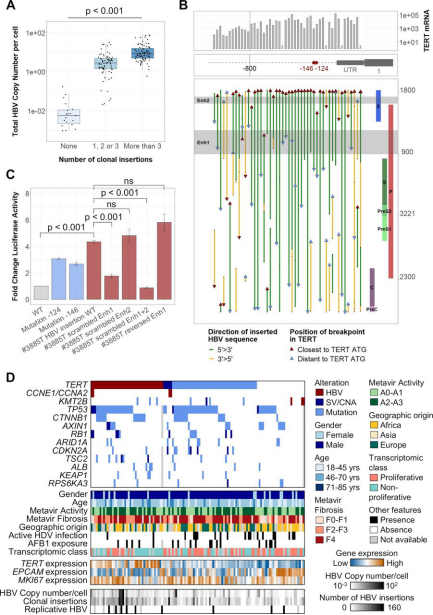
HBV整合经常限制人类染色体重排,其整合的克隆选择与两种不同的致癌机制有关。HBV基因组可以整合到癌症驱动基因中,并具有顺式激活作用。首先,HBV插入突变发展为HCC的过程中,在致癌基因附近整合病毒增强子可能会导致癌基因的强烈过度表达。其次,研究者发现在HBV整合位点频繁的染色体重排导致远处的癌症驱动基因(TERT,TP53,MYC)改变。HBV诱发的癌变也可能是由与远处病毒整合相关的癌驱动基因的频繁拷贝数改变所驱动的。研究证实,TERT启动子是HCC中主要的HBV整合热点。有趣的是,CCN-HCC显示出TERT启动子改变,而KMT2B整合的HCC没有显示出TERT启动子或任何其他驱动基因的改变,提示存在不同的致癌过程。
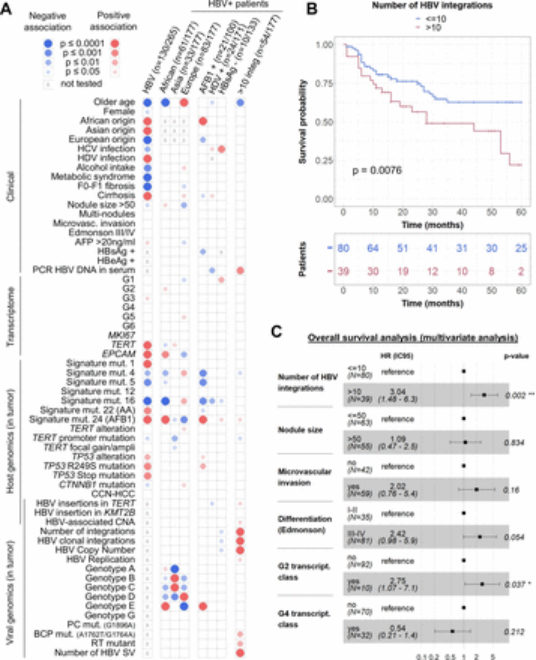
除此外,HBV整合数是HBV相关性肝癌的独立预后因素。HBV整合数量多的肿瘤预后较差。这与肿瘤大小、微血管浸润、分化状态和转录组等其他特征无关。有趣的是,这些患者明显年轻,并且肿瘤中携带高比例的HBV整合,通过插入启动子,TP53(p <0.001)或MYC(p = 0.03)影响了癌症驱动基因,如TERT(p = 0.02)。HBV相关的CNA。
由于大部分年轻患者中有发生大量基因插入的HCC,且预后较差,因此HBV整合具有直接的临床意义。
一方面,在非肿瘤组织中的HBV整合反映了病毒的活跃复制和肝组织中肝细胞的扩张,而炎症相关基因的表达却较低。另一方面,肿瘤中的HBV整合序列突出显示了具有功能性选择的细胞,这些细胞具有HBV相关的结构重排或作为驱动程序改变的插入诱变。由于具有克隆整合的非肿瘤组织显示出与炎症反应相关的基因的下调,这表明一些具有选择性优势而逃避免疫抗病毒反应的肝细胞可能会经历主动增殖并获得针对恶性转化的保护性特征。
总的来说,这项研究强调了除其他辅助因素外,HBV整合、HBV复制和肝癌发生过程中染色体不稳定性之间相互作用的复杂性。一方面,主要存在于非洲的黄曲霉毒素B1暴露,可通过TP53 R249S突变直接引发与HBV相关的HCC的发展。另一方面,HDV感染限制了HBV复制和病毒整合,但加速了年轻患者的慢性炎症和纤维化。
重要的是,该团队一系列研究表明,肿瘤中HBV整合的数量是与预后不良相关的病毒特征中的唯一标志。大量的HBV整合与非肿瘤肝组织中的病毒复制和肿瘤的不良预后有关。这表明需在病程早期便提供有效的抗病毒治疗,以限制HBV整合的数量和对抗直接与HBV相关的HCC发展。因此,这些肿瘤的异质性以及分子鉴定对确定新的特定治疗机会而言非常重要。
Reference:
Péneau C, Imbeaud S, La Bella T, et al. Hepatitis B virus integrations promote local and distant oncogenic driver alterations in hepatocellular carcinoma. Gut Published Online First: 09 February 2021.
doi: 10.1136/gutjnl-2020-323153
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#肝细胞癌#
83
#细胞癌#
45
#肝细胞#
43
#致癌驱动#
31
#HBV#
57
感谢
74
很好学习了
82
感谢分享
89
#致癌#
33
#局部#
0