肺癌新疗法!“双特异性疗法”获美国FDA突破性药物资格!
2020-03-13 汉鼎好医友 汉鼎好医友
近日,美国FDA授予双特异性疗法JNJ-6372(JNJ-61186372)“突破性疗法”认定,用于经含铂化疗后病情进展、携带表皮生长因子受体(EGFR)20外显子插入突变的转
近日,美国FDA授予双特异性疗法JNJ-6372(JNJ-61186372)“突破性疗法”认定,用于经含铂化疗后病情进展、携带表皮生长因子受体(EGFR)20外显子插入突变的转移性非小细胞肺癌(NSCLC)患者的治疗。
JNJ-6372是由丹麦Genmab和杨森公司联合开发的一种治疗癌症的双特异性抗体。该疗法目前正处于治疗晚期非小细胞肺癌的1期临床试验。

肺癌是全球第一大恶性肿瘤,在我国更是占人口恶性肿瘤死亡原因的第1位。据统计显示,非小细胞肺癌(NSCLC)患者占肺癌人群的80%左右,最常见的驱动突变是一种促进细胞生长和分裂的受体酪氨酸激酶--EGFR基因的过表达或突变。
EGFR 20外显子有插入突变的非小细胞肺癌(NSCLC)患者,通常对EGFR受体酪氨酸激酶抑制剂(TKI)治疗不敏感,与更常见的EGFR19外显子缺失的患者相比,预后更差。
目前,这类患者群体的治疗标准是常规的细胞毒性化疗。因为针对EGFR 20外显子有插入突变的肺癌患者,尚无FDA批准的靶向疗法。
双特异性抗体是一种能够识别并结合两个不同分子的蛋白质,而JNJ-6372就是这样一种靶向表皮生长因子受体(EGFR)和肝细胞生长因子受体(HGFR;cMET)的双特异性抗体。
此前,发表在《MAbs》杂志上的研究结果显示,JNJ-6372可以有效地抑制肿瘤的生长。作用机制是阻止肿瘤细胞的增殖,从而帮助治疗癌症。
这项突破性疗法认定是基于这项首个人体、开放标签、剂量增加研究的一期临床(NCT02609776)数据。目的是建立一个或多个推荐的2期剂量方案,并确定药物的限制毒性剂量。
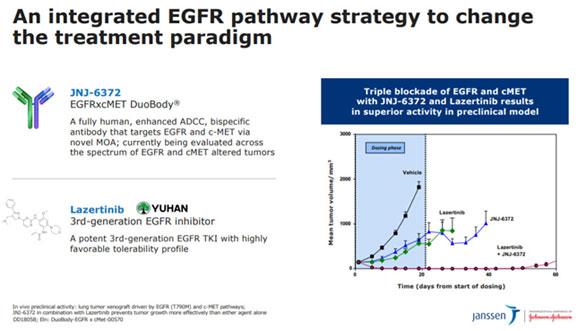
本研究评估了JNJ-6372单药治疗的安全性、药代动力学和初步疗效,并与新型第三代临床阶段治疗药物EGFR TKI --拉泽替尼(Lazertinibi)联合应用于晚期非小细胞肺癌的成年患者。
去年,韩国制药公司宇韩(Yuhan)表示已与杨森签署了一项协议,将授权拉泽替尼上市。同时两家公司合作开展全球性的临床试验,评估拉莫替尼在单药治疗和联合治疗方案中的效果和安全性。
这项研究旨在确定晚期NSCLC患者的推荐II期临床剂量,目前第二部分剂量扩展队列正在入组患者,以评估JNJ-6372单药治疗在携带基因组改变的多个NSCLC亚组中的活性,如C797S耐药突变或MET扩增。
JNJ-6372是一种新颖的双特异性抗体,有望使那些对目前可用的口服EGFR靶向疗法或免疫检查点抑制剂治疗无效、EGFR 20外显子有插入突变的肺癌患者受益。
2020年肺癌新进展
自2020年以来,针对肺癌的治疗方案多次获美国FDA审批。2月,美国FDA优先审批EGFR突变肺癌患者治疗新方案:雷莫芦单抗(英文名Ramucirumab)联合厄洛替尼(Erlotinib)用于一线治疗EGFR突变阳性转移性非小细胞肺癌(NSCLC)患者。
研究结果显示:相比对照组(安慰剂+厄洛替尼),雷莫芦单抗+厄洛替尼联合组的中位无进展生存期(PFS)达到了19.4个月,比对照组延长了7.2个月。
雷莫芦单抗是由美国礼来开发的全球首个靶向 VEGFR2(血管内皮生长因子受体2)的全人源化单克隆抗体药物,它通过抑制肿瘤血管生成来抑制肿瘤,于 2014 年在美国、日本和欧盟批准上市,尚未在国内上市。
曾经,肺癌是不治之症。但随着医学手段日新月异的今天,新一代分子靶向药物、免疫治疗药物层出不穷,肺癌正变成真正可治可控的慢性病!
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#特异性#
23
#突破性药物#
31
#突破性药物资格#
39
#药物资格#
39
#美国FDA#
21
#新疗法#
31
希望越来越多的新药造福病人
69