NEJM:尿路上皮癌所致的血尿-病例报道
2018-02-01 xing.T MedSci原创
吸烟和其他化学暴露是尿路上皮癌的危险因素。对治疗方案进行讨论后,患者选择接受机器人辅助腹腔镜肾膀胱袖状切除术。最后的病理评估显示为输尿管多发性、多灶性尿路上皮癌,手术边界为肿瘤细胞阴性。
患者为一名69岁的女性,因新发肉眼血尿而到急诊就诊。该患者有20包/年的吸烟史。
体格检查、全血计数和代谢试验结果正常。尿检结果显示每个高倍视野中超过100个红细胞和5-10个白细胞。尿培养阴性,尿细胞学检查未见恶性细胞。CT尿路造影显示右输尿管充盈缺损。硬性膀胱镜检查发现膀胱乳头状肿物,在输尿管蠕动时在右侧输尿管口可突出显示。在输尿管镜检查中,确定肿块长度为4厘米,有一个直径为5毫米的圆柱状茎;还发现了许多较小的输尿管远端肿块。病理检查证实为乳头状尿路上皮癌。
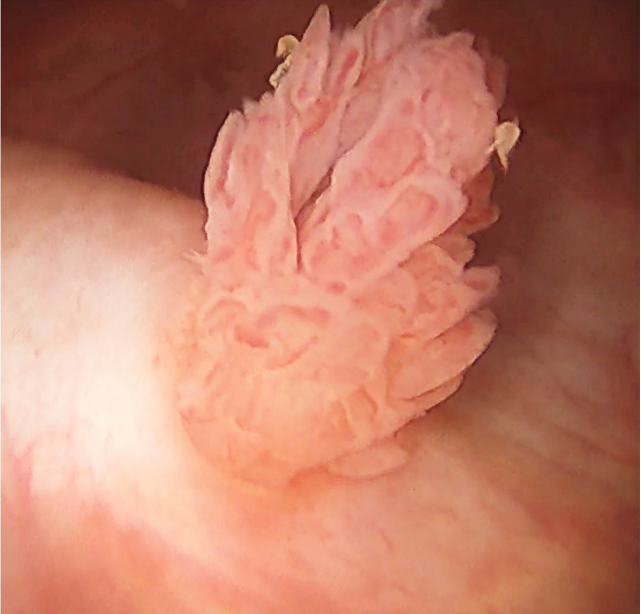
吸烟和其他化学暴露是尿路上皮癌的危险因素。对治疗方案进行讨论后,患者选择接受机器人辅助腹腔镜肾膀胱袖状切除术。最后的病理评估显示为输尿管多发性、多灶性尿路上皮癌,手术边界为肿瘤细胞阴性。
术后三个月,该患者情况良好,没有进一步血尿,膀胱镜检查没有发现疾病复发的迹象。
原始出处:
Conan So, et al. Urothelial Carcinoma.N Engl J Med 2018.http://www.nejm.org/doi/full/10.1056/NEJMicm1709216
本文系梅斯医学(MedSci)原创编译整理,转载需授权!
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










学习了
67
#血尿#
27
#上皮癌#
26
学习了谢谢分享
65
学习了新知识
66