新型抗肿瘤药物临床应用指导原则(2019版)
2020-03-16 MedSci MedSci原创
本指导原则涉及的新型抗肿瘤药物是指小分子靶向药物和大分子单克隆抗体类药物。基本原则为:病理组织学确诊后方可使用,靶点检测后方可使用。目前,根据是否需要做靶点检测,可以将常用的小分子靶向药物和大分子单克
本指导原则涉及的新型抗肿瘤药物是指小分子靶向药物和大分子单克隆抗体类药物。基本原则为:病理组织学确诊后方可使用,靶点检测后方可使用。目前,根据是否需要做靶点检测,可以将常用的小分子靶向药物和大分子单克隆抗体类药物分为两大类(表 1)

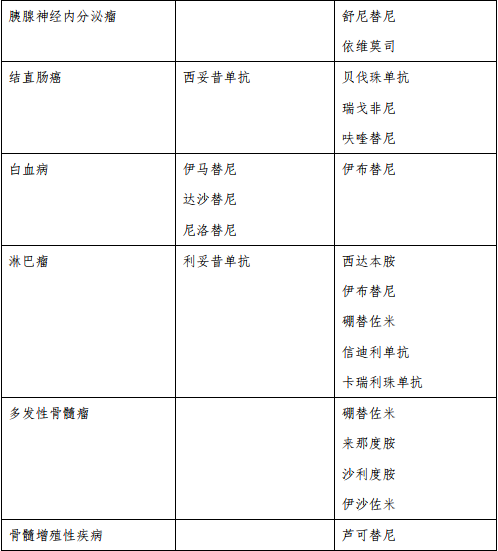
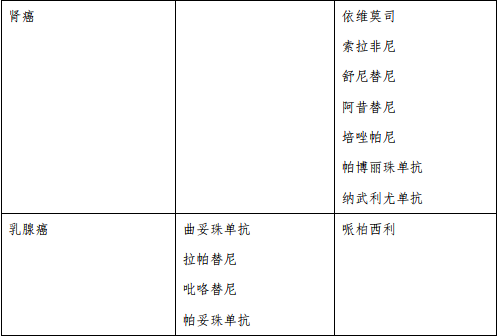
01 肿瘤药物分级
根据药物适应证、药物可及性和肿瘤治疗价值,将抗肿瘤药物分成两级。
1.普通使用级:有明确的临床使用适应证、已列入《国家基本药物目录》《国家基本医疗保险药品目录》和国家谈判药品的抗肿瘤药物品种。
2.限制使用级:有明确的临床使用适应证、未列入《国家基本药物目录》或《国家基本医疗保险药品目录》或国家谈判药品的抗肿瘤药物品种。
01 各系统肿瘤的药物临床应用指导原则
呼吸系统肿瘤用药
1.吉非替尼 gefitinib
制剂与规格:片剂:250mg
适应证:表皮生长因子受体(EGFR)基因具有敏感突变的局部晚期或转移性非小细胞肺癌(NSCLC)。
2. 厄洛替尼 erlotinib
制剂与规格:片剂:150mg
适应证:EGFR 基因具有敏感突变的局部晚期或转移性非小细胞肺癌(NSCLC)。
3. 埃克替尼 icotinib
制剂与规格:片剂:125mg
适应证:EGFR基因具有敏感突变的局部晚期或转移性NSCLC。
4. 阿法替尼
制剂与规格:片剂:30mg、 40mg
适应证:1).具有 EGFR 基因敏感突变的局部晚期或转移性 NSCLC, 既往未接受过 EGFR 酪氨酸激酶抑制剂(EGFR-TKI)治疗。2).含铂化疗期间或化疗后疾病进展的局部晚期或转移 性鳞状组织学类型的 NSCLC。
5. 达可替尼 dacomitinib
制剂与规格:片剂:15mg、 45mg,目前中国仅上市 15mg 规格
适应证:单药用于 EGFR19 外显子缺失突变或 21 外显子 L858R置换突变的局部晚期或转移性NSCLC患者的一线治疗。
6. 奥希替尼 osimertinib
制剂与规格:片剂:40mg、 80mg
适应证:1).具有 EGFR 外显子 19 缺失或外显子 21(L858R)置换 突变的局部晚期或转移性 NSCLC 成人患者的一线治疗。2).既往经 EGFR-TKI 治疗时或治疗后出现疾病进展,并 且经检测确认存在 EGFR-T790M 突变阳性的局部晚期或转移 性 NSCLC 成人患者的治疗。
7. 克唑替尼 crizotinib
制剂与规格:胶囊:200mg、 250mg
适应证:1).间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性 NSCLC 患者的治疗。2.ROS1 阳性的晚期 NSCLC 患者的治疗。
8. 阿来替尼 alectinib
制剂与规格:胶囊:150mg
适应证:ALK 阳性的局部晚期或转移性 NSCLC 患者的治 疗。
9. 塞瑞替尼 ceritinib
制剂与规格:胶囊:150mg
适应证:本品适用于此前接受过克唑替尼治疗后进展的或者对克唑替尼不耐受的 ALK 阳性的局部晚期或转移性 NSCLC 患者。
10.贝伐珠单抗 bevacizumab
制剂与规格:注射液:100mg(4ml) /瓶
适应证:贝伐珠单抗联合以铂类为基础的化疗用于不可切除的晚期、转移性或复发性非鳞状细胞 NSCLC 患者的一线 治疗。
11. 重组人血管内皮抑制素 endostatin
制剂与规格:针剂:15mg(3ml) /瓶
适应证:本品联合 NP 化疗方案用于治疗初治或复治的Ⅲ/Ⅳ期 NSCLC 患者
12. 安罗替尼 anlotinib
制剂与规格:胶囊:8mg、 10mg、 12mg
适应证:1).本品单药适用于既往至少接受过 2 种系统化疗后出现进展或复发的局部晚期或转移性 NSCLC 患者的治疗。对于存 在 EGFR 基因突变或 ALK 阳性的患者,在开始本品治疗前应 接受相应的靶向药物治疗后进展、且至少接受过 2 种系统化 疗后出现进展或复发。2).本品单药适用于既往至少接受过 2 种化疗方案治疗后 进展或复发的小细胞肺癌患者的治疗
13. 纳武利尤单抗 nivolumab
制剂与规格:注射液:40mg( 4ml) /瓶、 100mg( 10ml) / 瓶
适应证:本品单药适用于既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性 NSCLC 成人患者的二 线治疗,需排除 EGFR 基因突变和 ALK 融合的患者。
14. 帕博利珠单抗 pembrolizumab
制剂与规格:注射液:100mg(4ml) /瓶
适应证:1).帕博利珠单抗联合培美曲塞和铂类化疗药适用于 EGFR 基因突变阴性和 ALK 阴性的转移性非鳞状 NSCLC 的一线治疗。2).帕博利珠单抗适用于由国家药品监督管理局批准的 检测评估为 PD-L1 肿瘤比例分数(TPS)≥1%的 EGFR 基因突 变阴性和 ALK 阴性的局部晚期或转移性 NSCLC 一线单药治疗。
15. 依维莫司 everolimus
制剂与规格:片剂:2.5mg、 5mg、 10mg
适应证:无法手术切除的、局部晚期或转移性的、分化良好的、进展期非功能性胃肠道或肺源神经内分泌肿瘤成人 患者。
消化系统肿瘤用药
16. 索拉非尼 sorafenib
制剂与规格:片剂:0.2g
适应证:治疗无法手术或远处转移的肝细胞癌。
17. 瑞戈非尼 regorafenib
制剂与规格:片剂:40mg
适应证:1).既往接受过索拉非尼治疗的肝细胞癌患者。2).既往接受过伊马替尼及舒尼替尼治疗的局部晚期的、 无法手术切除的或转移性胃肠间质瘤患者。3).既往接受过氟尿嘧啶、奥沙利铂和伊立替康为基础的 化疗,以及既往接受过或不适合接受抗 VEGF 治疗、抗 EGFR 治疗(RAS 野生型)的转移性结直肠癌患者。
18. 仑伐替尼 lenvatinib
制剂与规格:胶囊:4mg
适应证:既往未接受过全身系统治疗的不可切除的肝细胞癌患者。
19. 曲妥珠单抗 trastuzumab
制剂与规格:针剂:440mg(20ml) /瓶
适应证:本品联合卡培他滨或 5-氟尿嘧啶和顺铂适用于 既往未接受过针对转移性疾病治疗的 HER2 阳性的转移性胃 腺癌或胃食管交界腺癌患者,对于顺铂和氟尿嘧啶类进展,而未使用过曲妥珠单抗的 HER2 阳性的转移性胃癌患者,可以考虑曲妥珠单抗联合其他有效的化疗药物治疗;曲妥珠单 抗只能用于 HER2 阳性的转移性胃癌患者, HER2阳性的定义 为使用已验证的检测方法得到的 IHC3+或 IHC2+/FISH+结果。
20. 阿帕替尼 apatinib 通用名: 制剂与规格:片剂:0.25g、 0.375g、 0.425g
适应证:既往至少接受过 2 种系统化疗后进展或复发的晚期胃腺癌或胃食管结合部腺癌患者,且患者接受阿帕替尼治疗时一般状况良好。
21. 伊马替尼 imatinib
制剂与规格:片剂:0.1g
适应证:1).用于治疗不能切除和/或发生转移的胃肠间质瘤成人患者。
2).用于 Kit(CD117)阳性胃肠间质瘤手术切除后具有明 显复发风险的成人患者的辅助治疗。
22. 舒尼替尼 sunitinib
制剂与规格:胶囊:12.5mg、 25mg、 37.5mg、 50mg
适应证:1).伊马替尼治疗失败或不能耐受的胃肠间质瘤患者。2).不可切除的、转移性高分化进展期胰腺神经内分泌瘤 成年患者。
23. 依维莫司 everolimus
制剂与规格:片剂:2.5mg、 5mg、 10mg
适应证:不可切除的、局部晩期或转移性的、分化良好的(中度分化或高度分化)进展期胰腺神经内分泌瘤成人患者。无法手术切除的、局部晩期或转移性的、分化良好的、进展期非功能姓胃肠道或肺源神经内分泌肿瘤( NET)成人患者。
24. 西妥昔单抗 cetuximab
制剂与规格:注射液:100mg(20ml) /瓶
适应证:用于治疗表达 EGFR、RAS 基因野生型的转移性结直肠癌,与伊立替康联合用于经含伊立替康治疗失败后的患者。
25. 贝伐珠单抗 bevacizumab
制剂与规格:针剂:100mg(4ml) /瓶
适应证:1).转移性结直肠癌。2).贝伐珠单抗联合以氟尿嘧啶为基础的化疗适用于转 移性结直肠癌患者的治疗。
26. 呋喹替尼 fruquintinib
制剂与规格:硬胶囊剂:1mg、 5mg
适应证:本品单药适用于既往接受过氟尿嘧啶类、奥沙 利铂和伊立替康为基础的化疗,以及既往接受过或不适合接 受 VEGF 治疗、 EGFR 治疗(RAS 野生型)的转移性结直肠癌 (mCRC)患者。
血液肿瘤用药
27.伊马替尼 imatinib
制剂与规格:(1)片剂:100mg、 400mg;(2)胶囊:50mg、 100mg
适应证:用于治疗费城染色体阳性的慢性髓性白血病 (Ph+CML)的慢性期、加速期或急变期;联合化疗治疗新诊 断的费城染色体阳性的急性淋巴细胞白血病(Ph+ALL)的儿童患者;用于治疗复发的或难治的费城染色体阳性的急性淋 巴细胞白血病(Ph+ALL)的成人患者;用于治疗嗜酸粒细胞 增多综合征( HES)和/或慢性嗜酸粒细胞白血病( CEL)伴 有 FIP1L1-PDGFRα融合基因的成年患者;用于治疗骨髓增生 异常综合征/骨髓增殖性疾病(MDS/MPD)伴有血小板衍生生 长因子受体(PDGFR)基因重排的成年患者。
28. 达沙替尼 dasatinib
制剂与规格:片剂:20mg、 50mg、 70mg、 100mg
适应证:对伊马替尼耐药,或不耐受的费城染色体阳性慢性髓细胞白血病慢性期、加速期和急变期(急粒变和急淋 变)成年患者。
29. 尼洛替尼 nilotinib
制剂与规格:胶囊:150mg、 200mg
适应证:1).新诊断的费城染色体阳性的慢性髓性白血病(Ph+CML) 慢性期成人患者。2).对既往治疗(包括伊马替尼)耐药或不耐受的费城染 色体阳性的 Ph+CML 慢性期或加速期成人患者。
30. 伊布替尼 ibrutinib
制剂与规格:胶囊:140mg
适应证:1).单药适用于既往至少接受过一种治疗的套细胞淋巴瘤患者的治疗。2).单药治疗初治及复发的慢性淋巴细胞白血病/小淋巴细胞淋巴瘤患者的治疗。3.单药或与利妥昔单抗联合治疗初治及复发的华氏巨 球蛋白血症。
31. 利妥昔单抗 rituximab
制剂与规格:针剂:100mg(10ml) /瓶、 500mg(50ml) /瓶
适应证:1). 有治疗指征的滤泡性非霍奇金淋巴瘤。2).CD20 阳性弥漫大 B 细胞性非霍奇金淋巴瘤( DLBCL)。
32. 西达本胺 chidamide
制剂与规格:片剂:5mg
适应证:适用于既往至少接受过一次全身化疗的复发或难治的外周 T 细胞淋巴瘤(PTCL)患者
33. 硼替佐米 bortezomib
制剂与规格:注射剂:1mg、 3.5mg
适应证:1).复发套细胞淋巴瘤。2).初治及复发难治性多发性骨髓瘤。
34. 信迪利单抗 sintilimab
制剂与规格:注射液:100mg(10ml) /瓶
适应证:本品适用于至少经过二线系统化疗的复发或难治经典型霍奇金淋巴瘤的治疗。
35. 卡瑞利珠单抗 Camrelizumab
制剂与规格:注射液:200mg/瓶
适应证:本品适用于至少经过二线系统化疗的复发或难治经典型霍奇金淋巴瘤患者的治疗。
36. 来那度胺 lenalidomide
制剂与规格:胶囊:10mg、 25mg
适应证:初治及复发难治性多发性骨髓瘤。
37. 沙利度胺 thalidomide
制剂与规格:(1)片剂:25mg;(2)胶囊:25mg
适应证:瘤型麻风病。
38. 伊沙佐米 ixazomib
制剂与规格:胶囊:2.3mg、 3mg、 4mg
适应证:与来那度胺和地塞米松联用,治疗已接受过至少一种既往治疗的多发性骨髓瘤成人患者
39.芦可替尼 ruxolitinib
制剂与规格:片剂:5mg
适应证:用于中危或高危的原发性骨髓纤维化(PMF)(亦称为慢性特发性骨髓纤维化)、真性红细胞增多症继发的骨髓纤维化(PPV-MF)或原发性血小板增多症继发的骨髓纤维化(PET-MF)的成年患者,治疗疾病相关脾肿大或疾病相关症状。
泌尿系统肿瘤用药
40. 依维莫司 everolimus
制剂与规格:片剂:2.5mg、 5mg、 10mg
适应证:既往接受舒尼替尼或索拉非尼治疗失败的晚期肾细胞癌(RCC),目前的研究主要基于透明细胞肾癌。
41. 索拉非尼 sorafenib
制剂与规格:片剂:200mg
适应证:转移性肾癌。
42. 舒尼替尼 sunitinib
制剂与规格:胶囊:12.5mg
适应证:转移性肾癌。
43. 阿昔替尼 axitinib
制剂与规格:片剂:1mg、 5mg
适应证:1).用于既往接受过一种酪氨酸激酶抑制剂或细胞因子治疗失败的进展期肾细胞癌(RCC)的成人患者。2).联合帕博利珠单抗适用于晚期肾透明细胞癌的一线治疗。
44. 培唑帕尼 pazopanib
制剂与规格:片剂:200mg
适应证:本品适用于晚期肾细胞癌( RCC)患者的一线治疗和曾接受细胞因子治疗的晚期 RCC 患者的治疗。
45. 帕博利珠单抗 pembrolizumab
制剂与规格:注射液 100mg
适应证:帕博利珠单抗联合阿昔替尼适用于晚期肾透明细胞癌的一线治疗。
46. 纳武利尤单抗 nivolumab
制剂与规格:注射液:40mg( 4ml) /瓶、 100mg( 10ml) / 瓶
适应证:本品联合伊匹单抗适用于 IMDC 评分为中高危的晚期肾细胞癌患者的一线治疗。
乳腺癌用药
47. 曲妥珠单抗 trastuzumab
制剂与规格:注射剂:440mg(20ml) /瓶
适应证:1).复发转移性乳腺癌:本品适用于 HER2 阳性转移性乳腺癌,单药用于已接受过多个化疗方案的转移性乳腺癌;与 紫杉醇或多西他赛等化疗药物联合,用于未接受化疗的转移 性乳腺癌患者。2).乳腺癌辅助治疗:本品适用于肿瘤直径> 0.5cm 的 HER2 阳性可手术乳腺癌的辅助治疗;对肿瘤直径<0.5cm 浸 润性乳腺癌,需要结合其他因素考虑是否使用。曲妥珠单抗 一般不与蒽环类药物联合使用,但可序贯使用;可与紫杉类 及其他(环磷酰胺、卡铂等)化疗药物合用,还可与放疗、 辅助内分泌治疗同时使用。3).乳腺癌新辅助治疗:与化疗联合新辅助治疗,继以辅 助治疗,用于局部晚期(包括炎性)的 HER2 阳性乳腺癌。 术后继续使用曲妥珠单抗总疗程为 1 年。
48. 拉帕替尼 lapatinib
制剂与规格:片剂:0.25g
适应证:拉帕替尼与卡培他滨联用,适用于 HER2 过表 达且既往接受过包括蒽环类、紫杉类和曲妥珠单抗治疗的晚 期或者转移性乳腺癌患者的治疗
49. 吡咯替尼 pyrotinib
制剂与规格:片剂:80mg、 160mg
适应证:吡咯替尼联合卡培他滨,适用于治疗 HER2 阳性、既往未接受或接受过曲妥珠单抗的复发或转移性乳腺癌患者。使用吡咯替尼前患者应接受过蒽环类或紫杉类化疗。 该适应证是基于一项 128 例既往接受或未接受过曲妥珠单抗 治疗的复发或转移性乳腺癌的Ⅱ期临床试验的结果给予的 有条件批准。该适应证的完全批准取决于正在进行的确证性 试验证实本品在该人群中的临床获益。
50. 帕妥珠单抗 pertuzumab
制剂与规格:注射液:420mg(14ml)/瓶
适应证:1).乳腺癌辅助治疗:本品与曲妥珠单抗和化疗联合,用 于高复发风险的 HER2 阳性早期乳腺癌患者的辅助治疗。帕妥珠单抗与曲妥珠单抗联合,还可与辅助内分泌治疗同时使 用。2).乳腺癌新辅助治疗:本品与曲妥珠单抗和化疗联合, 用于 HER2 阳性、局部晚期、炎性或早期乳腺癌患者(肿瘤 直径>2cm 或淋巴结阳性)的新辅助治疗。3).复发转移性乳腺癌治疗:本品与曲妥珠单抗和紫杉类 化疗药联合用于 HER2 阳性、转移性或不可切除的局部复发性乳腺癌患者。患者既往针对转移性疾病应未接受过抗 HER2 治疗,或既往辅助治疗阶段接受过抗 HER2 治疗,停止抗 HER2 治疗后一年以上复发转移的患者。
51. 哌柏西利 palbociclib
制剂与规格:胶囊:75mg、 100mg、 125mg
适应证:本品适用于激素受体(HR)阳性、 HER2 阴性的 局部晚期或转移性乳腺癌:1)与芳香化酶抑制剂联合使用, 作为绝经后女性患者的初始内分泌治疗。鉴于芳香化酶抑制 剂的作用机制,绝经前/围绝经期女性接受哌柏西利与芳香 化酶抑制剂联合治疗时,必须进行卵巢切除或使用促黄体生 成激素释放激素(LHRH)激动剂抑制卵巢功能。2)与氟维 司群联合使用治疗内分泌治疗后进展的转移性乳腺癌女性 患者。哌柏西利联合氟维司群用于绝经前/围绝经期女性, 需要与 LHRH 激动剂联合用药。3)男性乳腺癌:2019 年 4 月 4 日, FDA 批准了美国哌柏西利 HR 阳性、 HER2 阴性晚期 男性乳腺癌的适应证。
皮肤及软组织肿瘤用药
52. 伊马替尼 imatinib
制剂与规格:(1)片剂:100mg、 400mg;( 2)胶囊:100mg
适应证:对不能切除和/或转移性 KIT 突变的恶性黑色 素瘤患者。
53. 维莫非尼 vemurafenib
制剂与规格:片剂:240mg
适应证:经国家药品监督管理局批准的检测方法确定的 BRAFV600 突变阳性的不可切除或转移性黑色素瘤。
54. 帕博利珠单抗 pembrolizumab
制剂与规格:注射液:100mg(4ml) /瓶
适应证:适用于经一线治疗治疗失败的不可切除或转移性黑色素瘤的治疗。
55. 特瑞普利单抗 toripalimab
制剂与规格:注射液:240mg(6ml) /瓶
适应证:适用于既往接受全身系统治疗失败的不可切除 或转移性黑色素瘤的治疗。
56. 依维莫司 everolimus
制剂与规格:片剂:2.5mg、 5mg、 10mg
适应证:1).需要治疗干预但不适于手术切除的结节性硬化症 ( TSC)相关的室管膜下巨细胞星形细胞瘤( SEGA)成人和 儿童患者。
2).用于治疗不需立即手术治疗的结节性硬化症相关的肾血管平滑肌脂肪瘤(TSC-RAML)成人患者。
头颈部肿瘤用药
57. 尼妥珠单抗 nimotuzumab
制剂与规格:注射液:50mg(10ml) /瓶
适应证:与放疗联合治疗 EGFR 基因阳性表达的Ⅲ~Ⅳ 期鼻咽癌。
58. 索拉非尼 sorafenib
制剂与规格:片剂:200mg
适应证:治疗局部复发或转移的进展性的放射性碘难治性分化型甲状腺癌。
生殖系统肿瘤用药
59. 奥拉帕利 olaparib
制剂与规格:片剂:100mg、 150mg
适应证:铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗。
参考文献:
新型抗肿瘤药物临床应用指导原则(2019年版)[J].
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









有收获
106
#临床应用#
28
#肿瘤药物#
48
#肿瘤药#
48
#抗肿瘤药#
44