Alynlam的RNAi药物lumasiran治疗原发性高草酸尿症,完成向欧盟和美国的申请
2020-04-08 MedSci原创 MedSci原创
如果获得批准,lumasiran将成为1型原发性高草酸尿症(PH1)患者的首个治疗药物。
Alnylam公司针对超级罕见遗传性疾病--1型原发性高草酸尿症(PH1)的RNAi药物lumasiran,已经完成了向美国和欧洲的申请。
该公司表示,已经完成了向美国食品药品监督管理局(FDA)的滚动申请,并向欧洲药品管理局(EMA)提出了使用RNAi治疗剂的销售授权申请。
lumasiran是一种皮下注射的RNAi药物,利用Alnylam公司最新的ESC-GalNAc递送平台开发,能够降低肝脏中乙醇酸氧化酶的水平,从而消耗生成草酸所需的基质,减少草酸生成。
该公司表示,如果获得批准,lumasiran将成为PH1患者的首个治疗药物。
这些申请是基于关键的ILLUMINATE-A III期研究数据,lumasiran达到了所有主要和次要终点,尿草酸盐的排泄量显着减少,并"具有令人鼓舞的安全性和耐受性"。
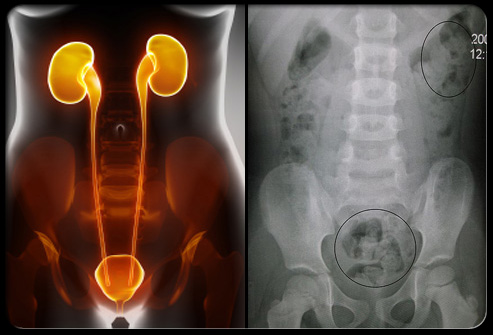
PH1的特征是草酸盐产量过多导致肾结石疼痛和复发。这种过量的草酸盐会导致肾脏功能受损,引起草酸盐晶体在骨骼、眼睛、皮肤和心脏中积聚,从而导致严重的疾病和死亡。
原始出处:
http://www.pharmatimes.com/news/alynlam_completes_eu,_us_filings_for_lumasiran_1337932
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#RNAi#
35
#LAM#
23
#原发性#
19
#RNAi药物lumasiran#
27
#RNAi药物#
45